Клінічна настанова: ХОЗЛ. Діагностика
Дата публікації: 15.11.2023
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: діагностика, ХОЗЛ, клінічна настанова
Хронічне обструктивне захворювання легень (ХОЗЛ) – це поширений респіраторний стан, що характеризується кашлем, задишкою та обмеженням повітряного потоку. Приблизно 10 відсотків осіб у віці 40 років і старше мають ХОЗЛ, хоча поширеність різна в різних країнах і зростає з віком. ХОЗЛ незмінно входить до числа головних причин смерті в Сполучених Штатах, щороку вбиваючи понад 120 000 людей; до пандемії COVID-19 (коронавірусна хвороба 2019 р.) це була третя основна причина у світі. Як наслідок його високої поширеності та хронізації, ХОЗЛ спричиняє високе використання ресурсів із частими візитами клініциста, численні госпіталізації через гострі загострення та потребу в хронічній терапії.
Долучайтесь до перегляду Ukrainian Family Medicine Week: попередити легше, ніж лікувати
Встановлення правильного діагнозу ХОЗЛ є важливим, оскільки належне лікування може зменшити симптоми (особливо задишку), зменшити частоту та тяжкість загострень, покращити стан здоров’я, підвищити фізичну здатність і продовжити виживання. Багато станів здоров’я у людей похилого віку можуть призвести до задишки або кашлю, тому респіраторні симптоми не слід пов’язувати з ХОЗЛ без належного обстеження та діагностики.
ВИЗНАЧЕННЯ
ХОЗЛ слід розуміти в контексті інших тісно пов’язаних звичайних респіраторних захворювань (емфізема, хронічний бронхіт і хронічна обструктивна астма), які представляють перекриваючий спектр захворювань дихальних шляхів.
Глобальна ініціатива з хронічної обструктивної хвороби легень (GOLD), проект, ініційований Національним інститутом серця, легенів і крові (NHLBI) і Всесвітньою організацією охорони здоров’я (ВООЗ), визначає ХОЗЛ як «гетерогенний стан легенів, що характеризується хронічним респіраторні симптоми (задишка, кашель, виділення мокротиння, загострення) внаслідок аномалій дихальних шляхів (бронхіт, бронхіоліт) та/або альвеол (емфізема), які спричиняють стійку, часто прогресуючу, обструкцію повітряного потоку».
На практиці діагностика ХОЗЛ вимагає всього наступного:
● Наявність легеневих симптомів (задишка, кашель або виділення мокротиння).
● Відповідний клінічний контекст (особливо, але не виключно, вплив тютюну).
● Докази обмеження повітряного потоку.
Хронічний бронхіт — хронічний бронхіт визначається як хронічний продуктивний кашель протягом певного періоду, як правило, щонайменше три місяці протягом кожного з двох послідовних років, у пацієнта, у якого інші причини хронічного кашлю (наприклад, бронхоектатична хвороба) були виключені. Це може передувати або слідувати за розвитком обмеження повітряного потоку. Це визначення використовувалося в багатьох дослідженнях, незважаючи на довільно обрану тривалість симптомів. У віці від 35 до 40 років у курців сигарет може розвинутися хронічний бронхіт і початися періодичні загострення симптомів навіть за відсутності обструкції повітряного потоку.
Емфізема. Емфізема описує розширення дихальних просторів дистально від термінальних бронхіол, що супроводжується руйнуванням стінок дихальних шляхів, патологічне явище, яке часто спостерігається у пацієнтів із ХОЗЛ. Ця знахідка клінічно проявляється ослабленням дихальних шумів і ознаками гіперінфляції легень під час обстеження або візуалізації; це часто асоціюється з задишкою. Емфізема класично не супроводжується макроскопічним фіброзом. Хоча емфізема може існувати в осіб, які не мають обмеження дихального потоку, вона частіше зустрічається серед пацієнтів із помірною або важкою обструкцією дихального потоку.
Обмеження повітряного потоку — обмеження повітряного потоку фізіологічно визначається як аномально знижена здатність до ефективного видиху. Тяжкість і наявність обмеження повітряного потоку визначають шляхом оцінки об’єму форсованого видиху за одну секунду (ОФВ 1) і співвідношення ОФВ 1 до загального об’єму форсованого видиху (він же форсована життєва місткість видиху [ФЖЕЛ]).
Обмеження потоку повітря може бути фіксованим або змінюватися у відповідь на зовнішні фактори (наприклад, вплив навколишнього середовища, температура та ліки). Астма визначається значною варіабельністю обструкції повітряного потоку, тоді як ХОЗЛ характеризується обструкцією, яка не є повністю оборотною за допомогою ліків.
Астма — Глобальна ініціатива з астми (GINA) дає наступне визначення астми: «Астма — це хронічне запальне захворювання дихальних шляхів, яке призводить до повторюваних епізодів хрипів, задишки, стиснення в грудях і кашлю. Ці епізоди пов’язані з широко поширеними, але змінна обструкція повітряного потоку, яка часто є оборотною спонтанно або після лікування». Епізодичний характер симптомів і оборотність обструкції повітряного потоку є клінічними ознаками, які допомагають відрізнити астму від ХОЗЛ. Однак у дорослих із тривалою астмою може розвинутися стійке обмеження повітряного потоку. Відрізнити цих пацієнтів від хворих на ХОЗЛ важко, особливо в контексті додаткових факторів ризику ХОЗЛ.

Взаємозв’язок між цими захворюваннями. Хронічний бронхіт та емфізема раніше були включені у визначення ХОЗЛ, і їх клінічні ознаки збігаються з характеристиками пацієнтів з астмою та ХОЗЛ. Це спричинило значну плутанину щодо належної класифікації пацієнтів із респіраторними симптомами та факторами ризику ХОЗЛ. Важливі моменти щодо цих взаємозв’язків включають:
● ХОЗЛ – пацієнти з емфіземою або хронічним бронхітом і стійким постбронходилататорним обмеженням повітряного потоку відповідають визначенню ХОЗЛ. Хронічний бронхіт, емфізема та постбронходилататорне обмеження повітряного потоку зазвичай виникають разом.
● Астма. Пацієнти з астмою, які мають лише викликану обструкцію дихальних шляхів або чиє обмеження повітряного потоку повністю оборотне за допомогою бронходилататорної терапії, не вважаються хворими на ХОЗЛ.
● Астма та ХОЗЛ. Пацієнти з астмою, у яких обмеження повітряного потоку не проходить повністю та які мають інші відповідні клінічні фактори ризику (наприклад, старший вік, історія контакту з іншими речовинами), вважаються хворими на астму та ХОЗЛ. Етіологія та патогенез ХОЗЛ у таких пацієнтів може відрізнятися від інших хворих на ХОЗЛ. Хоча дескриптори «перекриття астми та ХОЗЛ (ACO)» і «ХОЗЛ-А» були запропоновані для ідентифікації пацієнтів із захворюванням дихальних шляхів, які мають ознаки як астми, так і ХОЗЛ, ця тема залишається суперечливою. Єдиного, загальноприйнятого визначення не виникло. Центральними для більшості запропонованих визначень є вік >40 років, анамнез астми в молодшому віці, стійка постбронходилататорна обструкція повітряного потоку та докази часткової бронходилататорної оборотності.
Потрібне буде подальше вивчення цього зв’язку, щоб з упевненістю визначити, як адаптувати алгоритми лікування до цих пацієнтів. Література, що розвивається, передбачає диференціальну реакцію на інгаляційні глюкокортикоїди у пацієнтів із або без підвищеної кількості циркулюючих еозинофілів. GOLD і наші автори рекомендують периферичну еозинофілію для клінічного використання для фармакотерапії у всіх пацієнтів із ХОЗЛ.
Підгрупи пацієнтів з ХОЗЛ з еозинофілією можуть відчути клінічне покращення за допомогою біологічних препаратів, які показали користь при астмі.
● Перед ХОЗЛ – пацієнти з хронічним бронхітом або емфіземою без необоротної обструкції дихальних шляхів не мають ХОЗЛ, але мають високий ризик розвитку захворювання. Термін «пре-ХОЗЛ» використовується для ідентифікації таких осіб, які мають або респіраторні симптоми, рентгенологічні аномалії, що відповідають ХОЗЛ, або ранні зміни функції легень у контексті факторів ризику ХОЗЛ, але не мають обструкції дихальних шляхів, як це визначено ОФВ 1/ ФЖЕЛ. <0,7. Немає повного консенсусу щодо визначальних ознак пре-ХОЗЛ, але були запропоновані діагностичні критерії.

Епідеміологічні дослідження свідчать про те, що майже 50 відсотків теперішніх і колишніх курців без обструкції дихальних шляхів мають респіраторні симптоми, які корелюють зі зниженою фізичною здатністю, рентгенологічною емфіземою та потовщенням стінки, а також функцією легенів на нижній межі нормального діапазону. Незважаючи на те, що багато з цих пацієнтів лікуються бронходилататорами або інгаляційними глюкокортикоїдами не за призначенням, одне велике дослідження не продемонструвало покращення респіраторних симптомів або якості життя за допомогою подвійної терапії бронходилататорами тривалої дії (індакатерол-глікопіролат) порівняно з плацебо в цій популяції. Отже, існуючі дані не підтверджують терапію інгаляційними бронходилататорами для симптоматичних пацієнтів без обмеження дихальних шляхів. Необхідне додаткове дослідження для визначення відповідної профілактичної та підтримуючої терапії для цієї популяції.
● Інші захворювання дихальних шляхів. Пацієнти з обмеженням повітряного потоку внаслідок захворювань відомої етіології або специфічної патології (наприклад, муковісцидоз, бронхоектатична хвороба, облітеруючий бронхіоліт) не вважаються хворими на ХОЗЛ. Однак ці винятки визначені досить вільно.
ПАТОЛОГІЯ
У пацієнтів із ХОЗЛ гістологію не беруть як частину діагностичного обстеження. Переважні патологічні зміни при ХОЗЛ виявляються в дихальних шляхах, але також спостерігаються зміни в легеневій паренхімі та легеневій судинній системі. У конкретної людини характер патологічних змін залежить від особливостей основного захворювання (наприклад, хронічний бронхіт, емфізема, дефіцит альфа-1 антитрипсину), генетичної схильності та тяжкості захворювання. У той час як рентгенографічні методи не мають роздільної здатності гістології, комп’ютерна томографія високої роздільної здатності (HRCT) може оцінити легеневу паренхіму, дихальні шляхи і легеневу васкулатуру.
Патологічні особливості ХОЗЛ (за компартментами) включають:
● Дихальні шляхи. У дихальних шляхах ХОЗЛ призводить до хронічного запалення, збільшення кількості келихоподібних клітин, гіперплазії слизових залоз, фіброзу, а також до звуження та втрати дрібних дихальних шляхів. Крім того, колапс дихальних шляхів часто виникає через втрату прив’язки, спричинену емфізематозним руйнуванням альвеолярних стінок. У пацієнтів з хронічним бронхітом, у яких спостерігається гіперсекреція слизу, зазвичай спостерігається збільшення кількості келихоподібних клітин і збільшення підслизових залоз.
Хронічне запалення дихальних шляхів при хронічному бронхіті та емфіземі часто характеризується наявністю CD8+ T-лімфоцитів, нейтрофілів і CD68+ моноцитів/макрофагів. Для порівняння, бронхіальне запалення при астмі частіше характеризується наявністю CD4+ Т-лімфоцитів, еозинофілів і підвищенням інтерлейкіну (IL)-4 та IL-5. Однак ці знахідки не є діагностичними, оскільки може існувати значне збігання цих фенотипів запалення дихальних шляхів у окремих пацієнтів.
● Паренхіма легенів. Емфізема вражає структури, розташовані дистальніше кінцевої бронхіоли, що складається з респіраторних бронхіол, альвеолярних проток, альвеолярних мішечків і альвеол, відомих разом як ацинус. Ці структури в поєднанні з пов’язаними з ними капілярами та інтерстицієм утворюють легеневу паренхіму. Частина ацинуса, уражена постійним розширенням або деструкцією, визначає підтип емфіземи.
- Проксимальна ацинарна (також відома як центрілобулярна) емфізема належить до аномального розширення або руйнування респіраторної бронхіоли, центральної частини ацинуса. Це зазвичай асоціюється з курінням сигарет і є найпоширенішим підтипом емфіземи, який спостерігається у пацієнтів із ХОЗЛ. Центрілобулярна емфізема також спостерігається при пневмоконіозах вугільних робітників.
- Панацинарна емфізема належить до розширення або руйнування всіх частин ацинуса. Дифузна панацинарна емфізема є характерною ознакою дефіциту альфа-1 антитрипсину, хоча її можна спостерігати в поєднанні з проксимальною ацинарною емфіземою в інших пацієнтів із ХОЗЛ.
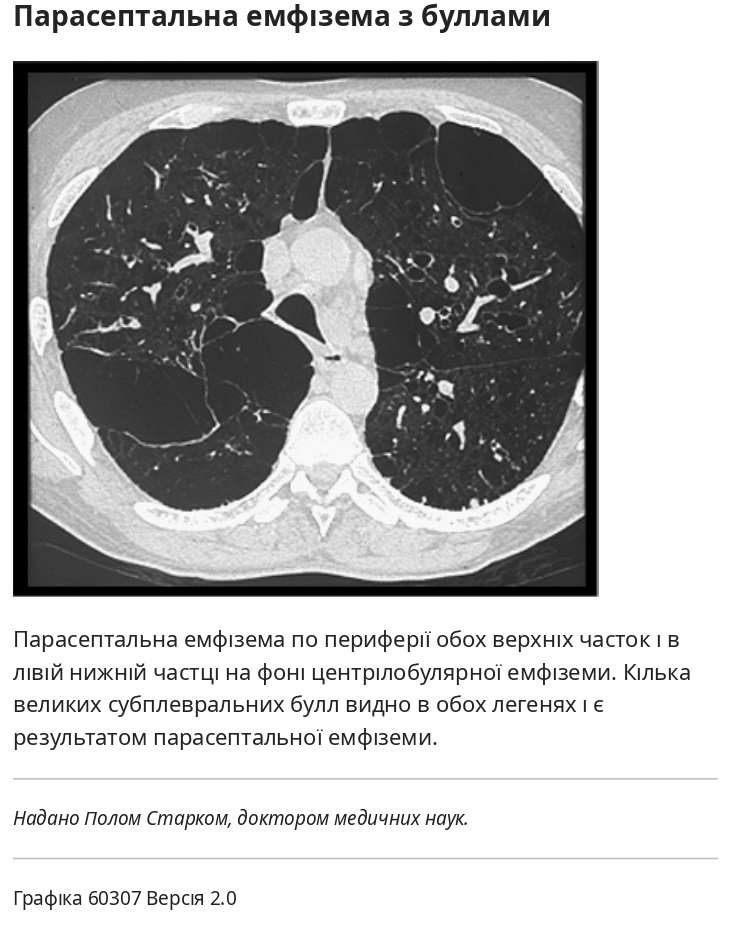
- При дистальній ацинарній (також відомій як парасептальна) емфіземі переважно уражаються альвеолярні протоки. Дистальна ацинарна емфізема може виникати окремо або в поєднанні з проксимальною ацинарною та панацинарною емфіземою. Коли вона виникає самостійно, широка субплевральна парасептальна емфізема може бути пов’язана зі спонтанним пневмотораксом, але в інших випадках вона не має клінічного значення.
● Легенева васкулатура – зміни в легеневій васкулатурі при ХОЗЛ включають гіперплазію інтими та гіпертрофію/гіперплазію гладкої мускулатури, які, як вважають, є результатом хронічної гіпоксичної вазоконстрикції малих легеневих артерій.

КЛІНІЧНА ПРЕЗЕНТАЦІЯ
Симптоми та характер початку — три основні симптоми ХОЗЛ: задишка, хронічний кашель і виділення мокротиння; найпоширенішим раннім симптомом є задишка при фізичному навантаженні. Менш поширені симптоми включають хрипи та стиснення в грудях. Однак будь-який з цих симптомів може розвиватися самостійно і з різною інтенсивністю.
Існують різні способи, за допомогою яких пацієнти з ХОЗЛ звертаються:
● Пацієнти, які ведуть дуже малорухливий спосіб життя, але мають мало скарг. Ці пацієнти потребують ретельного опитування, щоб отримати анамнез, який свідчить про ХОЗЛ. Деякі пацієнти несвідомо уникають задишки при фізичному навантаженні, змінюючи свої очікування та обмежуючи свою активність. Вони можуть не знати про ступінь своїх обмежень або про те, що їх обмеження спричинені респіраторними симптомами, хоча вони можуть скаржитися на втому.
● Пацієнти, у яких спостерігається прогресуюча задишка та хронічний кашель. У цих пацієнтів задишка спочатку може спостерігатися лише під час фізичного навантаження. Однак згодом це стає помітним при поступовому зменшенні навантаження або навіть у спокої. Хронічний кашель характеризується прихованим початком виділення мокротиння, яке спочатку відбувається вранці, але може прогресувати протягом дня. Добовий обсяг мокротиння рідко перевищує 60 мілілітрів. Мокрота зазвичай слизова, але під час загострень стає більш гнійною.
● Пацієнти з періодичними легеневими симптомами та ознаками – ці пацієнти мають мінімальні симптоми на початку, але епізодично розвиваються деякі з наступного: кашель, гнійне мокротиння, хрипи, втома та задишка. Як правило, інтервал між загостреннями зменшується в міру наростання тяжкості ХОЗЛ. Цей симптомокомплекс може бути діагностичною проблемою через збіг з іншими поширеними хронічними захворюваннями. Наприклад, поєднання періодичних хрипів і задишки може призвести до неправильного діагнозу астми. І навпаки, інші захворювання з подібними епізодичними проявами (наприклад, серцева недостатність, бронхоектатична хвороба, бронхіоліт) часто неправильно діагностуються як загострення ХОЗЛ.Приблизно 62 відсотки пацієнтів із помірним та тяжким ХОЗЛ повідомляють про варіабельність симптомів (наприклад, задишка, кашель, мокротиння, хрипи або стиснення в грудях) протягом дня або тижня; ранок зазвичай є найгіршим часом дня.
Пацієнти з ХОЗЛ можуть відчувати збільшення ваги (через обмеження активності), втрату ваги (можливо, через задишку під час їжі або посилення метаболічної роботи дихання), обмеження активності (включаючи сексуальну), кашель, синкопе або відчуття депресії чи тривоги. Втрата ваги, як правило, свідчить про прогресуючу хворобу та пов’язана з гіршим прогнозом.
До коморбідних захворювань, які можуть супроводжувати ХОЗЛ, належать рак легенів, бронхоектатична хвороба, серцево-судинні захворювання, остеопороз, метаболічний синдром, слабкість скелетних м’язів, тривога, депресія та когнітивна дисфункція. Пацієнти також можуть повідомити про сімейну історію ХОЗЛ або інших хронічних респіраторних захворювань.
Фактори ризику, включаючи куріння та інгаляційний вплив. Для пацієнтів із респіраторними симптомами важливо оцінити генетичні фактори, фактори ризику розвитку та навколишнього середовища, які можуть сприяти розвитку ХОЗЛ. Дедалі більше визнання цих різноманітних факторів ризику, крім паління, призвело до запропонованої таксономії «етіотипів» ХОЗЛ. Розуміння переважної етіології захворювання у конкретного пацієнта може дозволити більш цілеспрямоване зниження ризику.
Найбільш поширеним фактором ризику ХОЗЛ є куріння. Інші види впливу, включаючи використання пасивного диму та біомаси, також відіграють значну роль у всьому світі.
● Стаж паління – кількість і тривалість куріння сприяють тяжкості захворювання. Таким чином, ключовим кроком в оцінці пацієнтів з підозрою на ХОЗЛ є визначення кількості викурених пачок-років (пачок сигарет на день, помножених на кількість років). Історія куріння повинна містити вік початку куріння та вік відмови від куріння, оскільки пацієнти можуть недооцінювати кількість років куріння. При достатньому курінні майже всі курці розвинуть помітно знижену функцію легенів. У той час як дослідження показали загальну «криву доза-відповідь» для куріння та функції легенів, у деяких людей важке захворювання розвивається з меншою кількістю пако-років, а інші мають мінімальні або відсутні симптоми, незважаючи на багато пако-років.
Точний поріг для тривалості/інтенсивності паління сигарет, що призведе до ХОЗЛ, різниться від однієї людини до іншої. За відсутності додаткової генетичної/екологічної/професійної схильності куріння менше ніж 10-15 пачок років сигарет навряд чи призведе до ХОЗЛ.
● Історія впливу випаровування і пилу – Історія навколишнього середовища/професійна історія може виявити інші важливі фактори ризику ХОЗЛ, такі як вплив випаровувань або органічного або неорганічного пилу, включаючи дим побутової біомаси. Ці впливи допомагають пояснити значну меншість пацієнтів із ХОЗЛ, які ніколи не курили.
● Інші фактори ризику. Відомо, що деякі легеневі та системні інфекції спричиняють постійні структурні зміни в легенях, які сприяють ХОЗЛ. Зокрема, дитячі пневмонії, туберкульозна інфекція та вірус імунодефіциту людини (ВІЛ) асоціюються з високим ризиком подальшого розвитку ХОЗЛ. Подібним чином передчасні пологи та астма в ранньому віці можуть вплинути на розвиток легенів і збільшити ризик ХОЗЛ. Астму в анамнезі також важливо виявити, оскільки погано контрольована астма в дорослому віці може прогресувати до фіксованого обмеження повітряного потоку та ХОЗЛ. Сильна сімейна історія ХОЗЛ або інших хронічних респіраторних захворювань, особливо в ранньому віці, може свідчити про генетичну схильність до ХОЗЛ.

Фізичне обстеження — результати фізичного обстеження грудної клітки залежать від тяжкості ХОЗЛ.
● Легке захворювання – при легкому перебігу захворювання фізикальне обстеження може бути нормальним. Тонкі підказки включають подовжений час видиху та слабкі хрипи в кінці видиху під час форсованого видиху.
● Захворювання середнього та тяжкого ступеня – у міру збільшення тяжкості обструкції дихальних шляхів фізичне обстеження може виявити гіперінфляцію (наприклад, посилення резонансу перкусії), ослаблення дихальних шумів, хрипи, хрипи в основі легенів та/або віддалені тони серця. Ознаки тяжкого захворювання включають збільшення передньо-заднього діаметра грудної клітки («бочкоподібна» грудна клітка) та вдавлену діафрагму з обмеженими рухами на підставі перкусії грудної клітки.
● Термінальна стадія захворювання та хронічна дихальна недостатність. Пацієнти з термінальною стадією ХОЗЛ можуть приймати положення, які полегшують задишку, наприклад, нахилитися вперед із витягнутими руками та опорою на долоні або лікті. Ця поза може бути очевидною під час обстеження або про неї може свідчити наявність мозолів або набряклих бурс на розгинальних поверхнях передпліч. Інші дані фізичного обстеження включають використання допоміжних дихальних м’язів шиї та плечового поясу, видих через стиснуті губи, парадоксальне втягнення нижніх проміжків під час вдиху (тобто ознака Гувера), ціаноз, астериксис через важку гіперкапнію, а також збільшену, ніжну печінку внаслідок серцевої недостатності. Розтягнення шийних вен також може спостерігатися через підвищення внутрішньогрудного тиску, особливо під час видиху.
● Додаткові ознаки – Жовті плями на пальцях через нікотин і смолу від спаленого тютюну є підказкою до постійного та інтенсивного куріння сигарет. Булини пальців не є типовими для ХОЗЛ (навіть із супутньою гіпоксемією). Його наявність свідчить про такі супутні захворювання, як рак легенів, інтерстиціальне захворювання легень або бронхоектатична хвороба.
ДІАГНОСТИЧНА ОЦІНКА
Кого обстежити ? Подальше діагностичне обстеження ХОЗЛ доцільне у дорослих, які повідомляють про задишку, хронічний кашель або хронічне виділення мокротиння, або у яких спостерігалося поступове зниження рівня активності, особливо якщо вони мають фактори ризику ХОЗЛ (наприклад, куріння сигарет, дим внутрішньої біомаси). Дорослим без будь-яких симптомів не слід проходити подальше тестування на ХОЗЛ.
Деякі пацієнти зі значною симптоматикою ХОЗЛ не повідомляють про ці симптоми лікарям. Ми погоджуємося з Глобальною ініціативою з хронічної обструктивної хвороби легенів (GOLD) у відстоюванні активного виявлення випадків серед груп ризику. Анкета CAPTURE (Оцінка хронічного обструктивного захворювання легень у первинній медичній допомозі для виявлення недіагностованих респіраторних захворювань і ризику загострення) є добре перевіреним інструментом, який може допомогти виявити пацієнтів із прихованими симптомами, яким, ймовірно, допоможе терапія ХОЗЛ та тому будуть кандидатами на діагностичну оцінку за допомогою спірометрії. Примітно, що в одному великому дослідженні його використання як інструменту скринінгу клінічно значущого ХОЗЛ у популяції первинної медичної допомоги опитувальник CAPTURE продемонстрував чутливість 48 відсотків, специфічність 89 відсотків, позитивну прогностичну цінність 10 відсотків і кількість необхідних для скринінгу 82.
Базуючись як на аналітичному аналізі результатів скринінгового дослідження CAPTURE, так і на підвищенні уваги до симптомів, а не обмеження повітряного потоку як рушійної сили терапевтичних стратегій, використання CAPTURE без вимірювання пікового потоку може ідентифікувати пацієнтів, які підходять для подальшого лікування. оцінка та терапія. Пацієнти з результатом опитування від 0 до 2 мають менший ризик, тоді як пацієнти з балами від 3 до 6 повинні пройти спірометричне обстеження.
Поточні рекомендації не підтримують популяційний скринінг безсимптомних дорослих на ХОЗЛ за допомогою спірометрії, оскільки безсимптомна легка обструкція повітряного потоку не потребує лікування. Безсимптомні та некурящі особи з легкою обструкцією повітряного потоку, але без анамнезу астми, не мають такого ж прогресуючого зниження функції легень, яке спостерігається серед осіб, які мають подібний ступінь обструкції повітряного потоку та мають симптоми або продовжують палити.
Як оцінити — Пацієнти з ризиком розвитку ХОЗЛ повинні пройти обстеження за допомогою спірометрії; ми також зазвичай проводимо лабораторні аналізи на задишку (наприклад, загальний аналіз крові, тиреотропний гормон, N-кінцевий прогормон головного натрійуретичного пептиду [BNP]) і рентгенограму грудної клітки для оцінки інших захворювань серця та легенів.
Спірометрія — Спірометрія потрібна для встановлення діагнозу ХОЗЛ. Під час обстеження пацієнта щодо можливого ХОЗЛ ми проводимо спірометрію до та після введення бронходилататора, щоб визначити, чи є обмеження повітряного потоку та чи є воно частково або повністю оборотним. Обмеження повітряного потоку, яке є необоротним або лише частково оборотним при лікуванні бронходилататорами, є визначальною фізіологічною ознакою ХОЗЛ. Найважливішими значеннями, які вимірюють під час спірометрії, є об’єм форсованого видиху за одну секунду (FEV1) і форсована життєва ємність крові (FVC). Постбронходилататорне співвідношення ОФВ 1 /ФЖЕЛ визначає наявність необоротного обмеження повітряного потоку; прогнозоване значення відсотка постбронходилататора для ОФВ 1 визначає тяжкість обмеження повітряного потоку. Співвідношення FEV1 / FVC не використовується для визначення тяжкості обмеження повітряного потоку, оскільки FVC часто зменшується зі збільшенням обструкції через захоплення повітря або передчасне припинення видиху.
● Порогове значення для обмеження повітряного потоку – Ідеальний поріг для встановлення обмеження повітряного потоку при діагностиці ХОЗЛ емпірично не визначено. Ми погоджуємося з рекомендаціями GOLD, які підтримують просте та добре встановлене використання постбронходилататора FEV1 / FVC <0,7 як порогового значення для обмеження повітряного потоку.
Однак співвідношення ОФВ 1 /ФЖЕЛ зменшується з віком, тому використання нижньої межі норми (НМН) п’ятого процентиля співвідношення ОФВ 1 /ФЖЕЛ (або, що еквівалентно, z-показника -1,645), а не абсолютного значення <0,7 деякі обстоюють як роздільну точку для діагностики ХОЗЛ та інших обструктивних захворювань легень. На практиці несприятливі наслідки гіпердіагностики ХОЗЛ у людей похилого віку за допомогою фіксованого співвідношення дещо пом’якшуються перевіркою спірометрії лише у пацієнтів із симптомами та факторами ризику ХОЗЛ, але недостатня діагностика молодших людей із відхиленням від віку дихальних шляхів залишається проблемою.
● Альтернативи ОФВ 1 /ФЖЕЛ – об’єм форсованого видиху за шість секунд (ОФВ 6), отриманий шляхом зупинки видиху через шість секунд, а не після припинення потоку повітря, є прийнятним сурогатом для ФЖЕЛ. Переваги ОФВ 1 /ОФВ 6 включають менше розчарування пацієнтом і техніком, які намагаються досягти плато наприкінці тесту, меншу ймовірність синкопе, коротший час тестування та кращу повторюваність без втрати чутливості чи специфічності. Якщо використовується, LLN для ОФВ 1 / ОФВ 6 з Третього національного дослідження здоров’я та харчування (NHANES III) є прийнятним порогом для діагностики обмеження повітряного потоку. Рівняння спірометрії Global Lung Function Initiative (GLI) не включають контрольні значення ОФВ 6, тому цей метод не можна використовувати з програмним забезпеченням для спірометрії, яке базується на цих рівняннях.
Додаткове обстеження — за наявності хронічних респіраторних симптомів і відповідних факторів ризику спірометрія є єдиним обстеженням, необхідним для діагностики ХОЗЛ. Додаткове обстеження спрямоване на виключення альтернативних діагнозів.
● Лабораторні дослідження. Для пацієнтів із задишкою ми проводимо лабораторні дослідження як частину широкого обстеження потенційної етіології. Це часто включає повний аналіз крові для оцінки анемії, оцінку електролітів і функції нирок, рівень тиреотропного гормону та концентрацію BNP або N-кінцевого про-BNP (NT-proBNP) у плазмі як компонент оцінки. підозра на серцеву недостатність (СН).
● Рентгенограма грудної клітки – для пацієнтів із підозрою на ХОЗЛ ми зазвичай отримуємо рентгенограму грудної клітки для оцінки альтернативних паренхіматозних процесів і оцінки легеневих супутніх захворювань. Звичайна рентгенограма грудної клітки має низьку чутливість для виявлення ХОЗЛ. Наприклад, лише приблизно у половини пацієнтів із ХОЗЛ середнього ступеня тяжкості ідентифікують ХОЗЛ на звичайній рентгенограмі грудної клітки (тобто з чутливістю 50 відсотків).
Рентгенологічні ознаки, що вказують на ХОЗЛ (зазвичай спостерігається на пізніх стадіях захворювання), включають:
- Швидко звужуються судинні тіні, підвищена рентгенопрозорість легені, плоска діафрагма та довга вузька тінь серця на фронтальній рентгенограмі.
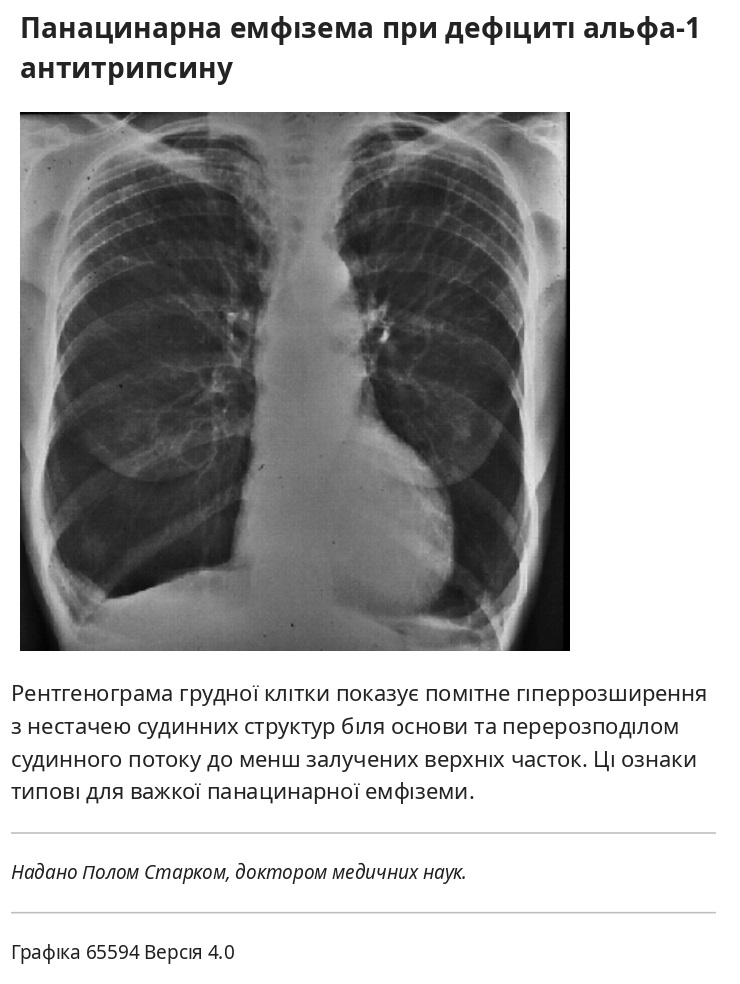
- На бічній рентгенограмі плоский контур діафрагми та збільшений загрудинний повітряний простір. Ці висновки зумовлені гіперінфляцією.
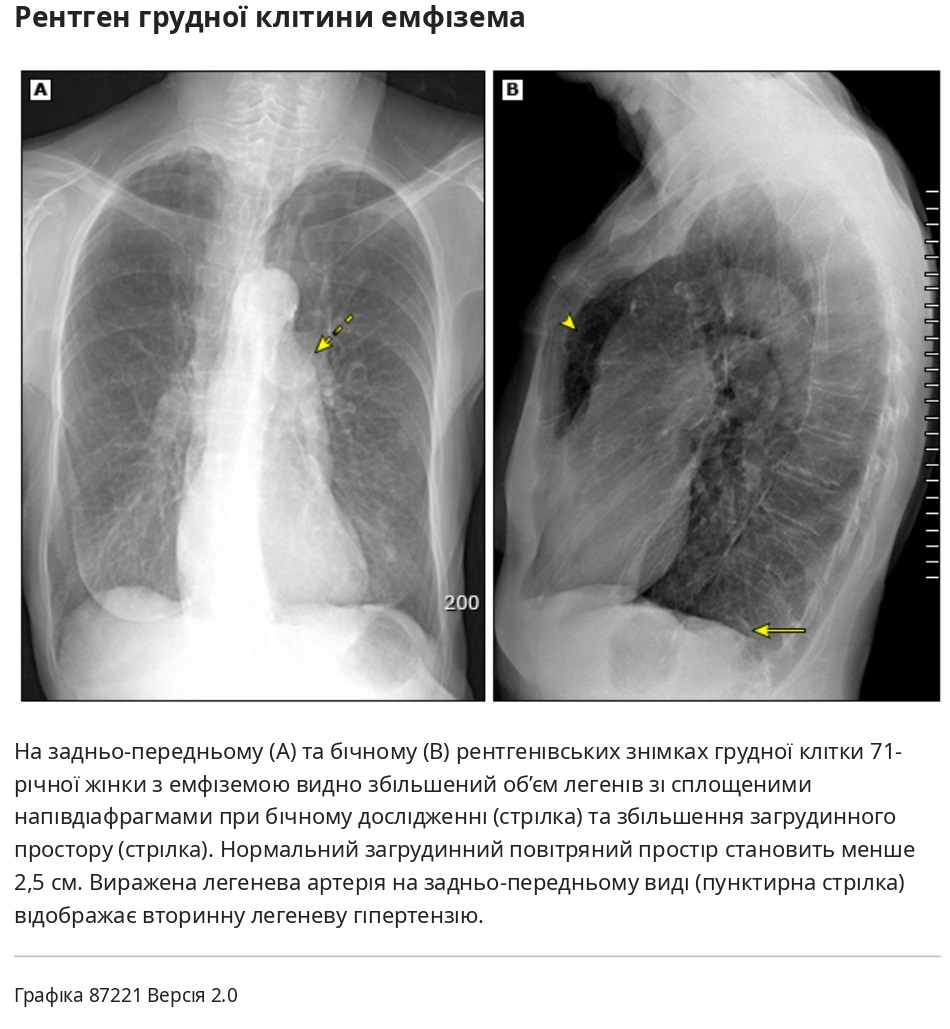
- Були визначаються як радіопрозорі ділянки діаметром понад один сантиметр, оточені дугоподібними тінями лінії волосся. Вони викликані місцевим важким захворюванням і можуть супроводжуватися або не супроводжуватися поширеною емфіземою.
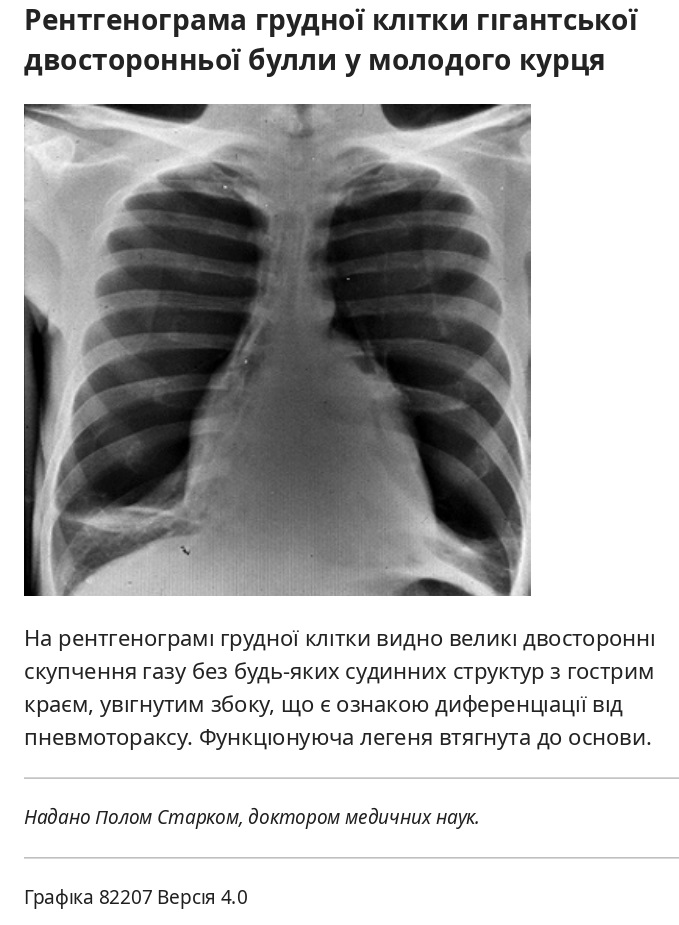
- Коли прогресуюча ХОЗЛ призводить до легеневої гіпертензії та легеневого серця, можуть спостерігатися виразні судинні тіні грудної клітки та втягнення тіні серця в ретростернальний простір. Збільшення серця може бути очевидним лише порівнюючи з попередніми рентгенограмами грудної клітки.
● Комп’ютерна томографія, для альтернативної діагностики або якщо спірометрія недоступна – є умови, де КТ грудної клітини є стандартним і доступним, тоді як спірометричне тестування може бути складним для проведення. КТ має більшу чутливість і специфічність, ніж стандартна рентгенографія грудної клітки для виявлення емфіземи. Особливо це стосується комп’ютерної томографії високої роздільної здатності (HRCT; тобто колімація від 1 до 2 мм). Експіраторне сканування, особливо коли використовується разом із інспіраторним скануванням, може допомогти оцінити ненемфізематозне захоплення повітря як сурогатний захід для невеликих аномалій дихальних шляхів
За відсутності інших результатів виявлена КТ емфізема, утримання повітря та ремоделювання дихальних шляхів, що залучає значну частину легенів, вказують на ХОЗЛ, і деякі виступають за ці результати як альтернативний діагностичний шлях. Оскільки спірометрія відіграє більшу роль у визначенні стадії захворювання, є більш економічно ефективною та дозволяє уникнути непотрібного радіаційного опромінення, ми не підтримуємо цей підхід, окрім випадків, коли неможливо отримати спірометрію.
КТ також може бути виконано, якщо симптоми або фізикальне обстеження вказують на потенційне ускладнення ХОЗЛ (наприклад, пневмонія, пневмоторакс, гігантські булли), є підозра на альтернативний діагноз (наприклад, тромбоемболічна хвороба) або показаний скринінг на рак легенів.
Певні ознаки комп’ютерної томографії можуть анатомічно охарактеризувати емфізему як центріацинарну (центрілобулярну), панацинарну або парасептальну, хоча це зазвичай не є необхідним для клінічного лікування:
- Центріацинарна емфізема виникає переважно у верхніх частках і утворює отвори в центрі вторинних легеневих часточок. Стінки емфізематозних просторів, як правило, непомітні, але центральні судини можуть бути видимими. Навпаки, стінки кіст при легеневому гістіоцитозі Лангерганса, іншому кістозному захворюванні легень у курців сигарет, товщі
- Панацинарна емфізема частіше вражає основи легенів і всю вторинну легеневу частку. Панацинарна емфізема може викликати генералізовану недостатність судинних структур. Серед пацієнтів з дефіцитом альфа-1 антитрипсину панацинарна емфізема є більш поширеною формою.
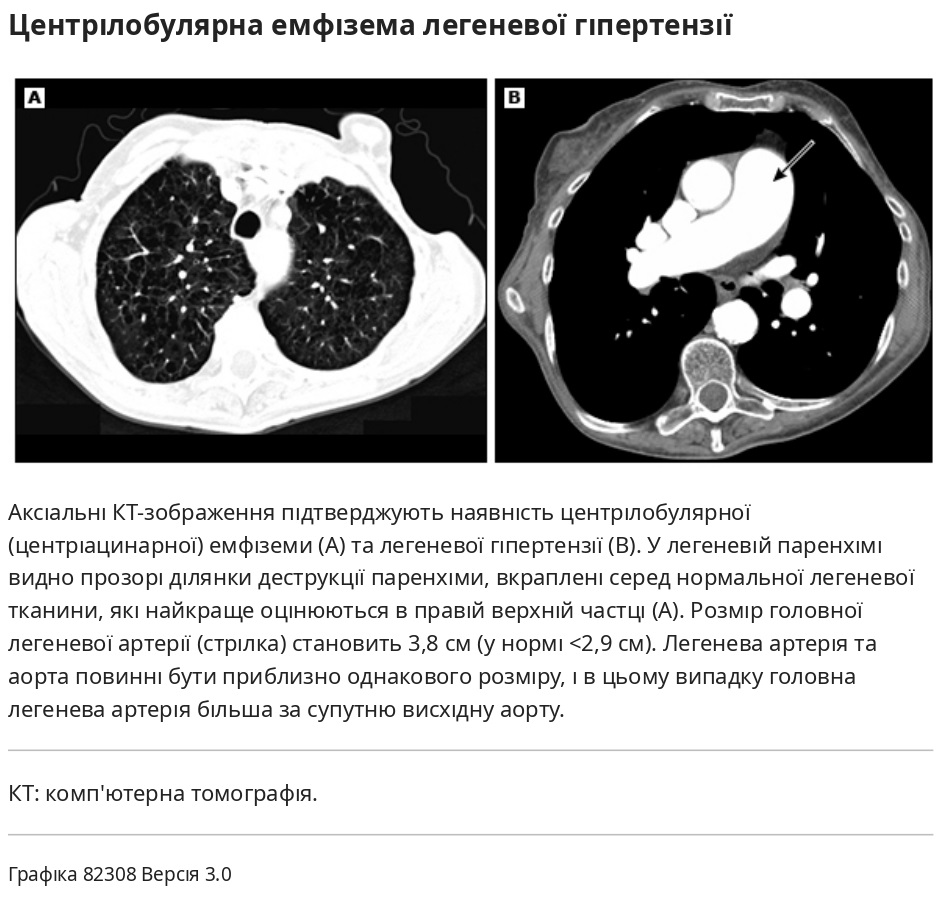
- Парасептальна (дистальна ацинарна) емфізема утворює невеликі субплевральні скупчення газу, розташовані на периферії вторинної легеневої частки
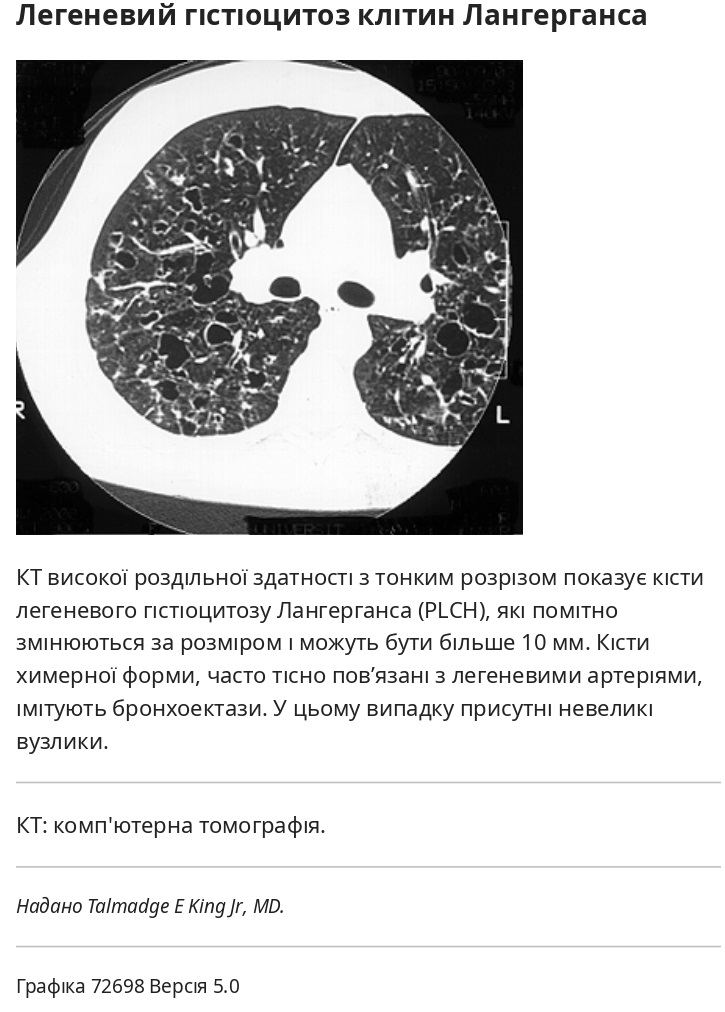
Новіші КТ-сканери з вищою роздільною здатністю та новими аналітичними методами можуть визначити розміри дихальних шляхів, хоча клінічне значення цих заходів не визначено. Подібним чином сканування з високою роздільною здатністю може виявити обрізання дистального судинного дерева, яке виникає внаслідок руйнування альвеол і пов’язаних з ними капілярних русл через емфізему. Кількісні параметри, засновані на щільності легенів, потовщенні стінки дихальних шляхів, дилатації дихальних шляхів і обрізанні судин, були встановлені для оцінки тяжкості емфіземи, захворювання дихальних шляхів і легеневої судинної патології, відповідно, але вони використовувалися в основному як інструменти дослідження і поки що не є такими. широко доступні.
ДІАГНОСТИКА
Наявність симптомів, сумісних із ХОЗЛ (наприклад, задишка в стані спокою або при фізичному навантаженні, кашель із виділенням мокротиння або без нього, прогресуюче обмеження активності), свідчить про діагноз, особливо якщо в анамнезі є контакт із тригерами ХОЗЛ (наприклад, тютюновий дим, професійний пил, дим біомаси в приміщенні), сімейний анамнез хронічного захворювання легенів або наявність супутніх захворювань.
Діагноз ХОЗЛ підтверджується наступним:
● Спірометрія, що демонструє обмеження повітряного потоку (тобто об’єм форсованого видиху за одну секунду/співвідношення форсованої життєвої ємності [FEV 1 /FVC] менше ніж 0,7 або нижче нижньої межі норми [LLN]), яке не є повністю оборотним після введення інгаляційного бронходилататора.
● Відсутність альтернативного пояснення симптомів та обмеження повітряного потоку.
ДИФЕРЕНЦІЙНА ДІАГНОСТИКА
Серед пацієнтів із задишкою, кашлем і виділенням мокротиння в середній або більш пізньому віці диференціальна діагностика широка (наприклад, серцева недостатність, ХОЗЛ, інтерстиціальне захворювання легенів, тромбоемболічна хвороба). Як правило, постійне обмеження повітряного потоку під час обстеження легеневої функції та відсутність рентгенологічних ознак серцевої недостатності чи інтерстиціального захворювання легенів скеровує клініциста до більш вузької диференціації, яка включає ХОЗЛ, хронічну обструктивну астму, бронхоектазичну хворобу, туберкульоз, констриктивний бронхіоліт та дифузний панбронхіоліт. Важливо, що ці умови не є взаємовиключними і зазвичай виникають разом. Наприклад, у пацієнтів з астмою може розвинутися ХОЗЛ, а у пацієнтів з ХОЗЛ може бути супутня бронхоектатична хвороба.
● Хронічна обструктивна астма – у літніх пацієнтів з астмою в анамнезі протягом життя може розвинутися хронічне ремоделювання дихальних шляхів, включаючи фіксовану обструкцію дихальних шляхів. Для пацієнтів без факторів ризику ХОЗЛ у цих випадках передбачуваним діагнозом є хронічна обструктивна астма. Однак у пацієнтів із факторами ризику ХОЗЛ чітке розмежування між хронічною обструктивною астмою та ХОЗЛ неможливо. Як приклад, пацієнт, який страждав на атопічну астму з дитинства та курив цигарки протягом 15 років у віці двадцяти та тридцяти років, у віці п’ятдесяти років може мати поєднання астми та ХОЗЛ. Визнання співіснування цих захворювань має важливе значення для розробки плану лікування, який відображає обидва основні процеси захворювання.
● Хронічний бронхіт із нормальною спірометрією – невелика частина курців сигарет має хронічний продуктивний кашель протягом трьох місяців у кожному з двох послідовних років, але не має обмеження повітряного потоку за тестами легеневої функції. Вони не вважаються хворими на ХОЗЛ, хоча у них може розвинутися ХОЗЛ, якщо вони продовжуватимуть палити.
● Обструкція центральних дихальних шляхів – обструкція центральних дихальних шляхів може бути спричинена численними доброякісними та злоякісними процесами та може імітувати ХОЗЛ із повільно прогресуючою задишкою при фізичному навантаженні з наступною задишкою з мінімальною активністю. Можуть спостерігатися монофонічні хрипи або стридор. Симптоми мінімально зменшуються при вдиханні бронходилататорів, якщо взагалі. Необхідний високий індекс підозри, оскільки звичайні рентгенограми грудної клітки рідко є діагностичними. Незважаючи на те, що петлі потоку-об’єму нечутливі, вони можуть показати характерні зміни центральної обструкції дихальних шляхів, часто до того, як будуть помічені аномалії спірометричних об’ємів
● Бронхоектатична хвороба. Бронхоектатична хвороба, стан аномального розширення бронхів, пов’язаний із хронічною або рецидивуючою інфекцією, має багато спільних клінічних ознак із ХОЗЛ, включаючи запалення дихальних шляхів, які легко спадаються, обструкцію повітряного потоку та загострення, що характеризуються посиленням задишки та виділенням мокротиння. На підставі яскраво виражених симптомів кашлю та щоденного виділення слизисто-гнійного мокротиння підозрюють бронхоектаз. Діагноз зазвичай встановлюється клінічно на підставі характерного кашлю та виділення мокротиння та наявності потовщення бронхіальної стінки та розширення просвіту на КТ грудної клітки.
● Серцева недостатність – серцева недостатність є поширеною причиною задишки серед пацієнтів середнього та старшого віку, а деякі пацієнти відчувають стиснення в грудях і хрипи внаслідок перевантаження рідиною через серцеву недостатність. Іноді відзначається обмеження повітряного потоку, хоча частіше спостерігається обмежувальна схема. Серцева недостатність зазвичай диференціюється за наявністю дрібних базилярних хрипів, рентгенографічними ознаками збільшення розмірів серця та набряку легенів. Рівень мозкового натрійуретичного пептиду (BNP) зазвичай підвищується при серцевій недостатності, але також може підвищуватися під час напруги правого відділу серця від легеневого серця.
● Туберкульоз. В регіоні, ендемічному щодо туберкульозу, загальна поширеність обструкції повітряного потоку становила 31 відсоток серед тих, хто раніше хворів на туберкульоз, у порівнянні з 14 відсотками серед тих, хто не хворів. Цей зв’язок не змінився після коригування респіраторних захворювань у дитинстві, паління та впливу пилу та диму. Таким чином, туберкульоз є одночасно фактором ризику ХОЗЛ і потенційним супутнім захворюванням.
● Констриктивний бронхіоліт. Констриктивний бронхіоліт, також відомий як облітеруючий бронхіоліт, характеризується підслизовим і перибронхіолярним фіброзом, що спричиняє концентричне звуження просвіту бронхіол. Констриктивний бронхіоліт найчастіше спостерігається після інгаляційної травми, трансплантації (наприклад, кісткового мозку, легенів) або в контексті ревматоїдного захворювання легенів чи запального захворювання кишечника. Симптоми включають прогресуючий початок кашлю та задишки, пов’язані з гіпоксемією у спокої або при фізичному навантаженні. Можлива поява трісків. Тестування легеневої функції показує прогресуюче та необоротне обмеження повітряного потоку. Результати інспіраторної комп’ютерної томографії включають центролобулярне потовщення бронхіальної стінки, бронхіолярну дилатацію, малюнок дерева в бруньці та мозаїчний малюнок затухання у формі матового скла.
● Дифузний панбронхіоліт – дифузний панбронхіоліт переважно спостерігається у некурящих чоловіків східноазіатського походження. Практично всі мають хронічний гайморит. При дослідженні легеневої функції часто зустрічається обструктивний дефект, хоча також може спостерігатися змішана обструктивно-рестриктивна картина. Рентгенограми грудної клітки та сканування HRCT показують дифузні центролобулярні вузлуваті та лінійні помутніння, що відповідають потовщеним і розширеним стінкам бронхіол із внутрішньопросвітними слизовими пробками.
● Лімфангіолейоміоматоз – лімфангіолейоміоматоз (LAM) спостерігається переважно у молодих жінок дітородного віку. Тестування легеневої функції часто виявляє легку обструкцію повітряного потоку, хоча може спостерігатися змішана обструктивно-рестриктивна картина. КТ зазвичай демонструє невеликі тонкостінні кісти, які іноді можна сплутати з емфіземою. Однак повітряні простори при емфіземі насправді не є кістами, а спричинені руйнуванням стінок альвеол і постійним розширенням дистальних повітряних просторів, тому «стінки» зазвичай невидимі.
ОЦІНКА ВАЖКОСТІ ТА СТАДІЇ
Було розроблено кілька різних стратегій для класифікації пацієнтів з метою лікування захворювання та прогнозу. У той час як історичні підходи, як правило, більш сильно зважували спірометричні значення, все більше визнається, що інші аспекти захворювання, такі як тяжкість симптомів, ризик загострень та наявність супутніх захворювань, важливі для досвіду пацієнта та прогнозу захворювання.
Системи класифікації GOLD — Хоча стратегія Глобальної ініціативи щодо хронічної обструктивної хвороби легень (GOLD) рекомендує діагностику ХОЗЛ за допомогою симптомів, що супроводжуються співвідношенням об’єму форсованого видиху за одну секунду (FEV1) / форсованої життєвої ємності легень (FVC) <0,7, тяжкість обструкції визначається прогнозованим ОФВ 1 відсоток. Система GOLD використовує чотири ступені:
● GOLD 1 (легке захворювання): прогнозований ОФВ 1 ≥80 відсотків
● GOLD 2 (захворювання середньої тяжкості): прогнозований показник ОФВ 1 від 50 до 80 відсотків
● GOLD 3 (важке захворювання): прогнозований показник ОФВ 1 становить від 30 до 50 відсотків
● GOLD 4 (дуже важке захворювання): ОФВ 1 <30 прогнозованих відсотків
Ця спірометрична система класифікації тяжкості є важливою через її простоту та подальше використання в багатьох клінічних випробуваннях та обсерваційних дослідженнях; однак його прогностична здатність щодо смертності скромна.
Інші групи запропонували потенційні альтернативи системі GOLD Grade на основі спірометрії. Наприклад, схема класифікації тяжкості обструкції повітряного потоку за співвідношенням (STAR) була отримана з використанням приблизно 25-го, 50 -го та 75 -го процентиля співвідношень ОФВ 1 /ФЖЕЛ з когортного дослідження COPDGene та підтверджена за допомогою COPDGene та другого незалежна когорта. Як і GOLD, ця класифікація поділяє пацієнтів із ХОЗЛ на 4 стадії: стадія STAR 1 визначається співвідношенням ОФВ 1 /ФЖЕЛ від 0,6 до 0,7; стадія STAR 2 за співвідношенням ОФВ 1 /ФЖЕЛ між 0,5 і 0,6; стадія STAR 3 за співвідношенням ОФВ 1 /ФЖЕЛ між 0,4 і 0,5; і стадії STAR 4 за співвідношенням ОФВ 1 /ФЖЕЛ <0,4.
Системи GOLD і STAR забезпечили аналогічну дискримінацію смертності та успішно розділили пацієнтів у досліджуваних когортах спостереження за задишкою, респіраторною якістю життя та візуалізаційною оцінкою захворювання. Потенційною перевагою системи STAR є те, що вона не залежить від прогнозованого розміру легенів на основі віку, зросту чи расової/етнічної приналежності. Однак це залежить від отримання якісної спірометрії (наприклад, плато видиху в останню секунду видиху або час видиху ≥15 секунд). STAR вимагає подальшої перевірки в популяційних когортах, перш ніж його можна буде широко впровадити.
У той час як ступінь GOLD стосується спірометричної тяжкості захворювання, GOLD рекомендує іншу систему, інструмент оцінки ABE, для використання для визначення початкової терапії. Інструмент оцінки GOLD ABE використовує індивідуальні симптоми (тобто модифіковану шкалу задишки за медичною дослідницькою радою [mMRC] або тест оцінки ХОЗЛта історію загострень для спрямування фармакотерапії. Багатовимірна оцінка GOLD "ABE" обговорюється більш детально окремо в контексті початкового лікування ХОЗЛ. Ми погоджуємося зі стратегією GOLD щодо щорічного моніторингу постбронходилататорної спірометрії для відстеження зниження ОФВ 1, що може ідентифікувати пацієнтів, хвороба яких прогресує швидше, ніж зазвичай. Подальша спірометрична оцінка також може бути корисною для прийняття терапевтичного рішення при розгляді кількох потенційних причин погіршення задишки. Нарешті, спірометричні показники залишаються важливим компонентом прийняття рішень щодо зменшення об’єму легень і трансплантації легень.
Індекс BODE — індекс BODE є ще однією системою оцінки тяжкості та прогнозу ХОЗЛ. Він розраховується на основі ваги (індексу маси тіла [ІМТ]), обмеження повітряного потоку (FEV 1), задишки (оцінка задишки mMRC) і фізичної здатності (шість хвилин ходьби), і це використовувався для оцінки індивідуального ризику смерті. Цей індекс забезпечує кращу прогностичну інформацію, ніж ОФВ 1 окремо, і може бути використаний для оцінки терапевтичної відповіді на ліки, легеневу реабілітаційну терапію та інші втручання.
Система COPD Foundation — Фонд COPD запровадив систему, яка включає сім доменів тяжкості, кожен з яких має терапевтичне значення Ці домени ґрунтуються на оцінці спірометрії, регулярних симптомів, кількості загострень за останній рік, оксигенації, емфіземи за результатами комп’ютерної томографії або об’єму легень, наявності хронічного бронхіту та супутніх захворювань. У сфері спірометрії Фонд ХОЗЛ використовує п’ять ступенів:
● SG 0: нормальна спірометрія
● SG 1: легкий, постбронходилататорний ОФВ 1 /форсована життєва місткість (ФЖЄЛ) <0,7, ОФВ 1 ≥60 відсотків прогнозованого
● SG 2: помірний, постбронходилататорне співвідношення ОФВ 1 /ФЖЕЛ <0,7, ОФВ 1 від 30 до 60 відсотків прогнозованого
● SG 3: Важкий, постбронходилататорний показник ОФВ 1 /ФЖЕЛ <0,7, ОФВ 1 <30 прогнозованих відсотків
● SG U: не визначено, співвідношення ОФВ 1 /ФЖЕЛ після бронходилататора >0,7, ОФВ 1 <80 відсотків прогнозованого
Перевагою цієї системи постановки є те, що вона спрощує інтерпретацію спірометрії; будь-який спірометричний результат призводить до класифікації, чого немає в системі GOLD.
У той час як ОФВ 1 використовується для оцінки тяжкості, співвідношення ОФВ 1 /ФЖЕЛ для цієї мети не використовується, оскільки вимірювання ФЖЕЛ стає менш надійним у міру прогресування хвороби (довгий видих є важким для пацієнтів), що робить співвідношення менш точним, якщо не забезпечується якісна спірометрія.
РЕЗЮМЕ ТА РЕКОМЕНДАЦІЇ
● Визначення – Глобальна ініціатива з хронічної обструктивної хвороби легенів (GOLD) визначає ХОЗЛ наступним чином: «ХОЗЛ — це гетерогенний стан легенів, що характеризується хронічними респіраторними симптомами через аномалії дихальних шляхів та/або альвеол, які спричиняють стійку, часто прогресуючу, обструкцію повітряного потоку.
Існує суттєве збіг між ХОЗЛ та іншими розладами, які можуть спричинити обмеження повітряного потоку (наприклад, емфізема, хронічний бронхіт, астма, бронхоектатична хвороба, бронхіоліт).
● Клінічні ознаки. Загальні прояви ХОЗЛ включають пацієнтів із невеликою кількістю скарг, але надзвичайно малорухливим способом життя; пацієнти з хронічними щоденними респіраторними симптомами (наприклад, задишка при фізичному навантаженні, кашель); та пацієнти з рецидивуючими гострими загостреннями (наприклад, хрипи, кашель, задишка, втома). Пацієнтів слід запитати про поточне куріння та кількість викурених пачок-років (пачки сигарет на день, помножені на кількість років); інші інгаляційні впливи; туберкульоз, ВІЛ, дитячі легеневі інфекції; астма в анамнезі; і сімейна історія захворювань легенів. Фізичне обстеження грудної клітки залежить від тяжкості ХОЗЛ, але часто є нормальним при легкій формі захворювання.
Діагностична оцінка. Необхідно розглянути діагноз ХОЗЛ і провести спірометрію до та після введення бронходилататорів у всіх пацієнтів, які повідомляють про будь-яку комбінацію задишки, хронічного кашлю або хронічного виділення мокротиння, особливо якщо в анамнезі є контакт із тригерами ХОЗЛ (наприклад,, тютюновий дим, професійний пил, дим біомаси в приміщенні), сімейна історія хронічного захворювання легенів або наявність супутніх захворювань. Для осіб із факторами ризику використання опитувальника CAPTURE (Оцінка хронічного обструктивного захворювання легень у первинній медичній допомозі для виявлення недіагностованих респіраторних захворювань і ризику загострення) та вимірювання пікфлоуму для оцінки незареєстрованих симптомів та потенційного обмеження повітряного потоку може визначити додаткових симптоматичних пацієнтів, які підходять для подальшого обстеження.
•Спірометрія до та після бронходилататорів – ХОЗЛ підтверджується, коли у пацієнта зі сумісними симптомами виявляється необоротне обмеження повітряного потоку (тобто співвідношення об’єму форсованого видиху після бронходилататора [FEV1] / форсованої життєвої місткості [FVC] менше ніж 0,7 [або нижче нижньої межі норми (НМН)]) і немає альтернативного пояснення симптомів і обструкції повітряного потоку.
•Додаткове обстеження – при оцінці пацієнтів із ХОЗЛ зазвичай проводять лабораторні дослідження та рентгенографію грудної клітки, щоб виключити альтернативні діагнози, оцінити наявність супутніх захворювань або оцінити зміну симптомів, яка свідчить про ускладнення ХОЗЛ. КТ грудної клітки виконується для оцінки аномалій, виявлених на звичайній рентгенограмі грудної клітки, щоб виключити певні ускладнення ХОЗЛ (наприклад, тромбоемболічні захворювання, рак легенів), або коли пацієнту розглядають операцію зі зменшення об’єму легенів, ендобронхіальних клапанів або трансплантацію легень.
● Диференційна діагностика. Серед пацієнтів, у яких у середньому чи старшому віці спостерігаються задишка, кашель і виділення мокротиння, диференціальна діагностика широка (наприклад, серцева недостатність, ХОЗЛ, інтерстиціальне захворювання легень, тромбоемболічна хвороба)
● Постдіагностичне обстеження – після встановлення діагнозу ХОЗЛ додаткове тестування може бути доречним для оцінки тяжкості захворювання та визначення оптимального початкового терапевтичного лікування.
- Етіологічна оцінка, включаючи тестування на альфа-1 антитрипсин. Якщо не проведено до встановлення діагнозу, нова діагностика ХОЗЛ повинна спонукати до пошуку основних етіологічних факторів. Усіх пацієнтів із ХОЗЛ доцільно перевірити на дефіцит альфа-1 антитрипсину (ААТ) шляхом визначення рівня ААТ у сироватці крові та визначення генотипу ААТ.
- Здатність до фізичних навантажень – для пацієнтів із ХОЗЛ ми проводимо формальний шестихвилинний тест ходьби з амбулаторним вимірюванням оксиметрії. Це дозволяє оцінити фізичну здатність, а також визначити газообмін під час тренування.
- Інші дослідження – Оцінка легеневих об’ємів і газообміну доречна для пацієнтів з ознаками більш тяжкого захворювання.
● Оцінка тяжкості та стадії
- Оригінальна система визначення GOLD базувалася виключно на постбронходилататорному ОФВ 1. Хоча він добре визнаний і широко використовується, його критикували за недооцінку важливості тяжкості симптомів, ризику загострень і наявності супутніх захворювань у прогнозуванні результату.
- Переглянута стратегія GOLD «ABE» використовує комбінацію індивідуальних симптомів та історії загострень і госпіталізацій через загострення для стратифікації симптомів і ризику загострення та визначення терапії.
- Інші багатовимірні системи визначення стадії включають індекс BODE і систему Foundation COPD.
ДЖЕРЕЛО: https://www.uptodate.com/








