Від таблеток до імпульсів: електрифікація медицини за допомогою периферичної нервової системи
Дата публікації: 19.02.2024
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: спинний мозок, нерви, стимуляція, периферична нервова система, центральна нервова система, імпульси, рефлекси
Центральна (ЦНС) та периферична (ПНС) нервова система працюють разом, щоб координувати та регулювати функції нашого тіла на додаток до розміщення нашого людського інтелекту. ЦНС є центром управління і включає мозок і спинний мозок. У той час як мозок обробляє інформацію, приймає рішення та надсилає інструкції, спинний мозок та пов'язана з ним ПНС є комунікаційною магістраллю, яка несе нервові сигнали до та з мозку.
ПНС складається з величезної мережі нервів, які розгалужуються від головного та спинного мозку до наших органів, кінцівок та тканин. Ретрансляція сигналів ПНС та мозок забезпечують зв'язок між ЦНС та рештою тіла. ПНС може не мати такої ж репутації рок-зірки, як мозок, але це кістяк нашого повсякденного життя. Вона відіграє ключову роль у наших сенсорних переживаннях, рефлексах і навіть вегетативних функціях, таких як травлення та серцебиття.
Neurology Thursday повернулись! Перегляньте записи заходів, що завершились та не забудьте зареєструватись на ті, що ще будуть!
Через всі ці критичні функції захворювання, що впливають на ПНС, можуть значно впливати на повсякденне життя, викликаючи обмеження рухливості, відчуття та координації. Вони порушують спілкування в конкретних типах нервів, таких як рухові нерви, відповідальні за контроль м'язів, сенсорні нерви, відповідальні за передачу відчуттів дотику, температури та больових відчуттів, або вегетативні нерви, які регулюють баланс нашої серцевої, легеневої та запальної реакції.
Нові лікарські рішення, як правило, розробляються для лікування дуже специфічного стану, і розробка нового препарату зазвичай займає роки, щоб пройти всі етапи, перш ніж він буде схвалений і виведений на ринок. Введення біоелектронної медицини, новий підхід, який використовує мову електричних імпульсів, щоб говорити безпосередньо зі складною мережею нервів у ПНС.
Біоелектронна медицина: електрика як терапія
Біоелектронна медицина стимулює електрично активні тканини, такі як нерви або м'язи, для придушення небажаних станів в організмі або для полегшення бажаних станів. Найвідомішим прикладом, який вже є на ринку, є серцевий кардіостимулятор, який стимулює серцевий м'яз. Периферична нервова система представляє особливий інтерес у сучасних дослідженнях біоелектронної медицини, оскільки це двонаправлене шосе, яке передає сигнали від мозку до органів і навпаки. Стимулюючи ПНС, можна усунути як органи, так і мозок.
Однією з переваг є те, що терапію можна контролювати за допомогою розумної електроніки: прилади, які є адаптивними та можуть бути налаштовані лікарем або навіть пацієнтом після імплантації. Його можна миттєво вмикати та вимикати за допомогою пульта дистанційного керування, що неможливо з перорально введеними препаратами. Крім того, лікування може бути автоматично скориговано на основі факторів навколишнього середовища або внутрішніх маркерів, які відображають стан здоров'я людини. Сьогодні ряд хронічних захворювань, таких як ревматоїдний артрит, хронічний біль та епілепсія, є мішенню для цієї терапії.
Imec використовує нанотехнології для розробки невеликих, малопотужних стимулюючих імплантатів для різних застосувань ПНС, подібних до своїх мініатюрних мозкових імплантатів для зондування. Насправді й мозкові, і ПНС імплантати мають схожі майбутні цілі.
По-перше, пристрої для обох цілей вивчають рішення для все більш детального зондування та/або стимуляції. По-друге, нові методи інкапсуляції, засновані на великих дослідженнях матеріалів, дозволять імплантатам оптимально функціонувати в організмі протягом місяців і років. По-третє, вони обидва прагнуть поєднати електричну стимуляцію та зчитування в режимі реального часу, щоб врешті-решт закрити цикл: стимуляцію у відповідь на відчуту інформацію. Нарешті, дослідники розглядають можливість поєднання технології імплантатів з різними методами, такими як ультразвук, для цілей стимуляції, а також для передачі енергії на імплантат.
Блукаючий нерв як кінцева ціль
Від спинного мозку нерви простягаються назовні до місця призначення. Чим нижче в тілі, тим специфічніші нерви. Стимуляція в кінцевій точці цих нервів вибірково впливає на органи-мішені, що технологічно полегшує направлення електричних імпульсів. Зворотний бік медалі, однак, полягає в тому, що пристрій повинен бути меншим і сидіти глибше в тілі, що створює проблему для хірургії, упаковування, зв'язку та доставлення енергії.
Чим ближче нерви до мозку, тим вони складніші. Наприклад, блукаючий нерв є найдовшим черепним нервом в організмі й безпосередньо пов'язаний з кількома органами та системами, такими як серце, легені та травна система. За допомогою імплантату ПНС стимуляція блукаючого нерва потенційно може вплинути на широкий спектр тілесних функцій з однієї (і більш поверхневої) точки втручання.
Стимуляція блукаючого нерва в шиї вже отримала визнання для певних форм стійкої до лікування епілепсії та депресії, тоді як хронічна мігрень з'являється як відносно нове застосування. Але ми ще не там. Блукаючий нерв - це 4-мм широка головоломка з нервів, що містять підпучки (фасцикули) з багатьма різними типами волокон, які розгалужуються, зливаються і скручуються вздовж нерва. Це робить стимуляцію правильних волокон у нерві.
Деякі пацієнти з епілепсією, які пройшли цей тип лікування, наприклад, скаржаться на зміни голосу, прискорене серцебиття або зміни в диханні, тому що імпульс, який заглушує судоми, також впливає на волокна, які проходять до гортані, серця та легенів.
Цільове стимулювання означає зосередження енергії стимуляції на меншій фізичній одиниці, від міліметрів до десятків міліметрів. Дослідники з imec та Інституту медичних досліджень Файнштейна співпрацюють, щоб радикально покращити селективність нервової стимуляції за допомогою нової техніки під назвою i2CS, заснованої на інтерференції електричних полів різних хвиль. Основні технологічні проблеми включають синхронну доставлення інтерференційних струмів через пари електродів та мінімізацію спотворення сигналу та витоку при введенні високих струмів на високих частотах.
Розширене пакування для імплантатів
Ще одна проблема полягає в тому, щоб розробити пакет, який дозволить пристрою залишатися в організмі протягом місяців або років. Правильна інкапсуляція та проводка мають першорядне значення для функціональності, довговічності та стабільності. Захисний бар'єр працює в обох напрямках. З одного боку, пристрій повинен бути захищений від суворого середовища тіла, оскільки рідини можуть поставити під загрозу його функціональність. З іншого боку, пристрій не повинен викликати будь-яку небажану реакцію навколишньої тканини тіла шляхом витоку небіосумісних матеріалів.
Більшість електронних імплантатів, схвалених FDA, мають досить громіздкий і жорсткий титановий корпус як герметична інкапсуляція. Хоча концепція перевірена, такий підхід потребує широкого огляду майбутніх імплантатів, які спрямовані на мініатюризацію - як з погляду матеріалів, так і методів пакування. CMST, дослідницька група imec в Гентському університеті, розробляє спеціальне пакування для довгострокових імплантатів.
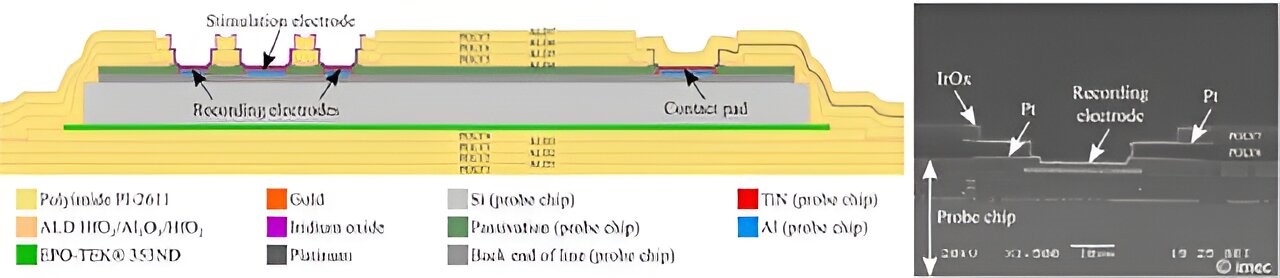
У публікації 2019 року вони представили платформу обробки для інкапсуляції імплантату ПНС на основі тонкоплівкових технологій виробництва. Дослідники працювали з м'якими матеріалами замість традиційних твердих матеріалів, таких як титан (сплави), щоб забезпечити мініатюризацію та ультравідповідність кінцевому пристрою. Крім того, м'яка інкапсуляція підвищує комфорт, має обмежену реакцію чужорідного тіла і пропонує конформальність, необхідну для покриття топографії чіпа.
Полімери, такі як поліімід, широко використовуються для інкапсуляції імплантованих електронних пристроїв. Однак полімерне пакування страждає від дифузії вологи, набряку, поганої адгезії та/або деградації матеріалу, що в кінцевому підсумку призводить до виходу з ладу пристрою. На відміну від цього, оксиди металів, такі як Al2O3, HfO2 та TiO2, що відкладаються шляхом осадження атомного шару (ALD), є ультратонкими (товщина порядку кількох нанометрів), надзвичайно щільними та конформними покриттями, як повідомляється, з відмінними властивостями вологоізобар’єру.
Щоб скористатися перевагами полііміду та шарів ALD, дослідники поєднали матеріали обох типів, щоб отримати механічно гнучкі інкапсуляції з відмінними бар'єрними властивостями. Вони розробили багатошарові стеки поліімідних плівок товщиною 5,5 мкм і шарів HfO2/Al2O3/HfO2 товщиною в діапазоні від 10 нм до 20 нм з особливою увагою до адгезії між шарами, щоб уникнути накопичення вологи на інтерфейсі.
Ця золота комбінація пройшла всі загальні бар'єрні тести. Як додаткова перевага, всі необхідні технологічні етапи сумісні з тонкоплівковими технологіями виробництва, що робить процес масштабованим до великого обсягу, недорогого виробництва.
Закриття циклу
Більшість імплантатів все ще передаються: ви вмикаєте/вимикаєте пристрій, стимуляція починається/зупиняється. Лікар може перемкнути інтенсивність стимуляції, і все. Одним із прикладів є пристрій, розроблений для стимуляції тазового нерва, який проходить через область навколо сечового міхура та статевих органів. Стимуляція заспокоює гіперактивний сечовий міхур у пацієнтів з синдромом подразненого сечового міхура, але вона також допомагає при таких станах, як нетримання сечі та певні сексуальні розлади. Отриманий прототип зараз знаходиться на доклінічній фазі розробки медичного пристрою.
Майбутнє, полягає в системі замкнутого кола, в якій стимуляція відбувається на основі виміряних параметрів. Це ідея нового проєкт для, де imec та консорціум, до якого він є частиною, нещодавно почали працювати над імплантатом для заглушки ампутованої руки, які зчитують і стимулюють нерв руки, щоб рухати штучною рукою. Для такого дизайну imec спиратиметься на свій досвід у зборі, обробці та стимуляції сигналів, а також на свій досвід у мініатюрних, малопотужних конструкціях з крайовими обчисленнями.
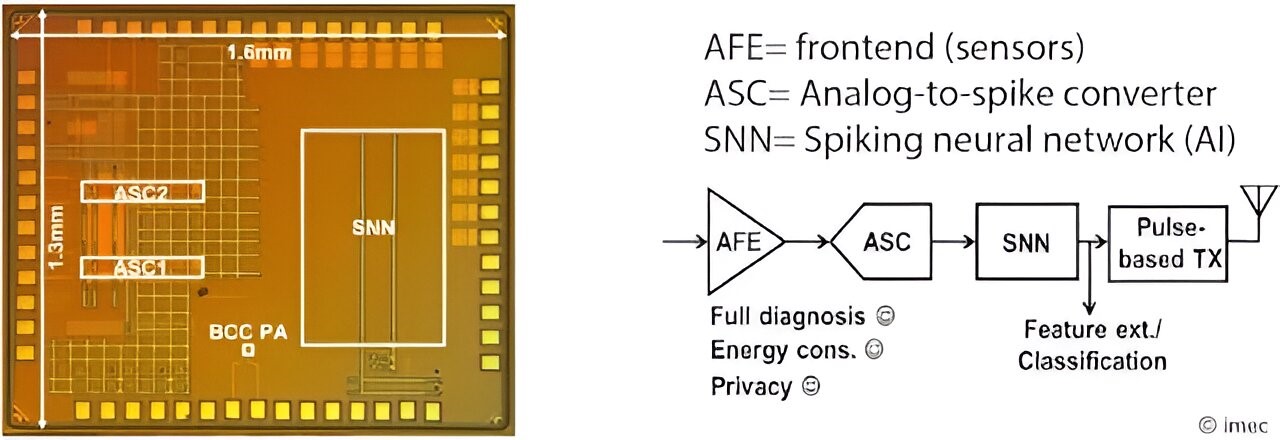
Для того, щоб націлитися на правильний нерв, пристрої повинні бути розміщені дуже близько до поверхні, наприклад, як манжета або всередині нерва. Ці просторові обмеження, своєю чергою, обмежують об'єм та енергію пристрою. Нервовий імплантат в ідеалі має об'єм міліметрового масштабу, і — оскільки немає місця для акумулятора — електронна система повинна споживати низьку потужність (набагато нижче 100 µВт), щоб забезпечити бездротову передачу енергії. З іншого боку, нервові сигнали (так звані спайки або потенціали дії), як правило, є рідкісними, але дуже швидкими подіями (мілісекундами), тому важлива висока часова роздільна здатність системи запису. Якби ці сигнали були відібрані зі звичайною високою швидкістю дискретизації, була б висока надмірність сигналу і, отже, погана ефективність системи.
Загальне споживання енергії обробки інформації та транспортування може бути значно зменшено, якщо оброблятимуться лише зміни (тобто дельта) сигналів. Команда imec в Нідерландах нещодавно переклала цю ідею на чіп, який - замість безперервної обробки сигналів - активний лише тоді, коли відбувається подія, тобто вгору і вниз фази потенціалів дій, тим самим створюючи тимчасові підписи.
Уявіть, що передані скроневі сигнатури потім можуть бути декодовані й повернуті в стимулятор імплантату для виконання нейромодуляції в режимі реального часу. Це значно зменшить затримку контролю та швидкість передачі даних, тим самим зменшуючи вимоги до бездротового зв'язку, а також енергоспоживання.
Як живити імплантат
Зі зростаючою складністю імплантатів енергоефективне живлення важливіше, ніж будь-коли. Вибір джерела живлення залежить від сценарію користувача і часто є балансом між тим, як часто користувачеві потрібен імплантат, скільки енергії він споживає і наскільки небезпечним для життя стан, який він полегшує.
Наприклад, штучну руку, згадану вище, можна зняти під час сну та зарядити на тумбочці. У цьому випадку недостатньо акумулятора або дуже маленької імплантаційної батареї. На іншому кінці спектра знаходяться імплантати, які безперервно стимулюють, такі як стимулятор Neurogyn для гіперактивного сечового міхура. Для них потрібні більші батареї, які або перезаряджаються, або замінюються за допомогою хірургічного втручання.
Останнім часом ультразвук викликав великий інтерес у сфері ПНС для живлення імплантатів. Ультразвук цікавий для біомедичних застосувань, оскільки хвилі поширюються через тканини з невеликим розсіюванням. Крім того, ці хвилі можуть бути високо сфокусовані за допомогою методів формування променя.
Маніпулюючи фазою та амплітудою кожного перетворювача в масиві, отриманий ультразвуковий промінь може керуватися електронним чином, не рухаючи перетворювач фізично. Це дозволяє спрямовувати промінь до певної цілі в тілі. Ці переваги роблять ультразвук переконливою альтернативою індуктивному живленню, що вимагає близької близькості та стабільного вирівнювання джерела та імплантату.
Дотик ультразвуку для стимуляції
Не тільки для живлення, ультразвук також розглядається з терапевтичних причин. Попри те, що електрика все ще є основним способом взаємодії ПНС зараз, ультразвук отримує все більшу увагу для стимуляції нервів. Він менш інвазивний, і здатність спрямовувати енергію ультразвуку на одну фокусну точку може дозволити більш точну стимуляцію, ніж електричну стимуляцію.
Ідея заснована на концепції гаптики в повітрі, в якій ультразвукові хвилі тиску на частотах нижче 500 Гц викликають відчуття дотику в повітрі. Imec досліджує, як цей принцип можна використовувати для стимуляції нервів, таких як блукаючий нерв.
ДЖЕРЕЛО: https://medicalxpress.com/
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу

Новий метод скринінгу для вимірювання прон ...

Пояснення дієти MIND: продукти, що борютьс ...

Високі дози фолієвої кислоти можуть запобі ...

Діабет у спеку: недооцінені ризики, які мо ...

Запис симпозіуму «Pharmacotherapia: терапі ...

ДЕЦ рекомендує включити велманазу альфа до ...


