Науковці вперше вилікували агресивний рак підшлункової залози у мишей. Чи повторять результат на людях?
Дата публікації: 17.03.2026
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: рак підшлункової залози, таргетна терапія, мутації генів, дослідження на мишах, прицільні протипухлинні препарати, онкогени, протиракові препарати, резистентність пухлин, комбінована протипухлинна терапія, експериментальні моделі раку
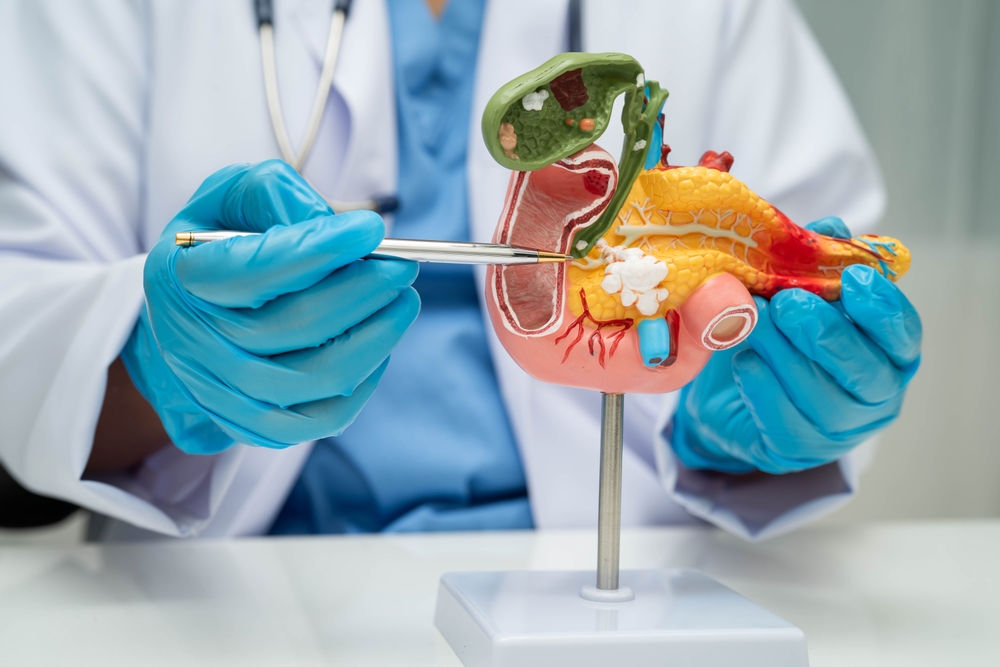
Навіть для сучасної науки рак підшлункової залози залишається одним із найагресивніших і найстійкіших до лікування. Нещодавно команда іспанських науковців подарувала нову надію у боротьбі з цією недугою: дослідники повністю подолали рак підшлункової залози в мишей — без агресивної хімієтерапії чи опромінення, лише завдяки комбінації трьох препаратів, націлених на пухлину. Водночас між успішним експериментом на мишах і появою нового стандарту лікування для людей лежить довгий і складний шлях.
Що прийшло на заміну хіміотерапії?
Сучасне лікування злоякісних пухлин суттєво відрізняється від методів XX століття, які базувалися на хімієтерапії — препаратах, що шкодять не лише раковим, а й здоровим клітинам. Завдяки генетичним дослідженням стало зрозуміло, що в основі більшості пухлин лежать зміни в конкретних генах, які запускають некероване розмноження клітин. Якщо самі гени поки що знешкоджувати не вміють, то прицільно зупиняти роботу шкідливих білків, створених за інструкцією онкогенів, уже іноді вдається.
Так з’явилися прицільні, або таргетні, препарати. Вони зв’язуються з конкретним хвороботворним білком і вже застосовуються при лейкемії, раку грудей, раку прямої кишки, легень та інших пухлинах. Попри високу вартість, вони нерідко значно ефективніші за попередні підходи. Наприклад, іматиніб дозволив істотно збільшити тривалість життя хворих на хронічну мієлоїдну лейкемію. Проте навіть таргетні препарати не завжди можуть впоратися з агресивним раком.
У чому слабкість прицільних препаратів?
Для багатьох пухлин прицільні препарати або не працюють зовсім, або до них дуже швидко виникає стійкість. Причина в тому, що клітини, зокрема пухлинні, — це складні білкові системи, де багато процесів, особливо ріст і розмноження, багаторазово дублюються. У межах однієї пухлини клітини теж не однакові: вони мають різні особливості, сильні та слабкі сторони. Тому боротьба з раком часто нагадує боротьбу з армією, яка вміє ухилятися від ударів і пристосовуватися до нової тактики.
Щоб подолати ці «лінії оборони», одного препарату часто недостатньо. Можна поєднувати кілька ліків або підвищувати дозу, але це нерідко супроводжується наростанням токсичності та тяжких побічних ефектів.
Чому рак підшлункової такий складний для лікування?
Попри успіхи таргетної терапії, при багатьох видах раку її ефективність залишається обмеженою. Наприклад, при раку легень із мутацією в гені рецептора епідермального фактора росту (EGFR) застосовують афатиніб, який у комбінації з пеметрекседом подовжував виживання без прогресування пухлини порівняно з традиційною хімієтерапією.
Оскільки білки EGFR надмірно утворюються в багатьох пухлинах, виникла ідея застосувати афатиніб і при раку підшлункової залози — особливо агресивному та стійкому до звичайної хімієтерапії. Шанси на п’ятирічне виживання при цьому захворюванні становлять у середньому лише близько 5%, а за наявності метастазів — ще менше.
Водночас приблизно у 85% хворих на рак підшлункової залози виявляють мутації в гені KRAS. Проте клінічно перевірених препаратів проти найпоширеніших мутацій цього гена — KRAS G12D і KRAS G12V — наразі немає. Розробку ускладнює велика кількість різних мутацій, для кожної з яких потрібен окремий підхід. Дослідники намагаються знайти універсальні препарати, які блокуватимуть більшість патологічних варіантів KRAS. Одним із таких є дараксонрасиб. Але навіть при раку легень він продемонстрував лише обмежену ефективність і супроводжувався високою частотою побічних ефектів.
Як підійшли до проблеми іспанські дослідники?
Іспанська команда з Національного центру онкологічних досліджень у Мадриді, вирішила спробувати комбінацію кількох таргетних препаратів. Дослідники поєднали дараксонрасиб і афатиніб, які впливають на KRAS та EGFR, з експериментальним препаратом SD-36, що запускає руйнування білка STAT3, важливого для розмноження ракових клітин.
У статті в журналі Proceedings of the National Academy of Sciences автори повідомили, що така потрійна комбінація змогла знищити штучно викликаний рак підшлункової залози в мишей, а самі тварини прожили 200–300 днів без повернення пухлин. Лікування також виявилося дієвим щодо людських ракових клітин, пересаджених мишам.
Чому ці результати ще не означають прорив для людей?
Попри обнадійливі результати, комбінація кількох препаратів — не нова стратегія. Вона не завжди підвищує ефективність, зате часто значно збільшує токсичність. Наприклад, поєднання афатинібу з гемцитабіном при раку підшлункової не покращило виживання, але суттєво підвищило частоту побічних ефектів. Крім того, в іспанському дослідженні на мишах використовували значно вищі дози препаратів, ніж ті, що застосовують у людей. Те, що переносить миша, для людини може виявитися небезпечним або навіть летальним.
Такі міжвидові відмінності в обміні речовин — звичайне явище, але саме вони часто заважають перенести успішні результати з тваринних моделей у клінічну практику. Чимало препаратів, які добре працювали в мишей, виявлялися неефективними або занадто токсичними для людей.
Перегляньте записи:
Який тоді сенс у дослідженнях на мишах?
Ідеального модельного організму, результати якого можна було б безпосередньо перенести на людину, поки що не існує. Але миші залишаються надзвичайно важливим інструментом у науці: вони маленькі, швидко розмножуються, їх відносно просто утримувати, а їхня біологія добре вивчена. Кожен успіх у лікуванні пухлин у мишей наближає створення ефективнішого лікування для людей. Усі сучасні таргетні препарати на певному етапі тестувалися саме на мишах, і без цих досліджень не було б мільйонів врятованих життів.
Дослідження потрійної комбінації таргетних препаратів при раку підшлункової залози, навіть якщо саме така схема не буде застосовуватися в людей, демонструє принципову можливість: агресивну пухлину потенційно можна знищити без хімієтерапії, опромінення й важких операцій — шляхом блокування конкретних клітинних білків.
Це дає надію, що з часом рак підшлункової залози теж стане або виліковним, або хоча б добре контрольованим захворюванням. Але між успіхом у мишей і реальними ліками для людей — ще роки клінічних випробувань, пошуку безпечних доз і подолання резистентності.
ДЖЕРЕЛО: Nauka
На платформі Accemedin багато цікавих заходів! Аби не пропустити їх, підписуйтесь на наші сторінки! Facebook. Telegram. Viber. Instagram.
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу
Дослідники прогнозують розвиток ішемічної ...

Вакцина проти COVID-19 у першому триместрі ...

Надмірна вага в ранньому віці пов’язана з ...

Носовий спрей як інноваційний підхід до до ...

Забруднення озоном як фактор ризику розвит ...

НСЗУ розпочала прийом пропозицій від закла ...




