Клінічна настанова: Лікування важкого рефрактерного атопічного дерматиту (екземи) у дітей
Дата публікації: 08.10.2024
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: атопічний дерматит, гормонотерапія, клінічна настанова, екзема, рефрактерний атопічний дерматит

Атопічний дерматит (АД) — це поширене хронічне запальне захворювання шкіри, що характеризується сверблячою екзематозною висипкою на шкірі. У більшості дітей розлад лікується за допомогою ретельного догляду за шкірою, стратегій відновлення бар'єра, місцевої терапії запалення та усунення факторів, що загострюють. Пацієнти з важким захворюванням, які не покращуються за допомогою місцевої терапії, можуть отримати користь від системних препаратів або фототерапії.
У цій темі розглядаються причини та лікування тяжкого рефрактерного АД у дітей.
ВИЗНАЧЕННЯ ВАЖКОГО АТОПІЧНОГО ДЕРМАТИТУ
Більшість пацієнтів з АД мають захворювання легкого та середнього ступеня тяжкості. Однак у частини пацієнтів розвиваються важкі симптоми. Важкий АД можна узагальнено описати як наявність поширених екзематозних уражень, невпинного свербежу або захворювання, яке значно погіршує якість життя пацієнта. Пацієнти з тяжким АД, які не реагують на місцеву терапію першої лінії, можуть бути класифіковані як такі, що мають важке рефрактерне захворювання.
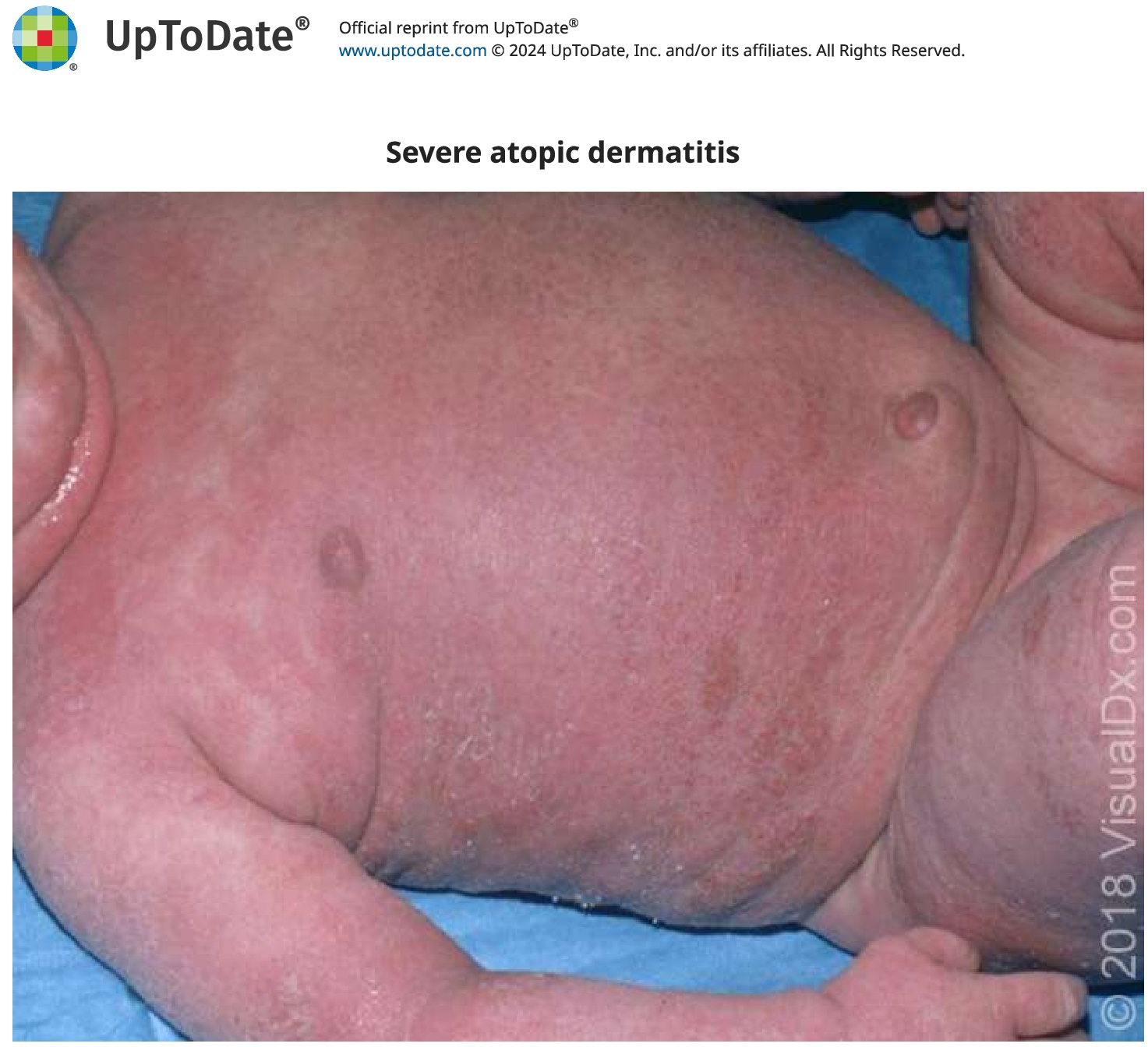
ОЦІНКА СТУПЕНЯ ТЯЖКОСТІ
У клінічних дослідженнях використовувалися шкали для визначення тяжкості АД, такі як Global Assessment дослідника (IGA), індекс оцінки атопічного дерматиту (SCORAD) та індекс площі та тяжкості екземи (EASI). Хоча такі шкали корисні для стандартизації результатів досліджень, вони не використовуються в клінічній практиці та можуть не відображати тяжкість захворювання, яку сприймають окремі пацієнти.
Міжнародне дослідження за участю понад 1000 пацієнтів або батьків дітей з АД з 34 країн виявило, що симптоми, які вважаються важливими на думку 80 відсотків учасників, включають свербіж, біль, відчуття гарячості або запалення шкіри, кровотечі, залучення видимих або чутливих органів ділянок тіла, тріщин, труднощі зі сном, кількість ураженого тіла та плач/виділення.
Було розроблено кілька інструментів оцінки тяжкості, які включають сприйняття пацієнтом тяжкості та контролю захворювання, пов’язаного з лікуванням:
● POEM – оцінка екземи, орієнтована на пацієнта (POEM), шкала, повністю розроблена пацієнтом і оцінювана пацієнтом, була запропонована як основний інструмент для доповнення оцінюваних клініцистами шкал для оцінки тяжкості захворювання та відповіді на лікування у пацієнтів.
● ADCT – Подібний інструмент під назвою Інструмент контролю атопічного дерматиту (ADCT) був валідований для пацієнтів віком від 12 років. Ця шкала з шести запитань розроблена для клінічного використання та має на меті визначити, чи перебуває стан під контролем, що може бути більш актуальним, ніж тяжкість захворювання на думку пацієнта. Версія для молодших пацієнтів також перевіряється.
Практичний посібник із візуальної оцінки тяжкості екземи, який також включає оцінку впливу хвороби на якість життя та психосоціальний добробут, був запропонований Національним інститутом здоров’я та передового догляду Великобританії:
● Легкий – ділянки сухої шкіри, нечастий свербіж (з невеликими ділянками почервоніння або без них); невеликий вплив на повсякденну діяльність, сон і психосоціальне благополуччя.
● Помірний – ділянки сухої шкіри, частий свербіж, почервоніння (з або без екскоріації та локального потовщення шкіри); помірний вплив на повсякденну діяльність і психосоціальне благополуччя, часті порушення сну.
● Важкий – широкі ділянки сухої шкіри, безперервний свербіж, почервоніння (з екскоріацією або без неї, значним потовщенням шкіри, кровотечею, виділенням, тріщинами та зміною пігментації); серйозне обмеження повсякденної діяльності та психосоціального функціонування, нічна втрата сну.
ОЦІНКА ПОТЕНЦІЙНИХ ПРИЧИН РЕФРАКТЕРНОЇ ХВОРОБИ
Обставини, які можуть сприяти виникненню тяжкого або резистентного АД, включають фінансові міркування, погану прихильність або неправильне використання ліків, наявність екологічних факторів, що загострюють, вторинну інфекцію та реакції гіперчутливості на місцеве лікування або інші алергени. Перш ніж розпочинати додаткове лікування АД, клініцисти повинні переконатися, що важке рефрактерне захворювання не є результатом присутності фактора, якого можна уникнути або лікувати.
Причини важкого атопічного дерматиту або того, який важко піддається лікуванню
|
Неправильний діагноз |
|
Неефективність лікування |
|
Неправильно використаний препарат |
|
Схема лікування занадто складна |
|
Неадекватні інструкції |
|
Ліки не використовуються через побоювання батьків або пацієнта побічної дії ліків |
|
Ліки недоступні |
|
Через високу вартість |
|
Не на формулярі |
|
В аптеці немає |
|
Алергічна реакція на ліки або засоби для догляду за шкірою (алергічний контактний дерматит) |
|
Вплив подразників |
|
Вплив алергену (харчового або екологічного) |
|
Важка хвороба |
Погана прихильність/неправильне застосування ліків — для багатьох пацієнтів недостатня прихильність до режиму лікування та основних методів догляду за шкірою сприяє стійкій хворобі. Понад 50 відсотків пацієнтів з АД не призначають лікування відповідно до рекомендацій своїх клініцистів. Конкретні причини неадекватного застосування лікування включають фінансові міркування, занепокоєння щодо побічних ефектів ліків, неприязнь пацієнтів до місцевих препаратів і недостатній час для клініцистів, щоб навчити пацієнтів щодо догляду за шкірою.
Фобія місцевих кортикостероїдів, яка визначається як занепокоєння або страх щодо використання місцевих кортикостероїдів, є поширеною, з поширеністю серед пацієнтів та осіб, які доглядають за ними, у всьому світі від 20 до понад 80 відсотків. Кортикостероїдна фобія, ймовірно, є причиною поганої прихильності до лікування та неефективності лікування серед пацієнтів з АД.
Фактори загострення/провокаційні чинники навколишнього середовища — обставини, які можуть сприяти виникненню тяжкого або резистентного АД, включають недотримання традиційної терапії, вторинну інфекцію, реакції гіперчутливості на місцеве лікування та постійний вплив тригерів спалахів захворювання.
Факторами, що загострюють АД, можуть бути низька вологість середовища; ксероз (сухість шкіри); піт і перегрів шкіри; емоційний або фізіологічний стрес; і вплив дратівливих речовин, таких як агресивні хімікати або мило. Уникнення цих факторів корисно для уникнення гострих спалахів, а також для тривалого лікування, хоча це не завжди можливо.
Інфекція.
Пацієнти з АД мають підвищений ризик вторинних шкірних бактеріальних, вірусних і дерматофітних інфекцій. Слід враховувати можливість вторинної інфекції у пацієнтів з ураженнями шкіри, які не піддаються традиційній терапії. Зокрема, лікарі повинні знати про можливість інфікування Staphylococcus aureus та вірусом простого герпесу (ВПГ).
Колонізація S. aureus частіше зустрічається в осіб з AD, ніж у загальній популяції, і S. aureus є поширеною причиною вторинної інфекції у цих пацієнтів. Наявність нагноєння або кірочок медового кольору свідчить про інфекцію S. aureus. Навіть за відсутності явної інфекції колонізація S. aureus може бути фактором загострення АД.
Вторинна інфекція ВПГ (герпетична екзема) також може виникнути і, рідко, може призвести до загрозливої для життя дисемінації ВПГ у пацієнтів з АД. Індикаторами цієї інфекції є перфоровані ерозії, геморагічні кірки, везикули. Рідко вірус Коксакі та вірус осповакцини (у вакцині проти натуральної віспи) можуть давати подібну клінічну картину.
Реакції гіперчутливості на лікування — уповільнені реакції гіперчутливості на контактні алергени в місцевих пом’якшувачах або ліках є ще однією причиною очевидної відсутності відповіді на лікування. Алергічний контактний дерматит може бути спричинений носієм або активними інгредієнтами в пом’якшувальних речовинах (наприклад, ланолін, пропіленгліколь, ароматизаторах, консервантах), місцевих імуносупресивних препаратах (наприклад, кортикостероїдах, інгібіторах кальциневрину) та місцевих антибіотиках (наприклад, бацитрацин, неоміцин).
Контактну алергію на місцевий пом’якшувальний засіб, ліки або інший алерген (наприклад, нікель) слід розглядати, якщо пацієнти мають АД, який не реагує на цю терапію або, здається, погіршується. Ідентифікація та усунення контактного алергену може призвести до швидкого клінічного покращення у хворих. Якщо є підозра на контактну алергію, слід провести патч-тест, щоб визначити відповідальний алерген.
Харчова алергія та алергія на навколишнє середовище.
У деяких випадках пацієнти з рефрактерною АД можуть мати недіагностовану харчову алергію чи алергію на навколишнє середовище, що може погіршити симптоми їхнього захворювання. Важливо виключити негайну та відстрочену гіперчутливість за допомогою тестування на алергію (наприклад, шкірний прик-тест, визначення специфічного імуноглобуліну Е [IgE], тестування на пластирі).
Однак клініцисти повинні усвідомлювати, що доказ сенсибілізації до алергену не є доказом клінічно значущої алергії. Крім того, навіть клінічно значуща харчова алергія часто не є тригером стійкої екземи, оскільки харчова алергія найчастіше проявляється кропив’янкою та ангіоневротичним набряком, а не дерматитом.
Підтвердження клінічної реактивності є особливо важливим при підозрі на харчову алергію у маленьких дітей, оскільки уникнення харчових алергенів може призвести до менш оптимального споживання їжі. Крім того, є деякі докази того, що уникання їжі може справді викликати сенсибілізацію, включаючи підвищений ризик розвитку анафілаксії.
Неправильний діагноз — неправильний діагноз може бути причиною неефективності традиційної терапії. Слід враховувати можливість інших розладів, які можуть проявлятися клінічними ознаками, схожими на АД. Вони можуть включати такі стани, як Т-клітинна лімфома шкіри, аутоімунні розлади та дефіцит харчування чи імунної системи.
Диференційна діагностика важкого атопічного дерматиту
|
Первинні захворювання шкіри |
|
Порушення шкірного бар'єру: синдром Нетертона, іхтіоз |
|
Запальні захворювання шкіри: псоріаз, контактний дерматит (подразнювальний або алергічний) |
|
Первинні імунодефіцити та ускладнення лікування |
|
Важкий комбінований імунодефіцит |
|
Синдром Віскотта-Олдріча |
|
Гіпер-IgE синдром |
|
Хвороба «трансплантат проти господаря». |
|
Первинні метаболічні стани |
|
Дефіцит мінералів або вітамінів: цинк (ентеропатичний акродерматит), піридоксин і ніацин |
|
Інше |
|
Шкірні інфекції: ВІЛ-асоційовані, імпетиго, себорейний дерматит |
|
Реакції на ліки |
|
Злоякісні новоутворення: Т-клітинна лімфома шкіри, хвороба Леттерера-Сіве |
IgE: імуноглобулін Е; ВІЛ: вірус імунодефіциту людини.
НАПРАВЛЕННЯ
Пацієнти з рефрактерним АД повинні бути оглянуті фахівцем (наприклад, дерматологом, алергологом), знайомим із поточними рекомендаціями щодо лікування та використанням лікування другої лінії, наприклад біопрепаратів, інших системних препаратів та фототерапії. Через невелику кількість рандомізованих досліджень лікування рефрактерного АД у дітей вікової групи клініцисти дуже різняться у застосуванні терапії другої лінії для дітей із тяжким захворюванням.
УПРАВЛІННЯ
Для лікування рефрактерного АД у дітей і підлітків існує ряд системних методів лікування. Однак важливо зазначити, що АД є хворобою, яка триває протягом усього життя, і початок системної терапії слід ретельно обдумати.
Оптимізація місцевої терапії
Основні принципи.
Після виключення факторів, потенційно пов’язаних із стійкою хворобою, наш початковий підхід полягає в спробі оптимізувати місцеве лікування протягом кількох тижнів. Це допоможе визначити тих дітей, які є кандидатами для терапії другої лінії. Щоб оптимізувати місцеве лікування:
- Переконайтеся, що використовується місцевий препарат відповідної сили, який, як очікується, зніме спалах приблизно через 5-10 днів
- Почніть лікування при перших ознаках спалаху
- Продовжуйте лікування до повного зникнення уражень шкіри
Вологі обгортання та проактивна терапія є додатковими методами, які допомагають оптимізувати місцеве лікування та, у багатьох ситуаціях, можуть подовжити інтервал між загостреннями.
Терапія вологим обгортанням — для дітей зі стійким тяжким АД, незважаючи на оптимальне лікування місцевими кортикостероїдами та/або місцевими інгібіторами кальциневрину, а також для дітей із гострим генералізованим загостренням АД ми пропонуємо терапію вологим обгортанням місцевими кортикостероїдами низької та середньої дії один-два рази на день протягом 3-5 днів і до 14 днів. Вологі обгортання можна тримати протягом двох або більше годин, залежно від переносимості, і навіть протягом ночі, якщо пацієнт почувається комфортно. Вологі обгортання також можна застосовувати протягом короткого часу (наприклад, від 15 до 30 хвилин) два або три рази на день.
● Застосування – вологі обгортання складаються з нижнього вологого шару та верхнього сухого шару. Зазвичай їх наносять поверх пом’якшувальних засобів та/або місцевих кортикостероїдів і залишають на місці до 24 годин. Бавовняний одяг у два шари може бути достатнім у деяких випадках, але еластичні бавовняні трубчасті бинти відповідного розміру, які можна розрізати, щоб закрити будь-яку частину тіла, можуть бути більш зручними в деяких ситуаціях. Спеціальні боді для терапії вологим обгортанням для немовлят і малюків також доступні у продажу.
Через підвищену системну абсорбцію місцевих кортикостероїдів при вологих обгортаннях деякі експерти запропонували розвести місцеві кортикостероїди низької та середньої ефективності в емолієнтах (наприклад, 1:20 для обличчя та тіла у немовлят і маленьких дітей) і обмежити тривалість лікування протягом кількох днів може знизити ризик пригнічення гіпоталамо-гіпофізарно-надниркової осі. Вимірювання рівня кортизолу в сироватці крові рано вранці натщесерце до і після лікування можна використовувати для оцінки системної абсорбції, хоча це зазвичай не проводиться для короткочасного застосування.
● Ефективність. Дані про ефективність вологих пов’язок є рідкісними та суперечливими через широку варіативність методів лікування (наприклад, тип пов’язки, що використовується, частота накладення, тривалість лікування) та характеристики пацієнта (наприклад, тяжкість AД, площа тіла). залучений). У той час як кілька обсерваційних досліджень і кілька невеликих рандомізованих досліджень підтверджують їх ефективність як короткострокового лікування (від 2 до 14 днів) для швидкої ремісії у дітей з тяжким захворюванням, інші дослідження показують, що вологі обгортання такі ж ефективні, як і звичайне місцеве лікування кортикостероїдами та пом’якшувачами.
● Побічні ефекти – побічні ефекти включають підвищену системну абсорбцію місцевих кортикостероїдів, загальний дискомфорт, озноб і фолікуліт. Повідомлялося про тимчасове зниження рівня кортизолу в сироватці крові рано вранці, хоча короткі курси (<2 тижнів) використання розбавлених кортикостероїдів низької та середньої ефективності не асоціювалися з тривалим пригніченням надниркових залоз.
Проактивна (підтримуюча) місцева терапія — після зменшення епізоду загострення пацієнти можуть продовжувати використовувати місцеву терапію місцевим кортикостероїдом середньої потужності або місцевим інгібітором кальциневрину (такролімус 0,03% або 0,1% або пімекролімус 1%) періодично в області раніше запаленої шкіри, щоб запобігти загостренням і подовжити інтервал між спалахами. Частота застосування проактивної терапії різна, причому деякі клініцисти рекомендують через день або двічі на тиждень протягом 4-12 тижнів.
Пом'якшувальні засоби слід рясно використовувати кілька разів на день.
Якщо пацієнт не реагує на проактивну терапію, нашою наступною лінією терапії є дупілумаб.
Дупілумаб — дітям старше шести місяців і підліткам із рефрактерним АД, який не контролюється оптимізованою місцевою терапією, а також дітям, які відмовляються від вологих обгортань, ми пропонуємо дупілумаб, а не іншу системну терапію.
Дупілумаб — це антагоніст рецептора альфа інтерлейкіну (IL) 4 та IL-13, схвалений Управлінням з контролю за продуктами й ліками США (FDA) для лікування дітей віком ≥6 місяців із помірним або тяжким АД.
● Застосування. Існують три схеми дозування на основі ваги для дітей старше 6 років і на основі віку та ваги для дітей <6 років.
- Діти з масою тіла 60 кг і більше – 600 мг навантажувальної дози, потім 300 мг кожні два тижні
- Діти від 30 до 59 кг – 400 мг навантажувальної дози, потім 200 мг кожні два тижні
- Дітям від 15 до 29 кг – навантажувальна доза 600 мг, потім 300 мг кожні чотири тижні.
- Діти від 6 місяців до 5 років – 200 мг кожні 4 тижні для дітей вагою від 5 до 15 кг і 300 мг для дітей вагою від 15 до 30 кг, особливо без навантажувальної дози.
● Ефективність.
Доступні дані щодо застосування дупілумабу дітям віком від шести місяців і підліткам. Результати рандомізованих досліджень, що оцінюють безпеку, фармакокінетику та ефективність дупілумабу у дітей ясельного віку, дітей та підлітків, можна порівняти з результатами досліджень дорослих. У порівнянні зі звичайними імуносупресивними препаратами, дупілумаб має сприятливий профіль безпеки і може використовуватися для тривалого лікування АД.
Терапія другої лінії
Діти від шести місяців до шести років
Циклоспорин. Циклоспорин є нашим імуносупресивним засобом першого вибору для дітей і підлітків з рефрактерним АД, для яких дупілумаб, інші дозволені системні засоби та фототерапія є недоступними, небажаними або неефективними. Циклоспорин має швидкий початок дії, і його ефекти можна помітити в перші кілька тижнів лікування.
● Застосування. Циклоспорин призначають у дозі від 3 до 5 мг/кг/день у два прийоми протягом двох-чотирьох місяців. Потім дозу можна поступово зменшувати протягом кількох місяців (наприклад, на 1 мг/кг/добу кожні один-три місяці) і припинити, коли досягнуто стабільного покращення. Після цього інтермітуюча терапія 3 мг/кг або 5 мг/кг на день двічі на тиждень (наприклад, у суботу та неділю) може бути варіантом для запобігання рецидивам при мінімізації токсичності.
● Моніторинг. Під час лікування слід контролювати функцію нирок і печінки. Необхідно контролювати мінімальні рівні циклоспорину, якщо клінічна відповідь є неадекватною. Побічні ефекти включають нефротоксичність, гепатотоксичність, гіпертензію, гіпертрихоз, підвищений ризик інфекції та злоякісних новоутворень.
● Ефективність. У рандомізованому дослідженні 2023 року порівнювали пероральний прийом циклоспорину 4 мг/кг/день і пероральний прийом метотрексату 0,4 мг/кг/тиждень протягом 36 тижнів у 103 дітей віком від 2 до 16 років із важким, непокірним АД (індекс оцінки атопічного дерматиту [SCORAD] ≥ 30 і неадекватна відповідь на потужне місцеве лікування, без попереднього впливу системних імунодепресантів або біопрепаратів). На 12-му тижні пацієнти в групі циклоспорину відчули більше покращення SCORAD порівняно з пацієнтами в групі метотрексату. Однак на 36-му тижні різниці між двома методами лікування не було. Після припинення лікування загострення були більш поширеними в групі циклоспорину. Найчастішими побічними ефектами були загострення АД (43 відсотки), головний біль (27 відсотків) і аномальна швидкість клубочкової фільтрації (27,5 відсотка) у групі циклоспорину, а також нудота (43 відсотки), загострення АД (29 відсотків) і втома (23). відсотків) у групі перорального метотрексату.
Метотрексат — для дітей із тяжким АД, у яких лікування циклоспорином протипоказано або не переноситься, метотрексат є альтернативним варіантом лікування. Метотрексат має повільний початок дії, і його ефекти стають очевидними через 6-8 тижнів лікування.
● Застосування.
Зазвичай ми починаємо з дози 0,5 мг/кг перорально один раз на тиждень. Дозу можна поступово збільшувати залежно від переносимості до максимальної 25 мг на тиждень. Для зниження токсичності метотрексату без втрати ефективності рекомендується пероральний прийом фолієвої кислоти 1 мг на день.
● Ефективність. Дослідження метотрексату для лікування БА у дітей обмежуються декількома ретроспективними дослідженнями і невеликими клінічними дослідженнями.
- У рандомізованому дослідженні за участю 103 дітей віком від 2 до 16 років із тяжким АД метотрексат у дозі 0,1 мг/кг/тиждень на 0-му тижні, а потім у дозі 0,4 мг/кг/тиждень (максимальна доза 25 мг перорально на тиждень) був таким же ефективним, як і циклоспорин у дозі 4 мг/ тиждень. кг/день на 36 тижні. За словами пацієнтів, спалахи після припинення лікування виникали рідше в групі метотрексату, ніж у групі циклоспорину (29 проти 43 відсотків). Нудота та втома були найпоширенішими побічними ефектами метотрексату.
- У ретроспективному дослідженні, яке включало 47 дітей віком від 2 до 18 років із тяжким АД, метотрексат у дозі від 0,2 до 0,5 мг/кг/тиждень викликав полегшення екземи, зменшення свербежу та зменшення використання місцевих кортикостероїдів через три-п’ять місяців. Повідомлялося про стійке покращення через 10-14 місяців серед 30 дітей, які пройшли принаймні 10 місяців лікування. Приблизно у 70 відсотків пацієнтів спостерігалося легке загострення під час терапії метотрексатом, яка лікувалася місцевими кортикостероїдами, незначною корекцією дози метотрексату або обома. Побічні ефекти були зареєстровані у 83 відсотків пацієнтів і включали легке підвищення рівня трансаміназ, нудоту, блювання та біль у животі.
- В іншому ретроспективному дослідженні за участю 55 дітей віком від 3 до 19,5 років із важким, тривалим АД, які отримували метотрексат у середній початковій дозі 0,37 мг/кг, у 42 пацієнтів (76 відсотків) спостерігалося покращення зі зниженням середнього вихідного рівня. Загальна оцінка дослідника (IGA) оцінка від 4,2 до 2,9 після шести-дев’яти місяців лікування. Побічні ефекти спостерігалися у 51 відсотка пацієнтів, найчастіше шлунково-кишковий дискомфорт і нудота (31 відсоток), потім втома (26 відсотків) і головний біль (16 відсотків).
● Побічні ефекти – Метотрексат є антагоністом фолієвої кислоти, який пригнічує реакції трансметилювання та сприяє вивільненню аденозину. Протизапальна дія метотрексату може бути зумовлена пригніченням проліферації лімфоцитів і протизапальною активністю аденозину. Метотрексат, як правило, добре переноситься. Побічні ефекти включають шлунково-кишкові розлади, гепатотоксичність, пригнічення кісткового мозку та, дуже рідко, гострий ідіопатичний легеневий фіброз.
Діти старше 6 років
Фототерапія — для дітей старше 6 років, які можуть співпрацювати з лікуванням, і підлітків із рефрактерним АД, для яких дупілумаб є небажаним, недоступним або неефективним, ми пропонуємо фототерапію вузькосмуговим ультрафіолетом B (NBUVB), якщо це можливо та прийнятно для пацієнтів або осіб, які доглядають за ними. Через свій сприятливий профіль безпеки NBUVB є більш відповідним початковим вибором, ніж інші форми фототерапії (наприклад, ультрафіолет A1 [UVA1], псоралени плюс ультрафіолет A [PUVA], широкосмуговий ультрафіолет B [UVB]).
Загалом лікування добре переноситься. Однак, враховуючи непрактичність частих візитів до клініциста для цього лікування та доступність нових системних методів, фототерапія зараз використовується рідше.
● Введення – NBUVB зазвичай використовується тричі на тиждень за прогресивним протоколом, який збільшує дозу з кожним лікуванням залежно від переносимості. Пацієнта зазвичай повторно оцінюють після 20-25 процедур.
● Ефективність. Дані щодо ефективності фототерапії NBUVB у дітей з АД обмежені кількома ретроспективними серіями випадків і одним проспективним дослідженням. В одному дослідженні, яке включало 25 дітей з АД, 17 досягли майже чистої або чистої шкіри з медіаною 24 процедур.
● Побічні ефекти – Короткострокові побічні ефекти NBUVB включають еритему, утворення пухирів, реактивацію простого герпесу. Немає досліджень, які б оцінювали канцерогенний ризик фототерапії у дітей з АД. Хоча систематичний огляд чотирьох досліджень, що оцінюють ризик раку шкіри серед дорослих і дітей з псоріазом, які отримували NBUVB, не виявив підвищеного ризику меланоми або немеланомного раку шкіри, пацієнтів, які отримують NBUVB фототерапію, слід спостерігати за допомогою щорічного огляду шкіри.
ДЖЕРЕЛО: https://www.uptodate.com
На платформі Accemedin багато цікавих заходів! Аби не пропустити їх, підписуйтесь на наші сторінки! Facebook. Telegram. Viber. Instagram.
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу

Міжнародний день людини з синдромом Дауна

Working with vulnerable children: therapeu ...
FDA схвалило терапію Nedosiran для рідкіс ...
Поздовжня ентеропластика, як спосіб первин ...

Вплив середовища на мінеральну щільність к ...

Контрацепція: консультування та вибір