Клінічна настанова: Діагностика та лікування Целіакії та хвороби Крона. Частина 2
Дата публікації: 05.10.2023
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: лікування, хвороба Крона, менеджмент, целіакія
Менеджмент Целіакії:
Як правило, існує шість ключових елементів у веденні пацієнтів з целіакією, які можна підсумувати:
- Консультація кваліфікованого дієтолога.
- Освіта про хворобу.
- Довічне дотримання безглютенової дієти.
- Виявлення та лікування дефіциту харчування.
- Доступ до адвокаційної групи.
- Постійне довготривале спостереження мультидисциплінарною командою.
|
Дієтичне харчування |
Як загальні правила, наступні дієтичні поради можна дати всім пацієнтам: ● Слід уникати продуктів, що містять пшеницю, жито та ячмінь. ● Безпечними є соєве або тапіокове борошно, рис, кукурудза, гречка та картопля. ● Уважно читайте етикетки на готовій їжі та приправах, звертаючи особливу увагу на добавки, такі як стабілізатори або емульгатори, які можуть містити глютен. ● Дистильовані алкогольні напої та оцет, а також вино не містять глютену. Однак слід уникати пива, елю, лагеру та солодового оцту, оскільки вони часто виготовляються із зерен, що містять глютен, і не дистильовані. Проте в Європі зараз продається безглютенове пиво, яке можна придбати по всьому світу. ● Молочні продукти спочатку можуть погано переноситися, оскільки багато пацієнтів з целіакією можуть мати вторинну непереносимість лактози. ● Овес слід вводити в раціон з обережністю, враховуючи різновид вівса зі змінною токсичністю та невизначеність щодо того, чи вважається овес, позбавлений глютену під час збирання, безпечним для всіх людей з целіакією |
|
Контроль дієти |
IgA антитканинна трансглютаміназа (tTG) або IgA (або IgG) дезамідований гліадиновий пептид (DGP) слід використовувати для моніторингу відповіді на безглютенову дієту. Ми проводимо серологічні дослідження через 6 і 12 місяців після первинного діагнозу целіакії та щорічно після цього |
|
Заповнення дефіциту поживних речовин |
Пацієнти повинні перевірятися на дефіцит вітамінів (A, D, E, B12), міді, цинку, каротину, фолієвої кислоти , феритину, заліза та вимірювати протромбіновий час (ПЧ) на предмет потенційного дефіциту вітаміну К. Дефіцит тіаміну, вітаміну B6, магнію та селену також може виникнути залежно від тяжкості захворювання та раціону харчування, і його слід перевірити за наявності клінічних ознак або симптомів дефіциту. Безглютенова дієта може спричинити закреп, оскільки в ній мало грубої їжі. Це зазвичай реагує на додавання клітковини з лушпинням насіння псиліуму |
|
Профілактика втрати кісткової маси |
Значна частина втрати кісткової маси пов’язана з вторинним гіперпаратиреозом, який, ймовірно, пов’язаний з дефіцитом вітаміну D. Пацієнти з пізньою стадією захворювання можуть мати біль у кістках, псевдопереломи або деформацію, але більшість пацієнтів протікають безсимптомно або мають лише підвищений рівень лужної фосфатази в сироватці крові або гіпокальціємію. Це можна лише частково змінити за допомогою безглютенової дієти; втрата щільності кісткової тканини в периферичному скелеті може зберігатися, незважаючи на очевидну нормалізацію в аксіальних ділянках скелета. Пацієнти з діагнозом целіакія повинні бути оцінені на втрату кісткової маси за допомогою DXA (двоенергетична рентгенівська абсорбціометрія). Моніторинг шляхом повторного сканування DXA через один рік корисний у пацієнтів з остеопенією, оскільки він дозволяє оцінити швидкість зміни мінеральної щільності кісткової тканини |
|
Пневмококова вакцинація |
Целіакія пов’язана з гіпоспленізмом. Тому рекомендується профілактичне введення пневмококової вакцини. Рекомендуємо прочитати клінічні настанови: Профілактика інфекції у пацієнтів з порушенням функції селезінки |
|
Менеджмент герпетиформного дерматиту |
Поліпшення герпетиформного дерматиту після відміни глютену може бути значно відстроченим (від 6 до 12 місяців) порівняно з реакцією кишкових проявів захворювання. Як наслідок, лікування сульфонами (такими як дапсон 100 мг/день) на додаток до уникнення глютену може бути необхідним для досягнення швидкого контролю |
|
Дослідницькі підходи |
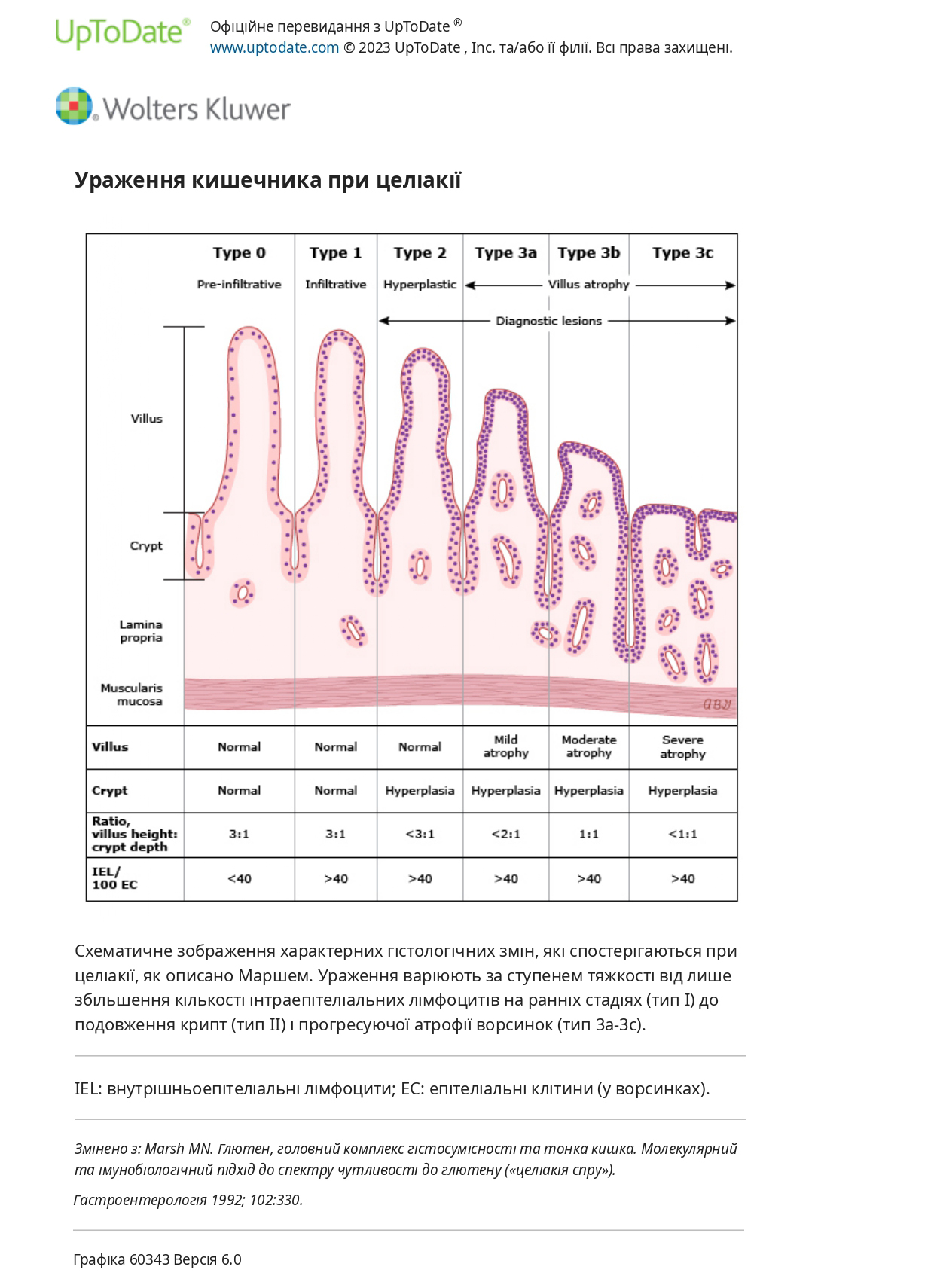
Інгібітор трансглутамінази 2 — інгібування трансглутамінази 2 було оцінено у пацієнтів з целіакією. У рандомізованому дослідженні 159 дорослих із добре контрольованою целіакією отримували одну з трьох доз (10 мг, 50 мг, 100 мг) селективного перорального інгібітора трансглутамінази 2 або плацебо протягом шести тижнів під час щоденного прийому глютену ( 3 грами/день). Лікування пероральним інгібітором трансглутамінази 2 у всіх трьох дозах значно послаблювало спричинене глютеном пошкодження слизової оболонки дванадцятипалої кишки, що вимірювалося за відношенням висоти ворсинок до глибини крипт, порівняно з плацебо |
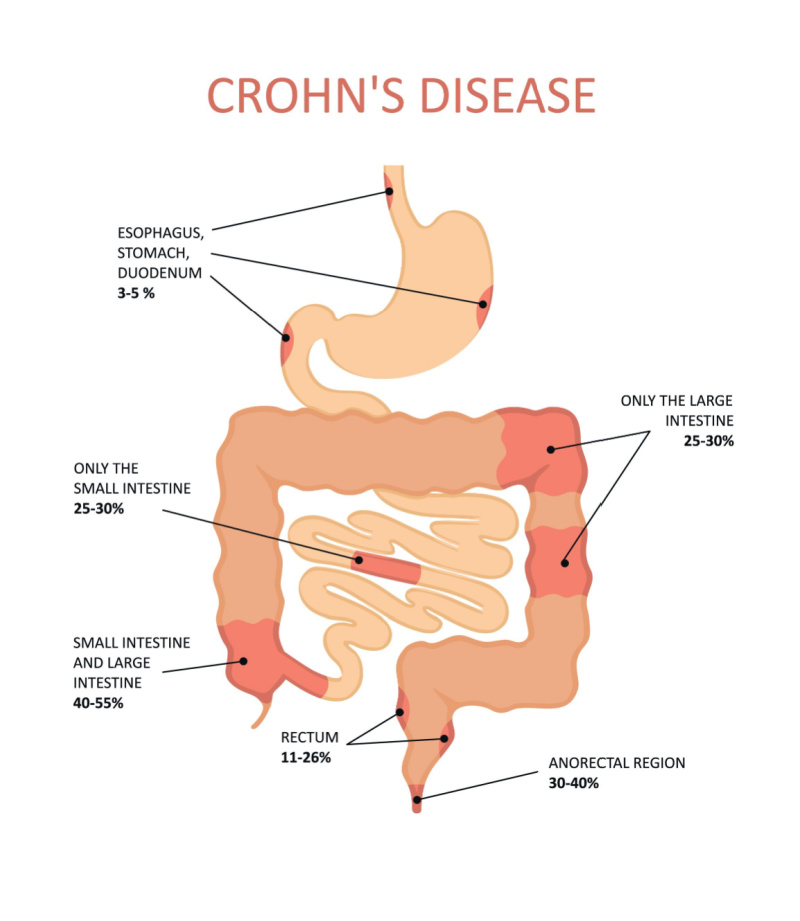
Менеджмент хвороби Крона:
Вибір терапії залежить від анатомічної локалізації захворювання, тяжкості захворювання та від того, чи є метою лікування індукція ремісії чи підтримка ремісії. Лікарська терапія, яка використовується для хвороби Крона, включає:
- Пероральні 5-аміносаліцилати (наприклад, сульфасалазин, мезаламін).
- Глюкокортикоїди (наприклад, преднізон, будесонід).
- Імуномодулятори (наприклад, азатіоприн, 6-меркаптопурин, метотрексат).
- Біологічна терапія (наприклад, інфліксимаб, адалімумаб, цертолізумаб пегол, наталізумаб, ведолізумаб, устекінумаб).
Тут буде розглядатись менеджмент легкої форми хвороби Крона.
|
Індекс активності хвороби Крона |
Дві системи, які часто використовуються, це індекс активності хвороби Крона (CDAI) (калькулятор 1) та індекс Харві-Бредшоу (HBI) (калькулятор 2), який є спрощеною похідною від CDAI. |
|
Кроки терапії: |
|
|
Поступова терапія |
Поступова терапія зазвичай починається з менш сильних ліків, які часто пов’язані з меншою кількістю побічних ефектів. Більш потужні та потенційно більш токсичні препарати використовуються лише в тому випадку, якщо початкова терапія неефективна |
|
Низхідна терапія |
Низхідна терапія починається з більш потужних методів лікування, таких як біологічна терапія та/або імуномодулююча терапія, на відносно ранньому етапі захворювання до того, як пацієнти стануть залежними від глюкокортикоїдів, і, можливо, навіть до того, як вони отримають глюкокортикоїди |
|
Мета лікування |
Метою лікування пацієнтів із хворобою Крона є досягнення ремісії (ендоскопічної, гістологічної та клінічної) шляхом демонстрації повного загоєння слизової оболонки |
|
Будесонід |
Рекомендується будесонід , вкритий кишковорозчинною оболонкою, як лікування першої лінії для індукції ремісії у пацієнтів з низьким рівнем ризику з помірно активною хворобою Крона клубової та проксимальної кишки. Будесонід із контрольованим вивільненням у клубовій кишці є кортикостероїдом із високим метаболізмом першого проходження через печінку. Будесонід починають з дози 9 мг на день протягом щонайменше чотирьох тижнів, але не більше восьми тижнів. Потім дозу будесоніду зменшують на 3 мг кожні два-чотири тижні протягом загального періоду терапії від восьми до 12 тижнів. Після досягнення ремісії у пацієнтів з легким ступенем хвороби Крона з первинним ураженням дистального відділу клубової кишки та правого відділу товстої кишки та зниження або припинення прийому будесоніду можна розпочати підтримуючу терапію. Пацієнтам, які не можуть успішно зменшити дозу будесоніду протягом трьох-шести місяців, показане посилення лікування тіопурином або біологічними препаратами, подібно до лікування хвороби Крона середнього та тяжкого ступеня |
|
Преднізолон |
Пероральні глюкокортикоїди (тобто преднізон і преднізолон ) є альтернативою початкової терапії для пацієнтів із легкою формою хвороби Крона, що вражає клубову та/або проксимальну кишку. Преднізон можна призначати пацієнтам з низьким ризиком, які не реагують на будесонід; однак пацієнти, які спочатку реагують на пероральні глюкокортикоїди, але не можуть переносити поступове зниження дози преднізону, більше не вважаються групою низького ризику і повинні бути перенесені до категорії середнього/високого ризику. Початкова доза преднізону становить 40 мг на день протягом одного тижня, і багато пацієнтів відреагують на цю дозу. У цей момент слід розпочати поступове зниження дози на 5-10 мг на тиждень з метою припинення прийому преднізону протягом одного-двох місяців |
|
5-аміносаліцилати |
Застосування 5-аміносаліцилатів (5-ASA) при хворобі Крона є суперечливим, і ми обмежуємо його використання пацієнтами з легкою формою хвороби Крона з обмеженим ураженням клубово-ободової кишки, які вважають за краще уникати глюкокортикоїдів. Для таких пацієнтів підходить пероральний препарат 5-ASA з повільним вивільненням, такий як мезаламін |
|
Дифузний коліт або ураження лівого відділу товстої кишки |
Для пацієнтів із легким дифузним колітом Крона або лівобічним захворюванням товстої кишки ми пропонуємо початкову терапію пероральним преднізоном у дозі 40 мг на день протягом одного тижня. У цей момент слід розпочати поступове зниження дози на 5-10 мг на тиждень з метою припинення прийому преднізону протягом одного-двох місяців |
|
Безсимптомні пацієнти, діагностовані випадково |
Для безсимптомних пацієнтів, які проходять звичайну скринінгову колоноскопію та випадково виявили дуже маленькі, неглибокі афти, повторна ілеоколоноскопія виконується через 6-12 місяців на додаток до клінічного моніторингу |
Інші локалізації захворювання:
|
Ураження порожнини рота |
Афтозні виразки, найпоширеніші ураження ротової порожнини, виникають у 20-30 відсотків дорослих пацієнтів із хворобою Крона. Афтозні виразки можуть вказувати на легке захворювання, яке відповідає запаленню кишечника, або більш серйозний прояв хвороби Крона. Хвороба Крона найчастіше уражає слизову оболонку губ і щік. Було описано широкий спектр додаткових уражень, включаючи набряк щік, гранулематозні утворення, хейліт і гранулематозний сіаладеніт. Ці аномалії можуть бути серйозними та домінувати в клінічній картині, спричиняючи дискомфорт, який перешкоджає пероральному прийому. Ураження порожнини рота зазвичай супроводжуються кишковими захворюваннями та реагують на лікування, спрямоване на кишкові захворювання. Ліки місцевого застосування, наприклад тріамцинолону ацетоніду, може забезпечити місцеве полегшення симптомів |
|
Періанальне захворювання |
Повне закриття фістули є основною терапевтичною метою для більшості пацієнтів. Для деяких пацієнтів зі складними періанальними норицями досяжною метою терапії є симптоматичне покращення (наприклад, зменшення болю в прямій кишці, зменшення дренажу) і покращення якості життя, але без повного загоєння та закриття фістули |
|
ПІДТРИМАННЯ РЕМІСІЇ |
Пацієнтам із незначною формою хвороби Крона з низьким ризиком, які досягли ремісії за допомогою глюкокортикоїдів (наприклад, будесоніду або преднізону ), ми рекомендуємо поступово зменшувати дозу глюкокортикоїдів, а потім припинити дозу з подальшим клінічним спостереженням та ілеоколоноскопією через 6–12 місяців |
|
Моніторинг під час ремісії |
На додаток до клінічного обстеження пацієнтів та за допомогою ілеоколоноскопії через 6-12 місяців після досягнення клінічної ремісії можуть бути корисними неінвазивні маркери запалення. Ми отримуємо неінвазивні маркери запалення, включаючи С-реактивний білок (СРБ) і фекальний кальпротектин під час колоноскопії, і корелюємо ці тести зі ступенем загоєння слизової оболонки. У деяких пацієнтів із хворобою Крона СРБ не корелює з ендоскопічними результатами, і ми не покладаємося лише на неінвазивні маркери для моніторингу пацієнтів у стані ремісії |
|
ІНШІ СПОСОБИ ТЕРАПІЇ |
|
|
Протидіарейні препарати |
Симптоматичне лікування протидіарейними препаратами є варіантом для пацієнтів, які не відповідають повністю на терапію першої лінії та мають легку форму хвороби Крона без ускладнень, таких як стриктури. Пацієнти з помірною або тяжкою хворобою Крона або пацієнти з ризиком кишкової непрохідності не повинні отримувати протидіарейні засоби. Ми пропонуємо лоперамід у разі потреби в малих дозах (тобто від 2 до 4 мг після епізоду рідкого стільця) для лікування діареї в цій ситуації через його ефективність і відносну безпеку в низьких дозах. Холестирамін або інші секвестранти жовчі є іншими варіантами для пацієнтів із нестриктурним захворюванням клубової кишки, які мають хронічну водянисту діарею |
|
Пробіотики |
Наявні дані не підтверджують клінічну ефективність пробіотичної терапії ні для індукції, ні для підтримки ремісії у пацієнтів із хворобою Крона |
|
Антибіотики |
Ми зазвичай не використовуємо антибіотики для пацієнтів із легкою формою хвороби Крона. Дані, що стосуються використання антибіотиків для лікування активної люмінальної хвороби Крона, були дещо суперечливими |
|
Дієтичні втручання |
Пацієнти з хворобою Крона, особливо із захворюванням клубової кишки, мають підвищену частоту набутої лактазної недостатності та симптоматичної непереносимості лактози. Якщо є підозра на непереносимість лактози, ми пропонуємо емпіричне дослідження уникнення лактози. Якщо діагноз викликає сумніви, можна провести водневий тест на лактозу. Якщо пацієнт реагує на уникання лактози або якщо дихальний тест позитивний, пацієнта слід проінструктувати уникати продуктів, що містять лактозу. Пацієнтам з обмеженим споживанням лактози слід призначати добавки кальцію, щоб мінімізувати ризик втрати кісткової маси. Інші дієтичні втручання, включаючи полівітаміни та харчові добавки, а також елімінаційні дієти у пацієнтів із хворобою Крона, спрямовані на покращення харчування та усунення харчових тригерів |
ДЖЕРЕЛО: https://www.uptodate.com/
Клінічна настанова: Діагностика та лікування Целіакії та хвороби Крона. Частина 1
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу

Вплив післяопераційного лікування остеопор ...

Нові клінічні рекомендації EASL щодо транс ...

Що потрібно знати про траншейну стопу?

Ольга Голубовська застерегла про початок с ...

Запис вебінару «Корисні аспекти ЕКГ у клін ...

Тривалий COVID пов'язаний з новими алергія ...