У пошуках вакцини від лейшманіозу
Дата публікації: 29.08.2023
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: вакцина, лейшманіоз, кала-азар, аденовірусний вектор

У Східній Африці вісцеральний лейшманіоз викликається одноклітинним паразитом під назвою Leishmania donovani, який передається через укуси самок піщаної мухи (Phlebotomus spp.). Потрапляючи в організм, найпростіші вражають імунні клітини. Через кілька місяців хвороба проявляється лихоманкою, анемією та набряком селезінки та печінки. «Вісцеральний лейшманіоз є вбивцею, якщо його не лікувати», — каже Елені Аєле, лікар з Університету Гондар у північній Ефіопії. А біженці та переміщені особи в регіоні є особливо вразливими.
Піщані мухи, які передають хворобу, процвітають в акацієвих лісах у прикордонних регіонах Ефіопії та Судану, а сон на відкритому повітрі підвищує ризик укусу людини. Укус не є гарантією розвитку захворювання.
«У середньому лише одна з десяти осіб, в організм яких потрапляє паразит, розвиває хворобу», — каже Керт Рітмейер, медичний учений з Амстердама з міжнародної організації допомоги «Лікарі без кордонів» (MSF, також відомої як «Лікарі без кордонів») — «Інші дев'ять вироблять природний імунітет».
Однак біженці знову опиняються в невигідному становищі: недоїдання під час конфлікту послаблює імунну систему людей, роблячи їх більш сприйнятливими до розвитку хвороб. Перенаселеність таборів також може сприяти передачі.
Частина програми Nature Outlook: забуті тропічні хвороби
Зв'язок між конфліктом і вісцеральним лейшманіозом було показано неодноразово. Після початку громадянської війни в 1983 році на території сучасного Південного Судану протягом наступного десятиліття приблизно одна третина чи близько 280 000 населення одного штату померла від вісцерального лейшманіозу. Коли у 2013 році в країні знову спалахнула війна, кількість випадків захворювання в деяких східних штатах зросла більш ніж утричі. А в Ефіопії, каже Аєле, війна призвела до збільшення кількості людей із пізньою стадією захворювання, тому що люди рідше зверталися до лікарні.
Остання війна в Судані спалахнула у квітні, і деякі мирні жителі тікають у сільські райони, відомі як гарячі точки лейшманіозу. Абхай Сатоскар, паразитолог з Університету штату Огайо в Колумбусі, відвідав лікарню в східному Судані в грудні минулого року і на власні очі побачив людей з цією хворобою. Він був свідком таборів з десятками тисяч людей, які тікали від конфлікту в Ефіопії, включаючи багатьох дітей, які раніше не заражалися цією хворобою. «Табори знаходяться в ендемічних районах, і вони очікують великого спалаху там», — каже Сатоскар. За його словами, приблизно 90% місцевих жителів у деяких селах мають ознаки попередньої інфекції.
Потреба в ефективних засобах захисту від хвороби очевидна, але знайти їх виявилося складно. Піщаних мух важко контролювати — вони менші за комарів, практично безшумні й не потребують води для відкладання яєць. Хвороба також важко піддається лікуванню. У Східній Африці стандартною терапією є прийом двох ін’єкційних препаратів щодня протягом 17 днів — важке завдання за найкращих обставин і майже неможливе в зоні конфлікту в країні з низькими ресурсами. Ліки також можуть бути токсичними для серця та інших органів, а ін’єкції болючі. Тому надії багатьох покладаються на вакцинацію. Ефективна вакцина може запобігти захворюванням і зупинити передачу. Десятиліття роботи досі не спромоглися створити вакцину проти лейшманіозу. Але тепер дослідники, які переслідують дві дуже різні стратегії вакцин, рухаються до випробувань на людях. Успіх будь-якої з них означатиме гігантський крок до боротьби з хворобою, яка жорстоко вражає людей, які вже опинилися в складних ситуаціях.
За межами традиційного
Сатоскар оптимістично дивиться на перспективу щеплення від лейшманіозу. «Імунологія та історія говорять нам, що вакцинація можлива», — каже він. Століттями бедуїни на Близькому Сході натирали вміст паразитарних виразок інфікованої людини на здебільшого приховані ділянки шкіри своїх дітей, наприклад сідниці. Ця практика навмисного зараження — відома як лейшманізація — викликала у дітей шкірні ураження, типові для форми хвороби, яка називається шкірним лейшманіозом. Але найважливіше те, що після одужання діти будуть захищені від майбутніх інфекцій. «Це майже як вакцина», — каже Сатоскар. Шрамів на обличчі, які, як боялися батьки, зашкодять перспективам одруження їхньої дитини, можна було уникнути, хоч і шляхом плям на менш помітних частинах тіла.
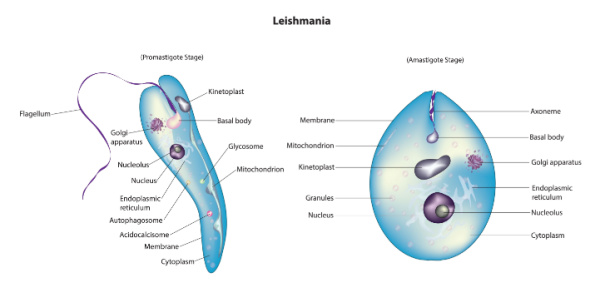
Хоча шкірні форми захворювання, наприклад, спричинені основними паразитами Leishmania, присутніми в регіоні, рідше смертельні, ніж вісцеральний лейшманіоз, наслідки все одно значні. «Ми називаємо їх менш важкими формами захворювання, але це не те, про що ви думаєте, якщо коли-небудь сідаєте з інфікованими дітьми й бачите ураження на їхній шкірі», — каже Натан Пітерс, імунолог з Університету Калгарі в Канаді. Шкірна форма захворювання також поширюється в зонах конфлікту.
Спроби створити вакцину проти всіх типів лейшманіозу, яка б забезпечувала такий же захист, як і лейшманізація, почалися ще в 1940-х роках. Вони були засновані на живих паразитах, але від цього підходу відмовилися після десятиліть роботи, оскільки він міг спровокувати захворювання, такі як великі неконтрольовані ураження шкіри. Потім вакцинологи звернулися до вакцин від убитих паразитів, а в 1980-х і 1990-х роках – до комбінацій білків паразита. Усе закінчилося провалом, незважаючи на спочатку багатообіцяючі результати досліджень на тваринах. Розчарування обчислюються сотнями.
Більшість вакцин працюють, викликаючи реакцію антитіл на частину збудника та закріплюючи цю пам’ять на В-клітинах, які виробляють антитіла. Коли патоген потрапляє в організм, антитіла чекають, щоб прикріпитися до нього та позначити його для знищення.
Це надзвичайно добре спрацювало для багатьох вірусів і бактерій, але одноклітинні організми, такі як Leishmania та паразит Plasmodium, що викликає малярію, є “складнішими клієнтами”. Вони розробили способи підтримувати хронічну інфекцію, маніпулюючи імунною системою та ховаючись у клітинах людини, де антитіла не можуть їх легко знайти та вбити. Замість цього потрібна відповідь Т-клітин — Т-клітини можуть розпізнавати та вбивати інфіковані клітини. На жаль, Т-клітинну відповідь важко індукувати у людей. Крім того, Т-клітини набагато важче вивчити та виміряти, ніж антитіла.
Після десятиліть досліджень вакцина, яка виробляє антитіла для боротьби з малярією, спричиненою Plasmodium falciparum, отримала рекомендацію ВООЗ в жовтні 2021 року. Зараз розробляються інші вакцини проти малярії, які надихають дослідників лейшманіозу.
Сучасні технології в арсеналі лікарів та епідеміологів
В Університеті Оксфорда, Великобританія, дослідники використовували сконструйовані віруси, які називаються аденовірусними векторами, щоб навчити Т-клітини організму знищувати малярійних паразитів, які ховаються в організмі. Переносник діє, проникаючи в клітини печінки та змушуючи їх виробляти білки малярійних паразитів. Потім ці білки відображаються на поверхні клітин, на якій їх помічають Т-клітини, які потім знищують інфіковані клітини. Вакцина проти малярії, розроблена на основі такої технології, має на меті спровокувати тривалу пам’ять про інфекцію, щоб Т-клітини могли швидко реагувати, якщо справжній паразит коли-небудь потрапить в організм.
Для деяких дослідників лейшманіозу розвиток вакцин, які використовують аденовірусні вектори, відкриває можливість. Пол Кей, імунолог з Університету Йорка, Велика Британія, каже, що він і його команда намагалися інвестувати в вакцини, які використовують ці вектори. Кей працює над перенесенням генетичного рецепта двох білків Leishmania в клітини за допомогою аденовірусного вектора. Потім Т-клітини розпізнають і вбивають ці паразитовані імунні клітини, а також встановлюють пам’ять. «Ми знаємо, що вірусно-векторні вакцини добре справляються зі створенням Т-клітин CD8, які відіграють роль у захисті від лейшманії, і Т-клітин CD4», — каже Пітерс.
У 2017 році Кей та його колеги повідомили, що вакцину-кандидата можна безпечно вводити людям. Подальше невелике дослідження в Судані надало деякі докази імунної відповіді у людей, які перенесли ускладнення вісцерального лейшманіозу, що вражає шкіру та може виникнути після лікування. Потім вакцину ввели більшій когорті з приблизно 80 осіб, але цьогорічні заворушення в Судані ускладнили завершення цього дослідження. Зіштовхнувшись із цією вимушеною перервою, команда Кея зараз розглядає можливість переходу на аденовірусний вектор, який використовувався у вакцині проти COVID-19, оскільки під час пандемії багато дізналися про цей носій вакцини. Але все ще незрозуміло, чи зможе вірусний вектор генерувати достатньо Т-клітин пам’яті, щоб зупинити лейшманіозу інфекцію, перш ніж вона пошириться.
Живі та бойові
Інша стратегія імунізації прагне більш точно відповідати тому, що відбувається під час природних інфекцій. Як правило, коли людину кусає піщана муха, слина та мікроби комахи притягують до місця укусу перші імунні клітини. Потім паразит проникає в ці імунні клітини і створює стійку інфекцію. «Існує величезний еволюційний тиск на паразитів, щоб викликати ці хронічні інфекції, щоб вони могли зберігатися достатньо довго, щоб їх підхопила інша піщана муха», — каже Девід Сакс, паразитолог з Національного інституту алергії та інфекційних захворювань США (NIAID). Як відомо бедуїнам, людина, яка була інфікована, має імунітет до вторинних інфекцій, і вважається, що цей ефект значною мірою залежить від Т-клітин. Тепер група дослідників у Північній Америці хоче імітувати цей процес, повернувшись до ідеї живої вакцини. «По суті, це лейшманізація, за винятком безпечного та визначеного продукту», — каже Сатоскар.
Група під керівництвом Хіри Нахасі, паразитолога та вакцинолога з FDA в Сільвер-Спрінг, штат Меріленд, послабила L. donovani шляхом інактивації гена. Коли його давали мишам і хом’якам, ослаблений паразит міг інфікувати клітини, але коли він потрапив усередину, йому було важко рости. «Вони зберігаються протягом 7-9 місяців, а потім починають вмирати», не викликаючи захворювання у тварин, каже Сатоскар, який є частиною дослідницької групи. Здавалося, що це забезпечує довгостроковий захист мишей і хом’яків від майбутньої інфекції.
Команда тепер переключила свою увагу на паразитів L. major, знайдених на Близькому Сході, які, на відміну від L. donovani, зазвичай залишаються в шкірі й, отже, повинні нести менший ризик. Дослідники сподіваються, що види достатньо схожі, щоб вакцина на основі ослаблених паразитів L. major забезпечила захист від широкого спектра видів, які викликають шкірні та вісцеральні захворювання, а також від інших видів, таких як Leishmania braziliensis, який викликає ураження слизових оболонок. оболонки носа, рота і горла.
Навіть ін’єкція генетично ослаблених паразитів не є повною копією природної інфекції Leishmania. Ослаблені паразити можуть існувати протягом багатьох місяців — достатньо довго, щоб створити імунну пам’ять, сподіваються дослідники, — але природна інфекція може призвести до того, що паразити залишаються в організмі на низьких рівнях на все життя. «Коли ви виконуєте лейшманізацію, ви заражаєтеся назавжди, і це забезпечує гарний захист від подальших викликів», — каже Пітерс. Деякі дослідники вважають, що ці паразити забезпечують Т-клітини постійним підштовхуванням і підтримують готовність організму швидко придушувати будь-які нові вторгнення.
Чи може жива вакцина зрівнятися із захистом, який забезпечує природна інфекція, стане зрозуміло лише після проведення випробувань в ендемічних регіонах. Однак це буде складно. Наприклад, сильні опади в Південному Судані за останні три роки перешкодили розмноженню піщаних мух у тамтешньому ґрунті, пригнічуючи передачу збудника. Це означає, що випробування, створене в одному місці, може мати проблеми з поверненням корисних даних просто тому, що того року було небагато випадків.
У Йорку Кей створив центр тестування вакцин, щоб дізнатися якомога більше про вакцини-кандидати перед тим, як почати польові випробування, щоб довести їх ефективність. Він виростив паразитів L. Major у своїй лабораторії, використовуючи інфіковану тканину молодої людини, яка подорожувала пустелею Негев в Ізраїлі. Близько дюжини волонтерів у Йоркширі відтоді дозволили самкам піщаних мух, які містять цих паразитів, кусати їхні руки. Через два-чотири тижні з’являються невеликі грудочки, які видаляють, щоб у добровольців не розвинувся лейшманіоз (паразити, наявні в Ізраїлі, зазвичай викликають лише легкі захворювання). Зараз група Кея пише свої висновки про ранню імунну відповідь на паразита — те, що важко дослідити в природних умовах, оскільки ознаки інфекції зазвичай з’являються місяцями, і лише тоді люди звертаються до медичних установ.
Наступним кроком для команди Кея є введення своєї вакцини добровольцям, піддавання їх контакту з інфікованими піщаними мухами та перевірка, чи є вона захистом. «Якщо це працює, це дає нам новий поштовх для тестування в реальних умовах», — каже Кей. «Якщо це не спрацює, ми, ймовірно, зупинимося».
Подальший шлях дослідників
Аденовірусні вакцини та живі вакцини не конкурують — кожна має свої переваги. Великим позитивним моментом для аденовірусних вакцин є те, що деякі країни, де лейшманіоз є ендемічним, наприклад Бразилія та Індія, тепер мають потужності з виробництва аденовірусів завдяки зусиллям щодо вакцинації проти COVID-19. Ці кошти можна використати для виробництва вакцин проти лейшманіозу на місцевому рівні. Однак, на відміну від живих вакцин, підхід вірусного вектора досі не показав, що він генерує достатню тривалу Т-клітинну відповідь для захисту від лейшманіозу. «Ви не маєте такої широти імунної відповіді, яку б спостерігали з неушкодженим паразитом», — каже Кей.
Докази природних інфекцій свідчать про те, що живі паразити можуть досягти тривалого захисту, але живі вакцини пов’язані зі значними матеріально-технічними проблемами. На відміну від аденовірусних вакцин, які можна зберігати в холодильнику, вакцину від живих паразитів слід зберігати при температурі — 80°C. Через пандемію COVID-19 інфраструктура доставки вакцин покращилася в таких ендемічних районах, як Східна Африка, але отримати вакцину від живих паразитів у віддалені сільські райони поблизу зон конфлікту все ще буде важко, і, ймовірно, пов’язані з цим витрати будуть більше, ніж для аденовірусної вакцини.
Зробити вакцини доступними для багатьох людей з низьким рівнем доходу, які знаходяться в групі ризику, є важливим для боротьби з цією хворобою. За оцінками Кейя, глобальний попит на вакцину може сягнути одного мільярда доз протягом десятирічного періоду, і що приблизно одна чверть ендемічних країн може дозволити собі заплатити за вакцину з ціною однієї дози близько 5 доларів США.
Навіть найоптимістичніші прогнози свідчать про те, що вакцина буде затверджена через 5–7 років. Кожен із цих років принесе ще півмільйона нових випадків вісцерального лейшманіозу та щонайменше 50 000 смертей. Набагато більше людей матимуть шрами від шкірних захворювань, якими щороку заражається близько півмільйона людей. «Діти можуть перестати ходити до школи, а жінки зазнають дискримінації», — каже Аєле. «У деяких частинах суспільства це вважається прокляттям», — додає вона.
ДЖЕРЕЛО: https://www.nature.com
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу
За 30 років захворюваність на артеріальну ...

Внутрішньосерцева ехокардіографія визнана ...
.jpg)
Клінічне завдання. Анорексія та лихоманка. ...

Перехрещення харчової і сезонної алергії

МОЗ готує новий протокол: лікувальна гіпот ...

Нове дослідження виявило, що шкіра має вла ...


.jpg)
