Клінічні настанови: профілактика інфекції у пацієнтів з порушенням функції селезінки
Дата публікації: 01.09.2023
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: вакцинація, клінічна настанова, аспленія, порушення функції селезінки, Клінічна настанова

ВСТУП
Пацієнти з порушеною функцією селезінки знаходяться в групі ризику серйозних і сильних інфекцій, викликаних інкапсульованими бактеріями (наприклад, Streptococcus pneumoniae), паразитами, що передаються через кров, та іншими інфекціями, у контролі яких селезінка відіграє важливу роль. Основні заходи для запобігання таким інфекціям включають навчання пацієнтів і опікунів, вакцинацію проти інкапсульованих бактерій, грипу, коронавірусної хвороби 2019 (COVID-19) і використання профілактичних антибіотиків.
ВИЗНАЧЕННЯ
Як анатомічна, так і функціональна аспленія та гіпоспленізм сприяють розвитку інфекції
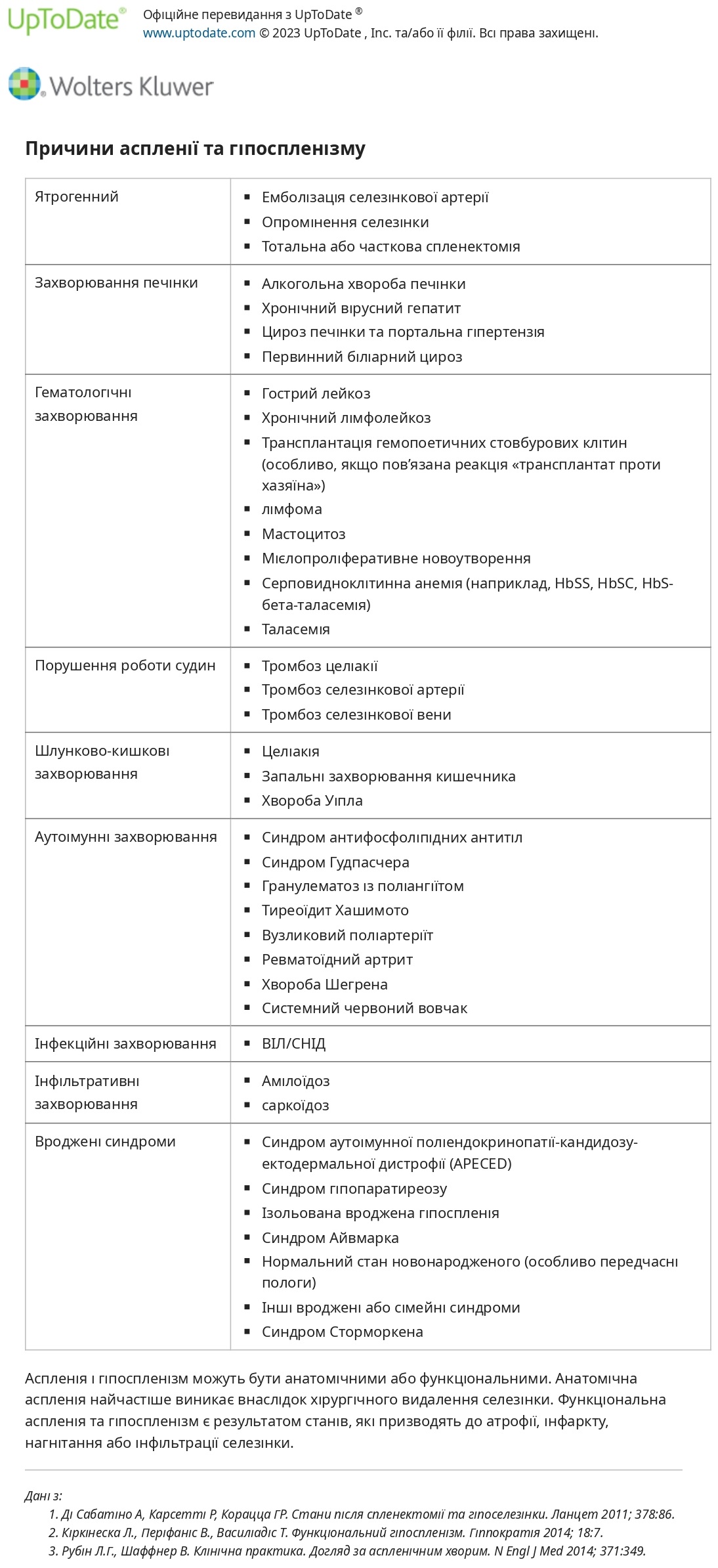
● Аспленія означає повну втрату функції селезінки і може бути анатомічною або функціональною. Анатомічна аспленія найчастіше є наслідком хірургічної спленектомії, що виконується при травмі або терапевтично (наприклад, при гемолітичних анеміях або імунних тромбоцитопеніях). Функціональна аспленія належить до повної втрати функції, спричиненої захворюваннями, і найчастіше зустрічається при серповидно-клітинній анемії. Рідко є вроджена відсутність селезінки.
● Гіпоспленізм означає часткову втрату функції селезінки та найчастіше спричинений захворюваннями, які призводять до атрофії, інфаркту, набухання або інфільтрації селезінки, такими як таласемія, хронічне захворювання печінки, вірус імунодефіциту людини (ВІЛ)/синдром набутого імунодефіциту (СНІД), імунні розлади або злоякісні пухлини.
Гіпоспленізм вважається клінічно значущим (тобто потребує додаткової вакцинації та/або антибіотикопрофілактики) у всіх пацієнтів із серповидно — клітинною анемією, пацієнтів із рецидивуючими інфекціями інкапсульованими мікроорганізмами (наприклад, S. pneumoniae, Haemophilus influenzae типу b або Neisseria meningitidis) у відсутність гуморального дефіциту та/або пацієнтів, які мають тільця Хауелла-Джоллі, що виявляються в мазку периферичної крові, або інші лабораторні докази дисфункції селезінки (наприклад, низька кількість циркулюючих імуноглобулінових [Ig]M В-клітин пам’яті).
НАВЧАННЯ ПАЦІЄНТІВ
Навчання пацієнтів із порушеною функцією селезінки, а також їхніх сімей та/або осіб, які доглядають за ними, щодо підвищення ризику інфікування протягом усього життя та стратегій мінімізації ризику має вирішальне значення для догляду. Пацієнти з більшою обізнаністю про свій стан, як видається, мають нижчий рівень важких і переважних інфекцій порівняно з тими, хто має менші знання.
При консультуванні пацієнтів ми наголошуємо на наступному:
● Підвищений ризик важкої інфекції. Ми повідомляємо пацієнтів з аспленією та гіпоспленією, що вони мають невеликий довічний підвищений ризик важкої або переважної інфекції певними патогенами І ризик інфікування, і пов’язана з цим смертність приблизно вдвічі або втричі вищі, ніж серед населення в цілому. Один аналіз показав, що ризик значного сепсису після спленектомії становить 1,3/1000 років спостереження за пацієнтом.
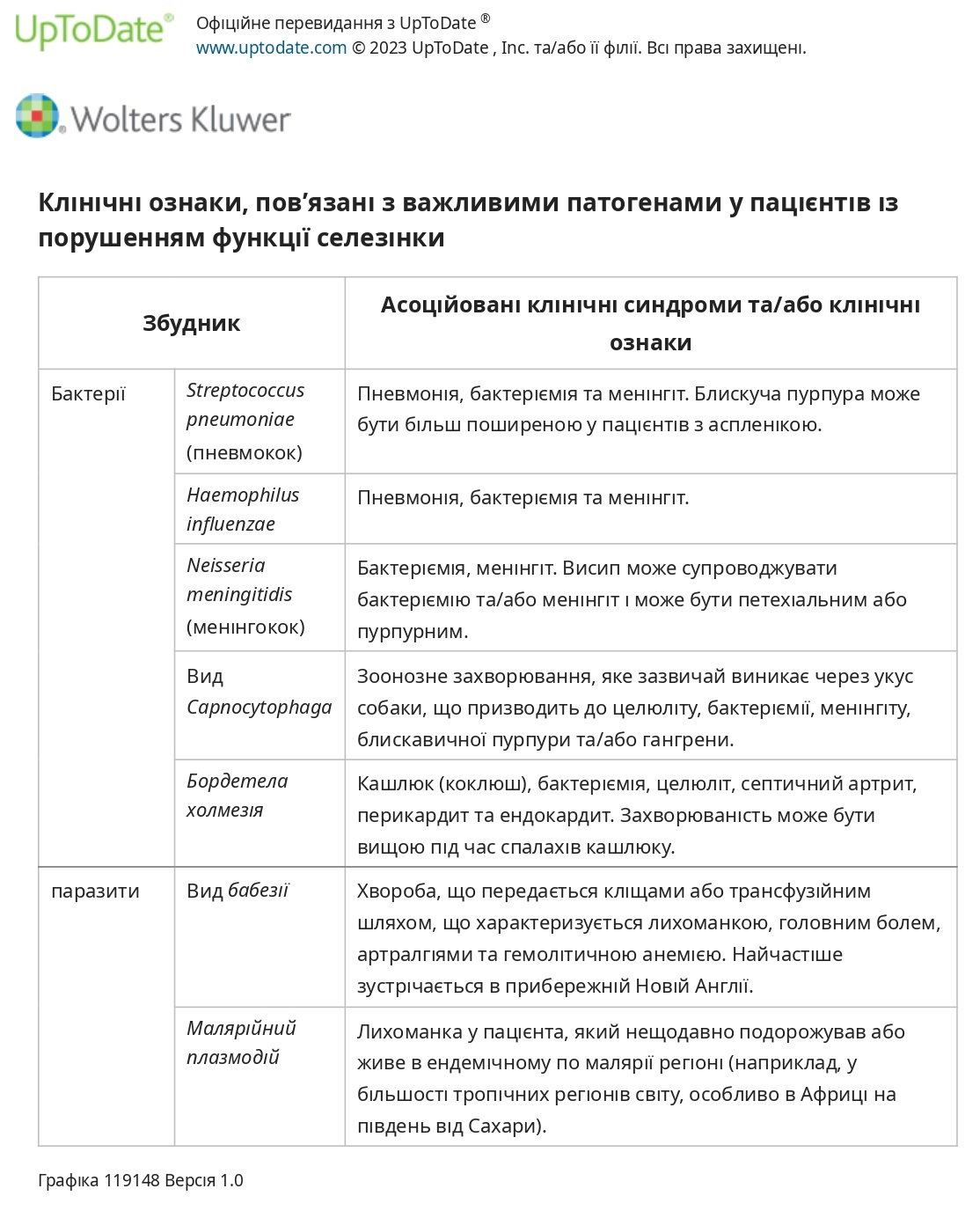
Важливість вакцинації
Ми наголошуємо на важливості отримання всіх щеплень і постійного проходження всіх щеплень, особливо тих, які спрямовані проти патогенів, пов’язаних із підвищеною захворюваністю та смертністю у пацієнтів із порушенням функції селезінки (наприклад, S. pneumoniae, N. meningitidis, тип H. influenzae б, та вірус грипу)
● Використання антибіотикопрофілактики – використання антибіотикопрофілактики, на додаток до вакцинації, додатково знижує ризик інфікування та поганих результатів. Ми обговорюємо ризики та переваги щоденної антибіотикопрофілактики з усіма пацієнтами та загалом віддаємо перевагу її використанню у пацієнтів із аспленією та гіпоспленією, які мають найвищий ризик важкої інфекції (наприклад, діти віком до 5 років, пацієнти з ослабленим імунітетом, пацієнти з тяжкими інфекціями в анамнезі, і пацієнти в перший рік після спленектомії). Ми радимо всім пацієнтам тримати під рукою запас антибіотиків для екстреної допомоги, які будуть використані при розвитку лихоманки чи інших ознак системної інфекції, і негайно звернутися за медичною допомогою у разі розвитку цих симптомів.
● Коли звертатися за медичною допомогою – Оскільки інфекції у пацієнтів із порушенням функції селезінки можуть швидко прогресувати, ми радимо пацієнтам, у яких розвивається гарячка (наприклад, температура ≥101°F/38,3°C) або інші ознаки системної інфекції (наприклад, озноб, озноб, блювання/діарея, головний біль) негайно звернутися до найближчого відділення невідкладної допомоги. Як правило, пацієнтам із симптомами, що вказують на вірусні захворювання верхніх дихальних шляхів (наприклад, ринорея, закладеність носа), у яких немає температури, не потрібно негайно звертатися за допомогою, і їх можна лікувати так само, як і пацієнтів із нормальною функцією селезінки.
Ми також радимо пацієнтам із порушенням функції селезінки негайно звертатися за медичною допомогою у разі будь-якого укусу тварини. Укуси собак, зокрема, можуть передавати Capnocytophaga canimorsus, який може швидко прогресувати та мати летальний результат у пацієнтів із порушенням функції селезінки. Додаткові запобіжні заходи включають уникання укусів кліщів у районах, де є ендемічний бабезіоз, і відвідування медичного працівника перед поїздкою, особливо в регіонах, де є ендемічна малярія для місцевих жителів.
ДІЇ ДО СПЛЕНЕКТОМІЇ
Для пацієнтів, яким проводиться повна або часткова спленектомія, певні заходи можуть допомогти мінімізувати ризик інфікування після операції.
Вибір часу планової спленектомії.
Вибір часу планової спленектомії в першу чергу визначається невідкладністю основного захворювання (наприклад, гемолітична анемія або спадковий сфероцитоз). Якщо спленектомію можна запланувати заздалегідь, надання достатнього часу для отримання важливих щеплень і/або дозрівання імунної системи може допомогти запобігти інфекціям після спленектомії.
Для дітей ми зазвичай відкладаємо спленектомію до 2 років, коли відповідь антитіл на полісахаридний бактеріальний антиген є функціонально більш розвиненою. У минулому спленектомію в дитячому віці часто відкладали до 5 років через високу поширеність інвазивних пневмококових інфекцій у пацієнтів з аспленією. Однак із широким застосуванням пневмококової кон’югованої вакцини поширеність пневмококових інфекцій значно знизилася. Відповідно, серед дітей із серповидно-клітинною анемією та гіпоспленією віком до п’яти років рівень інвазивних пневмококових захворювань знизився більш ніж на 90 відсотків із регулярним використанням пневмококової вакцини. При одночасному застосуванні щоденної антибіотикопрофілактики ризик інфікування ймовірно ще більше знижується. Таким чином, в умовах, де вакцинація проти пневмококів є загальною, виконання планової спленектомії після дворічного віку є доцільним, якщо є клінічні показання.
Для всіх пацієнтів доцільно підготуватися до спленектомії якомога раніше перед процедурою, щоб переконатися, що всі звичайні щеплення були отримані та можна було розпочати додаткову серію вакцин, рекомендовану для пацієнтів із селезінкою. Початок вакцинації за 10–12 тижнів до спленектомії гарантує, що серія первинної пневмококової вакцини, рекомендована для більшості дорослих і дітей із порушенням функції селезінки, може бути завершена до процедури, максимізуючи захист від S. pneumoniae.
Хірургічний підхід — через високу смертність, пов’язану з сепсисом у пацієнтів із селезінкою, слід застосовувати заходи, які дозволяють уникнути спленектомії, коли це можливо. Наприклад, виконання відновлення селезінки замість спленектомії під час дослідницької лапаротомії з приводу внутрішньочеревної травми або після ненавмисного пошкодження селезінки під час внутрішньочеревних процедур зберігає функціональну тканину селезінки та, як вважається, знижує ризик інфекції. Так само емболізація селезінкової артерії може зменшити потребу в спленектомії у пацієнтів із закритою травмою живота.
ВАКЦИНАЦІЇ
Рекомендовані вакцини. Найпоширенішими причинами сепсису та важких інфекцій у пацієнтів із порушенням функції селезінки, яким можна запобігти за допомогою вакцинації, є S. pneumoniae (пневмокок), H. influenzae типу b та N. meningitidis (менінгокок).
Для захисту від цих мікроорганізмів більшості пацієнтів із порушенням функції селезінки необхідно:
● 20 -валентна пневмококова кон’югована вакцина (PCV20) окремо або менш валентні пневмококові кон’юговані вакцини (наприклад, 15-валентна PCV [ PCV15 ], 13-валентна PCV [ PCV13 ]), а потім 23-валентна пневмококова полісахаридна вакцина (PPSV23) ≥ Через 8 тижнів.
● Вакцина проти H. influenzae типу b (Hib).
● Чотиривалентна менінгококова кон’югована вакцина ACWY (MenACWY).
● Серія моновалентної менінгококової вакцини серогрупи B (MenB-4C або MenB-FHbp).
Чотиривалентна менінгококова вакцина потребує ревакцинації (бустерні дози). Специфічні схеми вакцинації залежать від віку пацієнта та історії вакцинації, особливо серед маленьких дітей.
Окрім цих щеплень, пацієнти з порушенням функції селезінки повинні отримувати всі стандартні вакцинації відповідно до віку і вакцинацію проти COVID-19. Сама по собі аспленія не є протипоказанням для будь-яких щеплень, у тому числі живих вакцин. Однак імунодефіцитні стани, такі як гематологічні злоякісні новоутворення та ВІЛ-інфекція, можуть виникати одночасно з аспленією та можуть бути протипоказаннями.
Оскільки грип пов’язаний із підвищеним ризиком зараження S. pneumoniae, ми наголошуємо на важливості щорічної вакцинації проти вірусу сезонного грипу для всіх пацієнтів віком ≥6 місяців із порушенням функції селезінки.
Відповідь антитіл на вакцинацію є достатньо захисною у більшості пацієнтів з аспленією, але може бути нижчою, ніж у здорових людей. Щоб оптимізувати імунну відповідь на вакцинацію, ми вакцинуємо пацієнтів принаймні за 2 тижні, а в ідеалі за 10–12 тижнів до спленектомії, якщо це можливо. Якщо вакцини неможливо ввести принаймні за два тижні до спленектомії, ми вакцинуємо через два тижні після процедури. Людям з нехірургічною аспленією або гіпоспленізмом ми робимо щеплення, як тільки виявлено порушення функції селезінки.
Графіки вакцинації
Дорослі — на додаток до планових щеплень відповідно до віку та вакцинації проти COVID-19, дорослі, які проходять спленектомію або мають функціональну чи анатомічну аспленію чи гіпоспленізм, повинні отримати щеплення проти S. pneumoniae (пневмокока), H. influenzae типу b і N. meningitidis (менінгокок).
Пневмококова вакцинація
Дорослим із порушенням функції селезінки, які раніше не отримували пневмококову вакцину або чия історія вакцинації невідома, ми даємо одну дозу PCV20. Якщо PCV20 недоступний, можна використовувати PCV15. Якщо використовується PCV15, PPSV23 слід вводити через ≥8 тижнів після дози PCV15.
Для тих, хто раніше отримав пневмококову вакцину, підхід до вакцинації залежить від типу введеної вакцини:
Дорослі, які вже отримали вакцину PCV і PPSV23, не потребують подальшої вакцинації.
Дорослі, які отримали лише PCV13, повинні отримати вакцину PPSV23 через ≥8 тижнів після отримання PCV13.
Дорослі, які отримали лише вакцину PPSV23, повинні отримати PCV15 або PCV20 щонайменше через рік після PPSV23.
Вакцинація проти H. influenzae типу b
Одноразова доза вакцини проти Hib рекомендована перед спленектомією або пацієнтам з аспленією чи гіпоспленізмом. Ревакцинація не потрібна для Hib.
Дорослим, які раніше не були щеплені проти Hib (або якщо статус щеплення невідомий), ми даємо одну дозу Hib. Оскільки більшість дорослих мають імунітет до Hib (незалежно від статусу вакцинації), деякі експерти вважають за краще перевіряти титр антитіл до Hib і робити щеплення, лише якщо титри низькі або не виявляються.
Дорослим, які отримали одну або кілька доз Hib з інших причин (наприклад, одночасний імунодефіцитний стан), повторна вакцинація не потрібна.
Менінгококова вакцинація
Для більшості дорослих ми вводимо дві дози вакцини MenACWY з інтервалом ≥8 тижнів
Крім того, ми вакцинуємо дорослих проти менінгокока серогрупи B. Ревакцинація також необхідна для вакцини серогрупи В.
Вакцинація проти сезонного грипу
Ми рекомендуємо щорічно вакцинувати всіх пацієнтів із аспленією та гіпоспленією проти сезонного грипу. Хоча живі ослаблені вакцини можна безпечно вводити пацієнтам із порушенням функції селезінки, перевага віддається інактивованій вакцині проти грипу перед живою формою, оскільки вона однаково ефективна.
Діти
Рекомендації щодо вакцинації для дітей із порушенням функції селезінки залежать від віку пацієнта та історії вакцинації
Діти ≥2 років
Пневмококова вакцинація
Дітям віком ≥2 років, які отримали відповідні за віком пневмококові щеплення (наприклад, отримали повну серію з чотирьох доз PCV до 2 років), ми даємо одну дозу PPSV23.
Ми ревакцинуємо PPSV23 кожні п’ять-сім років після цього.
Для дітей віком від 2 до 5 років, які не завершили серію PCV, ми даємо додаткові одну або дві дози PCV залежно від кількості доз PCV, отриманих раніше. Після отримання відповідної кількості доз ми вакцинуємо PPSV23 через ≥8 тижнів після останньої дози PCV. Ми ревакцинуємо PPSV23 кожні п’ять років після цього.
Дітям віком ≥6 років, які не пройшли серію PCV або ніколи не отримували PCV, ми призначаємо одну дозу PCV, а потім PPSV23 через ≥8 тижнів. Ми ревакцинуємо PPSV23 кожні п’ять-сім років після цього.
Вакцинація проти H. influenzae типу b
Вакцинація протиHib рекомендована перед спленектомією або пацієнтам зі встановленою аспленією чи гіпоспленізмом.
Дітям, які пройшли регулярну рекомендовану первинну вакцинацію проти Hib, додаткова вакцинація не потрібна.
Дітям ≥2 років, які не були щеплені проти Hib або які не пройшли повну серію вакцинації, або якщо статус вакцинації невідомий, ми даємо одну або дві дози Hib залежно від віку дитини та історії попередньої вакцинації проти Hib
Ревакцинація проти Hib не потрібна.
Менінгококова вакцинація
Дітям із порушенням функції селезінки рекомендуються два види менінгококової вакцинації: квадривалентна менінгококова кон’югована вакцина, яка захищає від менінгококових серотипів A, C, W та Y
Дітям ≥2 років, які не були щеплені проти N. meningitidis, ми вводимо чотиривалентну вакцину MenACWY. Ці вакцини вводяться серією з двох доз з інтервалом не менше восьми тижнів.
Дітям віком ≥10 років ми також вводимо одну з вакцин серогрупи B.

Вакцинація проти сезонного грипу
Ми рекомендуємо щорічно вакцинувати всіх дітей віком ≥6 місяців проти сезонного грипу. Хоча живі ослаблені вакцини можна безпечно вводити пацієнтам із порушенням функції селезінки, перевага віддається інактивованій вакцині проти грипу перед живою формою, оскільки вона однаково ефективна та доступна. Дітям старше 9 років потрібна лише одна вакцинація проти грипу, незалежно від їхньої історії вакцинації. Дітям молодшого віку (віком від шести місяців) потрібні дві дози вакцини проти грипу з інтервалом принаймні в чотири тижні, коли вони починають сезонну імунізацію проти грипу, з одноразовими щорічними дозами після цього.
Діти віком до 2 років. Дітям віком до 2 років з аспленічною та гіпоселезінковою хворобами ми вводимо всі вакцини, рекомендовані для їхньої вікової групи, за тією ж схемою, що й дітям із нормальною функцією селезінки. Це включає стандартно рекомендовану чотиридозову серію пневмококової кон’югованої вакцини (PCV13 або PCV15), серію вакцин, націлену на Hib, і сезонну вакцинацію проти грипу (для осіб > 6 місяців).
Крім того, ми вводимо одноразову дозу пневмококової полісахаридної вакцини (PPSV23), коли дитині виповнюється два роки. Як і з усіма іншими, ми ревакцинуємо PPSV23 кожні п’ять-сім років після цього.
Терміни вакцинації
Оптимальний час вакцинації залежить від причини порушення функції селезінки, терміновості спленектомії (у разі її виконання) та необхідності одночасного імуносупресивного лікування.
Пацієнтам з нехірургічною аспленією або гіпоспленізмом (наприклад, порушення функції селезінки внаслідок серповидно-клітинної анемії або іншого захворювання) серію вакцин слід розпочинати, як тільки буде виявлено порушення функції селезінки.
Пацієнтам, які підлягають плановій спленектомії, в ідеалі вакцинацію слід починати приблизно за 10–12 тижнів до операції, щоб рекомендовану серію вакцин можна було завершити принаймні за 14 днів до спленектомії. Якщо всі рекомендовані серії вакцин не можуть бути завершені протягом цього періоду часу, серію вакцин можна відновити через 14 днів після спленектомії для більшості пацієнтів.
Для пацієнтів, які отримуватимуть хімієтерапію або інше імуносупресивне лікування після спленектомії, вакцинацію зазвичай відновлюють приблизно через три місяці після цього лікування.
Пацієнтам, які перенесли екстрену спленектомію, серію вакцин слід розпочинати через 14 днів після спленектомії. Якщо щеплення були зроблені до 14-го дня після операції, доцільно повторити ці щеплення через вісім тижнів після введення початкових доз.
Кілька невеликих досліджень показують, що у пацієнтів, ймовірно, розвивається адекватна відповідь антитіл на вакцинацію, коли вакцини вводяться приблизно через 14 днів після видалення селезінки. У невеликому рандомізованому дослідженні відповіді функціональних антитіл виявились найбільшими у пацієнтів, вакцинованих на 14-й день після спленектомії, порівняно з тими, хто вакцинувався на більш ранніх термінах. Відповіді функціональних антитіл на 14 день були близькі до відповідей здорових контрольних, але не були еквівалентними. У наступному невеликому рандомізованому дослідженні не було виявлено суттєвої різниці у відповідях антитіл на PPSV23 між пацієнтами, вакцинованими на 14-й день після спленектомії, порівняно з тими, вакцинованими на 28-й день.
Вакцинація проти COVID-19
Усі відповідні особи з порушенням функції селезінки, які не мають протипоказань, повинні бути вакциновані проти важкого гострого респіраторного коронавірусу 2, вірусу, який викликає COVID-19. Хоча ефективність вакцинації проти COVID-19 безпосередньо не вивчалася в осіб із порушенням функції селезінки, очікується деяке ослаблення імунної відповіді. Як і інші пацієнти з ослабленим імунітетом, пацієнти з порушенням функції селезінки повинні отримати три дози мРНК-вакцин проти COVID-19.
Як і з іншими вакцинами, ми, як правило, намагаємося робити щеплення, коли у пацієнта найімовірніше виникне захисна імунна відповідь (тобто принаймні за два тижні до або два тижні після спленектомії або коли ефект імуносупресивних препаратів є найнижчим). Однак під час пандемії ми зважуємо ймовірність розвитку захисної імунної відповіді проти ймовірності зараження COVID-19 (наприклад, місцеву поширеність) при визначенні часу.
Ускладнень вакцинації проти COVID-19, які безпосередньо пов’язані зі спленектомією, немає. Однак тяжкість імунної тромбоцитопенії (рідкісні ускладнення вакцинації) може бути вищою серед спленектомованих пацієнтів з анамнезом кількох попередніх терапій.
ПРОФІЛАКТИКА АНТИБІОТИКАМИ
Існує два основні підходи до використання антибіотиків для запобігання важким інфекціям у пацієнтів із аспленією та гіпоспленією:
● Щоденна антибіотикопрофілактика.
● Емпіричне лікування антибіотиками при лихоманці або інших ознаках системної інфекції.
Ці підходи є взаємодоповнюючими. Ми надаємо всім пацієнтам з аспленією та гіпоспленією екстрений запас антибіотиків, які слід використовувати у випадку лихоманки або інших ознак і симптомів інфекції, а також інструкцію про те, щоб звернутися до найближчого медичного закладу, коли такі ознаки або симптоми виникають. Відібраним пацієнтам ми призначаємо щоденну антибіотикопрофілактику на додаток до екстреної допомоги.
Щоденна антибіотикопрофілактика — зазвичай ми визначаємо потребу в щоденній профілактиці та її тривалість індивідуально для кожного пацієнта. Фактори, які ми враховуємо при цьому визначенні, включають вік пацієнта, імунний статус, історію інфекцій інкапсульованими мікроорганізмами, потенційні побічні ефекти антибіотиків, місцеву поширеність мікроорганізмів, стійких до антибіотиків, а також цінності та переваги пацієнта. Загалом ми віддаємо перевагу щоденній антибіотикопрофілактиці пацієнтів з аспленією або порушенням функції селезінки, які мають вищий ризик важких інфекцій через молодий вік, супутні імунодефіцитні стани або історію сепсису, спричиненого інкапсульованими бактеріями. Пеніцилін і амоксицилін є переважними засобами для щоденної профілактики. Альтернативою пеніцилінам є цефалоспорини, фторхінолони та макроліди
- Для більшості дітей з анатомічною або функціональною аспленією/гіпоспленізмом ми забезпечуємо щоденну антибіотикопрофілактику до 5 років і протягом принаймні одного року після спленектомії.
- Дітям і дорослим із супутніми імунодефіцитними станами (наприклад, гематологічні злоякісні пухлини, гіпогаммаглобулінемія, трансплантація солідних органів, прогресуюча хвороба печінки або ВІЛ-інфекція) ми призначаємо антибіотикопрофілактику принаймні до 18 років і часто до тих пір, поки у пацієнта імунодефіцит або протягом життя.
- Дітям або дорослим із сепсисом або іншими важкими інфекціями, спричиненими інкапсульованими мікроорганізмами (наприклад, S. pneumoniae), ми часто забезпечуємо довічну профілактику.
- Для дорослих ми забезпечуємо щоденну антибіотикопрофілактику протягом принаймні одного року після спленектомії.
Для інших пацієнтів з аспленією та гіпоспленією старше 5 років ми не призначаємо щоденну антибіотикопрофілактику за відсутності ознак високого ризику, описаних вище.
Приймаючи рішення розпочати чи припинити щоденну антибіотикопрофілактику, ми зазвичай обговорюємо ризики та переваги антибіотикопрофілактики з кожним пацієнтом та/або їхніми родинами. Хоча переваги запобігання важкій інфекції очевидні, недоліки тривалого застосування антибіотиків не є незначними. До них належать потенційні реакції гіперчутливості або інші несприятливі явища, зміна мікробіому, поява стійких до ліків патогенів, труднощі з дотриманням і неповний захист у регіонах, де висока стійкість до антибіотиків S. pneumoniae. Пацієнти, у яких щоденна профілактика не використовується або її припиняють, повинні отримувати добре налагоджену медичну допомогу, розуміти попереджувальні ознаки, а також лікування можливого аспленічного сепсису, і усвідомлювати, що ризик важкої інфекції залишається довічним.
У метааналізі двох рандомізованих досліджень, у яких оцінювали 457 дітей із серповидно- клітинною анемією та функціональним гіпоспленізмом, щоденна пеніциліно профілактика була пов’язана з триразовим зниженням (3 проти 9 відсотків) частоти пневмококової інфекції порівняно з плацебо (співвідношення шансів [OR ] 0,37, 95% ДІ 0,16-0,86). Більше з цих двох досліджень було проведено у дітей віком до 5 років і було припинено достроково після виникнення 13 випадків пневмококового сепсису (три летальних) у групі плацебо та двох у групі пеніциліну, що відповідає 84-відсотковому зниженню ризику з пеніцилінопрофілактика. Значне зниження частоти пневмококової інфекції та пов’язаної з нею смертності також спостерігалося серед дітей зі спленектомією, які отримували антибіотикопрофілактику, порівняно з тими, хто не отримував профілактики. Оскільки ці дослідження проводилися в епоху, коли використання пневмококової вакцини ще не було широко поширеним, а резистентність S. pneumoniae до пеніциліну була надзвичайно низькою, величина зниження ризику, що спостерігається в цих дослідженнях, може бути не такою значною сьогодні.
Оптимальна тривалість антибіотикопрофілактики не визначена. Наше рішення припинити антибіотикопрофілактику у віці 5 років для більшості дітей було прийнято на основі рандомізованого дослідження, яке показало подібний ризик інвазивного пневмококового захворювання у пацієнтів, які припинили антибіотикопрофілактику у віці 5 років, порівняно з тими, хто продовжував антибіотикопрофілактику після 5 років. В аналізі 400 дітей із серповидно-клітинною анемією та функціональною аспленією, за якими спостерігали в середньому 3,2 року, інвазивне пневмококове захворювання виникло у 2 відсотків пацієнтів, які отримували профілактику після 5 років, порівняно з 4 відсотками пацієнтів, які припинили профілактику у віці 5 років (OR 0,99), 95% ДІ 0,14-7,10). Протягом періоду дослідження не було смертей, і всі учасники отримали пневмококову вакцинацію.
Оскільки дані, що підтверджують передову практику, обмежені, рекомендації органів влади відрізняються. Як приклад, рекомендації Spleen Australia від 2017 р. рекомендують щоденну антибіотикопрофілактику для дітей з аспленією та гіпоспленією до 5 років, принаймні три роки антибіотикопрофілактики після спленектомії як у дорослих, так і у дітей, а також довічну профілактику для пацієнтів з ослабленим імунітетом та/або тих, хто має анамнез перенесеного сепсису. Британські рекомендації 2011 року рекомендують щоденну антибіотикопрофілактику для груп високого ризику, до яких належать діти з аспленієою та гіпоспленією (віком до 16 років), дорослі старше 50 років, пацієнти з ослабленим імунітетом та/або ті, у кого в анамнезі був сепсис. Для пацієнтів без особливостей високого ризику рекомендується приймати індивідуальне рішення. Навпаки, інші експерти припускають, що для пацієнтів старше 5 років, які не мають особливостей високого ризику, достатньо 1-2 років щоденної профілактики після спленектомії через загальне зниження захворюваності на пневмококові захворювання.
Вибір антибіотиків — Пеніцилін і амоксицилін є переважними засобами для щоденної профілактики. Альтернативою пеніцилінам є цефалоспорини, фторхінолони та макроліди.
● Для більшості дорослих і дітей, які потребують щоденної профілактики, ми використовуємо пероральний пеніцилін V або пероральний амоксицилін.
●Для дорослих і дітей з реакціями гіперчутливості на пеніцилін ми використовуємо цефалоспорини, якщо це можливо. Як правило, пацієнти з легкими не-IgE-опосередкованими реакціями на пеніцилін добре переносять цефалоспорини. Оскільки багато пацієнтів з іншими типами реакцій гіперчутливості на пеніцилін також можуть переносити цефалоспорини, ми часто направляємо цих пацієнтів до алерголога, щоб визначити, чи можна безпечно використовувати цефалоспорини перед початком профілактики.
●Для дорослих, які не можуть використовувати цефалоспорини, ми використовуємо фторхінолони або макроліди. Для дітей, які не можуть використовувати цефалоспорини, ми використовуємо макроліди.
У всіх випадках ми беремо до уваги місцеву поширеність антибіотикорезистентності S. pneumoniae, зважуючи переваги та ризики щоденної профілактики та вибираючи антибіотик. У регіонах, де рівень резистентності високий, користь від щоденної профілактики менша. Коли поширеність резистентності до пеніциліну/бета-лактамів перевищує 30 відсотків, ми віддаємо перевагу використанню фторхінолонів для дорослих. Однак це рідкісний сценарій, і фторхінолони пов’язані зі значними побічними ефектами (наприклад, подовженням інтервалу QT, тендинопатіями та можливістю несприятливої взаємодії між лікарськими засобами). Тому ми ретельно та індивідуально зважуємо ризики та вигоди в цій ситуації.
Екстрене введення антибіотиків — ми надаємо всім пацієнтам з аспленією та гіпоспленією екстрений запас антибіотиків, які слід використовувати у разі лихоманки або інших ознак і симптомів системної інфекції (наприклад, озноб, озноб, головний біль, блювота або діарея). Екстрений запас повинен бути під рукою вдома, на роботі та, в ідеалі, завжди з пацієнтом для негайного використання в разі потреби. І пацієнти, і постачальники повинні ретельно стежити за тим, щоб екстрений запас антибіотиків не закінчився.
Для дорослих або дітей, які приймають щоденну антибіотикопрофілактику, ми зазвичай обираємо антибіотик із ширшим спектром дії та/або з іншого класу антибіотиків, ніж антибіотик, який використовується для щоденної профілактики.
Ми радимо пацієнтам прийняти разову дозу призначеного їм екстреного антибіотика (якщо є під рукою) і негайно звернутися до найближчого відділення невідкладної допомоги, якщо з’явиться гарячка чи інші ознаки та симптоми інфекції. Інфекції у пацієнтів із порушенням функції селезінки можуть стати блискавичними та/або смертельними протягом кількох годин після появи симптомів. Швидке лікування, включаючи раннє застосування відповідних антибіотиків, може покращити результати.
ДЖЕРЕЛО: https://www.uptodate.com/
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу

У 2022 році смертність від кору в світі зр ...
Івермектин у дітей вагою <15 кг: нові дані ...

Стрептококові інфекції групи А в педіатрич ...

Пандемія залишила спадок ожиріння серед шк ...

Клінічна настанова: Боротьба з паразитарни ...

Дослідники заявили про «універсальну» вакц ...


.jpg)
