Сибірська виразка: діагностика та лікування
Дата публікації: 22.06.2023
Автори: Скоробагатова Назія АнатоліївнаКандидат медичних наук, хірург 1 категорії, гемостазіолог. Сфера професійних інтересів — невідкладна хірургія, менеджмент системи крові. Медичний редактор accemedin.com
Ключові слова: діагностика, лікування, профілактика, сибірська виразка
Сибірська виразка є одним із найбільших інфекційних захворювань хвороби давнини. П'ята і шоста кари у біблійній книзі Вихід, можливо є спалахами сибірської виразки у великої рогатої худоби та людей, відповідно. Чорне лихо, хвороба, яка прокотилася Європою в 1600-х роках, спричинивши великої кількості смертей людей і тварин, ймовірно була сибірською виразкою. У 1876 році сибірська виразка стала першою хворобою для виконання постулатів Коха (тобто першим захворюванням, для якого твердо встановлена мікробна етіологія), а через 5 років, у 1881 р. - першим бактеріальним захворюванням, проти якого проводилася імунізація. За оцінками, у світі щорічно реєструється від 20 000 до 100 000 випадків сибірської виразки, але в Сполучених Штатах на початку 20-го століття щорічна захворюваність становила лише 127 випадків, а згодом вона знизилася до менше 1 випадку на рік — показник зберігається протягом останніх 20 років (дані станом на 2001 рік). Великі спалахи сибірської виразки в людей в сучасну епоху: понад 6000 (переважно шкірних) випадків, що були зареєстровані в Зімбабве між жовтнем 1979 року і березнем 1980, і 25 шкірних випадків в Парагваї в 1987 році після вбивства інфікованої корови. Сибірська виразка, в умах більшості, являтє собою найбільшу загрозу біологічної війни.
Дуже значний привід пригадати про сибірську виразку в контексті біотероризму відбувся у 2001 році в США. Було задокументовано 12 клінічних випадків сибірської виразки. Серед них два випадки інгаляційної сибірської виразки (один із них смертельний) серед працівників видавничої компанії таблоїдів у Бока-Ратоні, штат Флорида, та чотири інших випадки інгаляційної сибірської виразки (два з них із летальним результатом) серед поштових працівників у Вашингтоні, округ Колумбія, і Трентоні, Нью-Джерсі. Шість інших підтверджених випадків сибірської виразки були шкірної форми, включаючи два випадки шкірної сибірської виразки в Нью-Йорку в осіб, які знаходились в офісах головних телевізійних мереж, і один випадок у поштового працівника в Трентоні. Широке занепокоєння викликали повідомлення про те, що конверти зі спорами сибірської виразки надсилалися до офісів у Вашингтоні, округ Колумбія, та інших місцях.
Бактеріологія
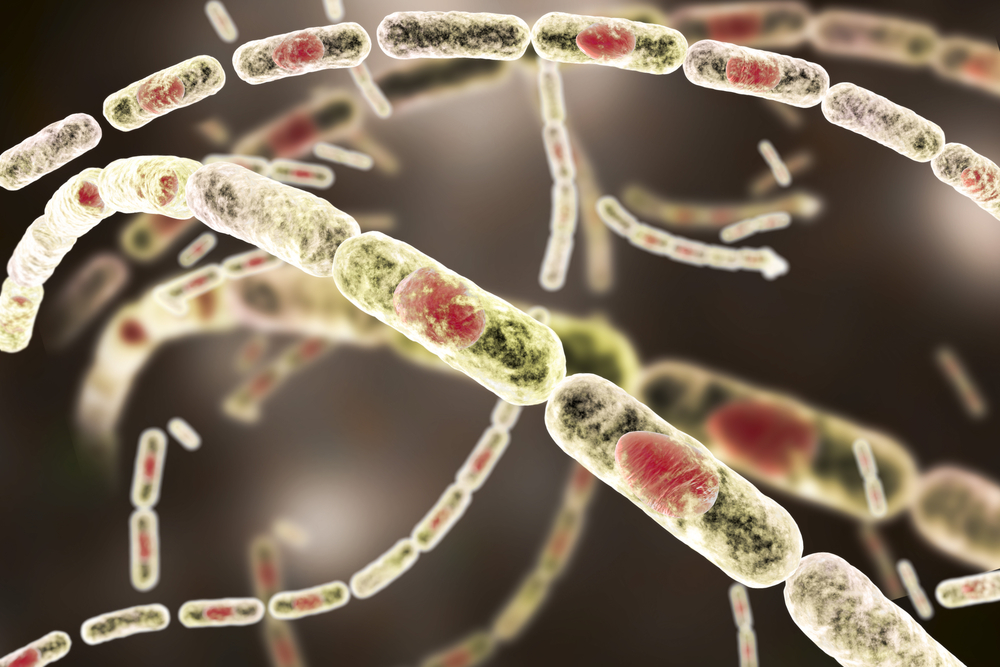
Bacillus anthracis — велика грампозитивна аеробна спороутворююча паличка розміром 1,0–1,5 мкм на 3,0–10,0 мкм. На відміну від інших видів сапрофітної палички (B. subtilis і B. cereus), збудник нерухливий, негемолітичний на агарі з овечою кров’ю, добре росте при температурі 37°C і утворює великі колонії з неправильно звуженими виростами (вигляд «голови Медузи»). In vitro він росте у вигляді довгих ланцюжків, але в організмі інфікованої людини чи тварини він виглядає як один організм або ланцюг із двох або трьох бацил. Утворює мукоїдні колонії та демонструє помітну капсулу при вирощуванні на живильному агарі, що містить 0,7% бікарбонату натрію в присутності 5-20 % вуглекислого газу. Коли поживні речовини вичерпуються, утворюються стійкі спори, які можуть зберігатися в ґрунті десятиліттями. Спори не утворюються в тканинах хазяїна, якщо інфіковані рідини організму не піддаються впливу навколишнього повітря. Спори B. anthracis проростають під впливом багатого поживними речовинами середовища, такого як тканини або кров тварини чи людини.
Незважаючи на те, що B. anthracis є однією з найбільш відомих молекулярно мономорфних бактерій, вдалося розділити всі відомі штами на п’ять категорій (що дає певні підказки щодо їхнього географічного походження) на основі змінної кількості тандемних повторів у варіабельній ділянці гена vrrA.
Патогенез
Основні фактори вірулентності B. anthracis кодуються двома плазмідами — одна бере участь у синтезі поліглутамілової капсули, яка пригнічує фагоцитоз вегетативних форм, а інша містить гени синтезу екзотоксинів, які вона виділяє. Екзотоксини є подвійними, складаються з B (зв’язуючого) білка, необхідного для проникнення в клітину-хазяїна, та A (ферментативно активного) білка. Компонент B відомий як захисний антиген і є спільним для обох токсинів. Компонент A набрякового токсину є фактором набряку, кальмодулін-залежною аденілатциклазою, яка відповідає за помітний набряк у місцях інфекції, пригнічення функції нейтрофілів і перешкоду виробленню моноцитами фактора некрозу пухлини та інтерлейкіну-6. Компонент А другого токсину, летального токсину, є металопротеазою цинку, яка інактивує мітоген-активовану кіназу протеїнкінази, що призводить до інгібування внутрішньоклітинної передачі сигналів. Смертельний токсин стимулює вивільнення макрофагами фактора некрозу пухлини α та інтерлейкіну-1β — механізм, який, очевидно, сприяє раптовій смерті від токсичних ефектів, що відбувається у тварин із високим ступенем бактеріємії (досягаючи 107-108 бацил на мілілітр крові, видимої при фарбуванні за Грамом) і термінально високий рівень летального токсину.
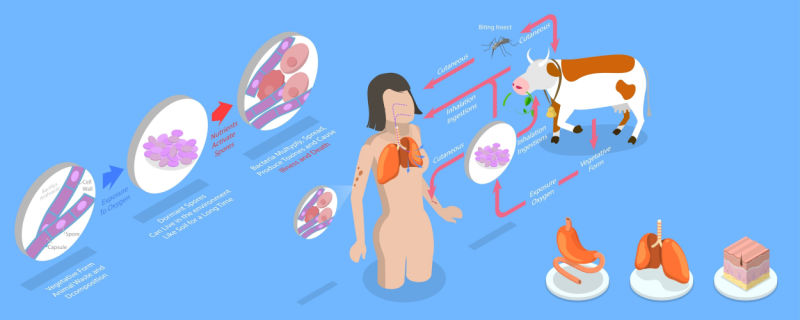
Інфекція починається з проникнення спори через пошкоджену шкіру (шкірна сибірська виразка) або потрапляння через слизову оболонку (шлунково-кишкова сибірська виразка). Після поглинання макрофагами в місці інфікування відбувається проростання до вегетативної форми з наступним позаклітинним розмноженням і утворенням капсули та токсину. У макак-резус вдихання спор (діаметром від 1 до 2 мкм) призводить до їх осідання в альвеолярних просторах, звідки вцілілі спори транспортуються лімфатичними шляхами до лімфатичних вузлів середостіння, де проростання відбувається до 60 днів пізніше. Ці спостереження стали основою для рекомендації про те, що антибіотикопрофілактику інгаляційного впливу слід проводити протягом 60 днів.
Епідеміологія
Спорова форма цього організму може виживати в навколишньому середовищі протягом багатьох десятиліть. Певні умови навколишнього середовища формують зони сибірської виразки — території, де ґрунт щільно контамінований спорами сибірської виразки. Такі умови включають ґрунт, багатий органічними речовинами (pH <6,0) і різкі зміни клімату, такі як рясні опади після тривалої посухи.
Частково через стійкість у ґрунті сибірська виразка є досить важливою ветеринарною хворобою,
особливо домашніх травоїдних. Окрім зараження при випасі в районах з високою контамінацією, травоїдні тварини можуть інфікуватись через укуси деяких мух. Стерв'ятники можуть механічно поширювати мікроорганізм в навколишньому середовищі.
Спори сибірської виразки добре піддаються аерозоляції та набувають стійкості проти погіршень умов навколишнього середовища. Більш того, ці спори, 2-6 мкм в діаметрі, мають ідеальний розмір для ураження слизової нижніх дихальних шляхів людини, підвищуючи ймовірність зараження.
У природних умовах люди заражаються сибіркою (зазвичай шкірною формою) через контакт із зараженими тваринами або зараженими продуктами тваринного походження, такими як шкури, шерсть, волосся та бивні зі слонової кістки. Рідко шлунково-кишкова (або ротоглоткова) сибірська виразка розвивається після вживання погано термічно обробленого інфікованого м’яса. Випадки інгаляційної сибірської виразки (також відомої як хвороба сортувальників вовни) були пов’язані з широкомасштабною обробкою шкір і вовни в закритих фабричних приміщеннях, де можна вдихати аерозольні спори сибірської виразки.
Клінічні особливості
Інгаляційна сибірська виразка
Термін «інгаляційна сибірська виразка» є кращим, ніж сибірська пневмонія, з огляду на патогенетичну послідовність, вираженість геморагічного грудного лімфаденіту та медіастиніту та відсутність типової бронхопневмонії при клінічному або патологоанатомічному дослідженні. Однак у приблизно 25 % смертельних випадків інгаляційної сибірської виразки бувають ознаки вогнищевого, геморагічного, некротичного ураження легенів, яке нагадує вогнищеве ураження Гона при первинному туберкульозі.
Інгаляційна сибірська виразка починається після контакту з інокулятом, з поглинанням спори легеневими макрофагами. Макрофаги переносять спори в трахеобронхіальні або середостінні лімфатичні вузли; тут, B. anthracis знаходить сприятливе середовище для зростання та вегетації. Мікроорганізм починає виробляти антифагоцитарну капсулу і щонайменше три білки, які відіграють роль у вірулентності: набряковий токсин, летальний токсин та захисний антиген. Ці токсини призводять до некрозу лімфатичної тканини, що своєю чергою викликає вивільнення великої кількості B. anthracis. Мікроорганізми потрапляють в кровотік, тому швидко розвивається смертельна бактеріємія.
Класичний клінічний опис інгаляційної сибірської виразки є двофазним захворюванням. На початковій стадії, яка йде після інкубаційного періоду 1-6 днів, вона проявляється як неспецифічна хвороба, що характеризується легкою лихоманкою, нездужанням, міалгією, непродуктивним кашлем і деяким болем у грудях або животі. Протягом 2-3 днів після короткого періоду покращення хвороба переходить у другу фазу. Ця фаза починається раптово і включає лихоманку, гостру задишку, потовиділення та ціаноз. Стридор присутній у деяких пацієнтів через зовнішню обструкцію трахеї збільшеними лімфатичними вузлами, розширенням середостіння та підшкірним набряком грудей і шиї. Приблизно у половини пацієнтів притуплення та ригідність потилиці розвиваються внаслідок ускладнення сибірської виразки менінгітом. Друга стадія хвороби швидко прогресує до шоку з супутньою гіпотермією, і смерті, що настає протягом 24-36 годин; 16 з 18 випадків, зареєстрованих у Сполучених Штатах між 1900 і 1978 роками, були летальними.
Дуже рідко первинне ураження інгаляційної сибірської виразки виникає на слизовій оболонці носа або назальних пазухах. Виражений набряк обличчя та густі желатиноподібні виділення з носа є типовими ознаками такої форми сибірки.
Шкірна сибірська виразка
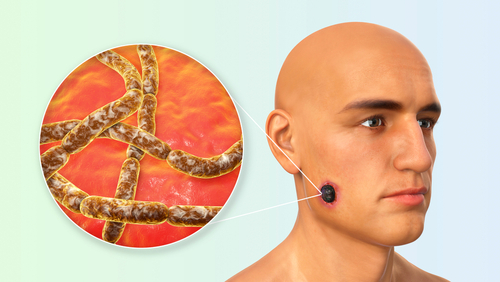
Понад 95% в сибірської виразки, що зустрічається в природі, має шкірну форму. Спора потрапляє на місце порізу або садна, зазвичай на руках, обличчі або шиї. Первинне ураження — безболісна свербляча папула — з’являється через 1-7 днів після введення ендоспори. Протягом 1-2 днів дрібні везикули оточують папулу або розвивається везикула діаметром 1-2 см, заповнена прозорою або серозно-кровною рідиною, що містить поодинокі лейкоцити та численні великі грампозитивні палички. Везикула збільшується, і можуть розвиватися супутникові везикули. Навколо ураження помітний драглистий набряк без ямок. Часто спостерігаються субфебрильна температура і нездужання. Везикула розривається, піддається некрозу і збільшується, утворюючи виразку, покриту характерним чорним струпом. Набряк може стати масивним, особливо, коли ураження знаходяться на обличчі або шиї, і іноді, множинні булли розвиваються разом із помітними токсичними ефектами. Слід уникати розрізу або обробки таких ранніх уражень, оскільки це може збільшити ймовірність бактеріємії. Струп висихає і відпадає через один-два тижні з невеликими кінцевими рубцями. Спочатку спостерігається регіонарна лімфаденопатія. Вторинне інфікування стрептококами або Staphylococcus aureus є рідкісним явищем, але про це можна стверджувати за рецидивом гарячки з лімфангітом, місцевим болем і гнійними виділеннями.
Бактеріємія при шкірній формі сибірки є рідкісним ускладненням. Без лікування антибіотиками смертність може досягати 20%.
Шлунково-кишкова сибірська виразка
Симптоми шлунково-кишкової сибірської виразки з’являються через 2-5 днів після вживання недостатньо прожареного м’яса, що містить спори, і включають нудоту, блювоту, лихоманку та біль у животі. Прояви швидко прогресують до тяжкої кривавої діареї та ознак гострого живота. Первинні кишкові ураження є виразковими і виникають переважно в термінальному відділі клубової або сліпої кишки. Виразка шлунка може супроводжуватися гематемезисом. Геморагічний мезентеріальний лімфаденіт також є ознакою шлунково-кишкової сибірської виразки, і може виникнути виражений асцит. Смертність перевищує 50%.
Відкладення та проростання спор у ротоглотці може викликати орофарингеальну сибірську виразку. Симптоми включають сильний біль у горлі, лихоманку, дисфагію та іноді респіраторний дистрес, який спричинений супутнім вираженим лімфаденітом і масивним набряком. Можна побачити виразки ротової порожнини або глотки, вкриті псевдомембраною.
Сибірковий менінгіт
Сибірсковий менінгіт може виникнути в результаті бактеріємії після інгаляційної сибірської виразки і рідше зустрічається після інших форм сибірської виразки. Спинномозкова рідина в більшості випадків геморагічна, спостерігається поліморфно-ядерний плеоцитоз. Присутні численні великі інкапсульовані грампозитивні бацили. Смертність наближається до 100%, але іноді пацієнти, які отримували антибіотики, виживають.
Діагностика
Диференційна діагностика
Діагноз сибірської виразки встановлюється на основі клінічних даних та історії контакту з продуктами тваринного походження з-за кордону, або на переробному підприємстві, або вдома.
Інші ураження шкіри, які слід враховувати при диференціальній діагностиці шкірної сибірської виразки, включають стафілококовий фурункул або шкірну інфекцію (зазвичай болючу), ектиму (зазвичай без набряку чи системних проявів), гангренозну ектиму (зазвичай у пацієнтів з нейтропенією та бактеріємією, спричиненою синьогнійною паличкою), orf або псевдовіспа (при якому відсутній драглистий набряк і утворюється струп, але немає помітного великого струпа), і укус коричневого павука-відлюдника (спричиняє біль із початковим некрозом).
Яскраві грипоподібні симптоми, які нещодавно виникли у пацієнта з розширеним середостінням, сьогодні можуть свідчити про діагноз сибірської виразки, особливо якщо таких випадків більше одного. Однак туляремія може спричинити подібну гостру лімфаденопатію середостіння.
У разі підозри на сибірську виразку необхідно негайно повідомити місцеві або державні відділи охорони здоров’я, епідеміологів лікарень і місцеву або державну медичну лабораторію. У CDC доступні рекомендації щодо клінічної та лабораторної діагностики, обробки зразків, дезактивації обладнання та постконтактної профілактики.
Лабораторна діагностика
Передбачувана ідентифікація в лікарняній лабораторії базується на прямому забарвленні за Грамом мазку ураження шкіри (везикулярної рідини або струпа), цереброспінальної рідини або крові, що містить інкапсульовані широкі грампозитивні палички. Діагноз верифікується також на основі показників росту, виявлених на культурах овечого кров’яного агару — негемолітичних колоній і великих, нерухомих, неінкапсульованих, грампозитивних спороутворюючих паличок. На агарі МакКонкі зростання не відбувається.
Додаткові критерії для підтвердження присутності B. Anthracis включають сприйнятливість до лізису гамма-фагом або пряме флуоресцентне фарбування антитілами полісахаридного антигену клітинної стінки. Швидкі скринінгові аналізи для використання безпосередньо на клінічних зразках (включно з мазками з носа) і зразках навколишнього середовища є інструментами дослідження для використання державними лабораторіями LRN і CDC; вони включають виявлення нуклеїнової кислоти тантигену (імуноферментний аналіз [ELISA] для захисного антигену та капсули).
Серологічне дослідження є корисним лише ретроспективно і вимагає зразків з гострої фази та фази одужання для порівняння. При шкірній і орофарингеальній сибірській виразці розвиваються антитіла до протективного антигену або до капсули (у 68-92% випадків і 67-94% випадків відповідно). Виконання таких аналізів на зразках сироватки, отриманих від пацієнтів з відомими або підозрюваними випадками сибірської виразки під час гострої фази та фази одужання, було б корисним для перевірки цих серологічних тестів і, можливо, для підтвердження діагнозу у випадках, коли пряме культуральне дослідження не дало потрібної інформації. Серологічні тести контактних осіб, ймовірно, не допоможуть у прийнятті рішень щодо когось із нещодавніх контактів, з огляду на той факт, що зразок сироватки, отриманий під час фази одужання через кілька тижнів, буде необхідним для серологічної діагностики. Проте такі тести можуть мати епідеміологічну цінність для подальшої діагностики можливих субклінічних випадків органами охорони здоров’я.
Постконтактна профілактика
Лікування антимікробними препаратами не є виправданим для безсимптомних осіб, якщо тільки органи охорони здоров’я або правоохоронні органи не встановили, що існує очевидний ризик контакту з речовиною, документально підтвердженою сибірською виразкою. Дійсно, тривале непотрібне використання антибіотиків може бути шкідливим, оскільки воно може сприяти відбору резистентних штамів комменсалів.
Рекомендації щодо постконтактної профілактики
Рекомендується тривалий період профілактики через тривалий латентний період, який може пройти до проростання спор, отриманих через інгаляційний вплив B. anthracis. Через загрозу біотерористичної атаки та оскільки штам B. anthracis може мати резстентнысть до багатьох антибіотиків (пеніцилін, доксициклін, хлорамфенікол, макроліди та рифампіцин), ципрофлоксацин є препаратом вибору для початкової терапії.
Вакцина проти сибірської виразки, що складається з неінфекційного стерильного культурального фільтрату ослабленого штаму B. anthracis , адсорбованого на ад’юванті гідроксиду алюмінію, вводиться військовослужбовцям збройних сил у США з 1998 року. Захисним компонентом є захисний антиген. Вакцину вводять через 0, 2 та 4 тижні та повторно через 6, 12 та 18 місяців. Його ефективність була продемонстрована в дослідженнях, у яких він забезпечував повний захист від аерозольного зараження мавп через 8 тижнів і 88% захист від аналогічного зараження через 100 тижнів. Щорічні ревакцинації необхідні для підтримки імунітету. Жодних серйозних побічних ефектів, пов'язаних із його використанням, не повідомлялося. Проте запаси вакцин надзвичайно обмежені, і на цей час вакцина не рекомендована для використання медичними працівниками чи населенням. Якщо вакцина стане широко доступною, передбачаэться, що її використання через 0, 2 і 4 тижні може скоротити період постконтактної антимікробної терапії до 30-45 днів.
Антимікробна терапія
Пеніцилін був препаратом вибору для лікування сибірської виразки протягом багатьох десятиліть, і лише дуже рідко була виявлена стійкість до пеніциліну у природних ізолятів. In vitro B. anthracis також чутливий до більшості інших широко використовуваних антимікробних препаратів, таких як ципрофлоксацин, офлоксацин, левофлоксацин, тетрацикліни, хлорамфенікол, макроліди, аміноглікозиди, кліндаміцин, іміпенем, рифампін, ванкоміцин, цефазолін та інші цефалоспорини першого покоління. Він стійкий до цефуроксиму, цефалоспоринів розширеного спектра дії, таких як цефотаксим і цефтазидим, азтреонаму, триметоприму та сульфаметоксазолу.
Клінічо виражена інгаляційна сибірська виразка
Рекомендована початкова терапія для дорослих із клінічно вираженою інгаляційною сибірською виразкою становить 400 мг ципрофлоксацину внутрішньовенно кожні 12 годин. Можна розглянути можливість використання подвійної початкової терапії (ципрофлоксацин плюс пеніцилін), з огляду на частий і швидкий розвиток ускладнюючого менінгіту та клінічний досвід проникнення цереброспінальної рідини при внутрішньовенному введенні високих доз пеніциліну.
Шкірна сибірська виразка
Для легких випадків шкірної сибірської виразки у дорослих рекомендується пероральне лікування ципрофлоксацином (500 мг кожні 12 годин). Якщо штам є сприйнятливим, пероральний доксициклін (100 мг кожні 12 годин) або амоксицилін (500 мг кожні 8 годин) може розглядатись як альтернатива. Лікування повинно тривати протягом 60 днів у контексті біотероризму, на відміну від 7-10 днів у випадку природного захворювання. Важка шкірна сибірська виразка лікується тими ж препаратами та дозуваннями, що й інгаляційна сибірська виразка.
Лікарняний інфекційний контроль і дезінфекція
Оскільки немає даних про передачу від людини до людини навіть у випадку пацієнтів з інгаляційною сибіркою, пацієнтів із сибіркою можна госпіталізувати в стандартну лікарняну палату зі стандартними запобіжними заходами. Необхідно вживати запобіжних заходів при контакті з пацієнтами, у яких є дренажні ураження шкіри. Біологічні рідини з вогнищ ураження, слід вважати небезпечними відходами і їх слід спалювати або автоклавувати.
Для дезактивації забруднених територій слід використовувати спороцидні розчини, дозволені для використання в лікарнях. Можна використовувати комерційно доступний відбілювач або 0,5% розчин гіпохлориту (розведення побутового відбілювача 1:10), але він може викликати корозію деяких поверхонь.
Заключення
З огляду на відносно короткий інкубаційний період і швидке прогресування захворювання, ідентифікація пацієнтів та застосування адекватних лікувально-профілактичних заходів стратегії можуть являти собою виклик, що потребує підвищеної обізнаності та всебічної готовності для працівників сфери охорони здоров’я.
Література:
- Cieslak TJ, Eitzen EM Jr. Clinical and epidemiologic principles of anthrax. Emerg Infect Dis. 1999 Jul-Aug;5(4):552-5. doi: 10.3201/eid0504.990418. PMID: 10458964; PMCID: PMC2627745.
- Swartz MN. Recognition and management of anthrax--an update. N Engl J Med. 2001 Nov 29;345(22):1621-6. doi: 10.1056/NEJMra012892. Epub 2001 Nov 6. Erratum in: N Engl J Med 2002 Feb 21;346(8):634. PMID: 11704686.
- Bossi, P., Garin, D., Guihot, A. et al. Biological weapons. Cell. Mol. Life Sci. 63, 2196–2212 (2006). https://doi.org/10.1007/s00018-006-6308-z
- https://www.cdc.gov/anthrax/
- Popescu R, Pistol A, Miltaru L, Caplan D, Cucuiu R, Popovici F. Two cases of infection with Bacillus anthracis, Romania, October 2011. Euro Surveill. 2011 Nov 10;16(45):20008. PMID: 22114977.
- Chraibi H, Haouach K, Azouzi AI, Gaamouche K, Kaidi A, Khalidi TE, Alifadl A, Bjani L, Mountasser A. Maladie du charbon cutanée: sept cas [Cutaneous anthrax: seven cases]. Ann Dermatol Venereol. 2009 Jan;136(1):9-14. French. doi: 10.1016/j.annder.2008.10.021. Epub 2008 Dec 9. PMID: 19171223.
- Greenfield RA, Drevets DA, Machado LJ, Voskuhl GW, Cornea P, Bronze MS. Bacterial pathogens as biological weapons and agents of bioterrorism. Am J Med Sci. 2002 Jun;323(6):299-315. doi: 10.1097/00000441-200206000-00003. PMID: 12074485.