Майбутнє лікування муковісцидозу — глобальна перспектива
Дата публікації: 21.11.2024
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: муковісцидоз, статті Аксемедін, муковісцидоз це, муковісцидоз у дітей, муковісцидоз симптоми, чи можна вилікувати муковісцидоз, муковісцидоз лікування, муковісцидоз тип мутації, скринінг на муковісцидоз
Дорогі друзі!
Сьогодні, в Європейський день поширення інформації про муковісцидоз, ми хочемо привернути увагу до цього рідкісного, але важливого захворювання. Цей день, заснований Європейським товариством муковісцидозу (EFCS) у 2006 році, має на меті не лише підвищення обізнаності, а й створення платформи для об’єднання пацієнтів, лікарів, науковців та терапевтів.
Муковісцидоз (МВ) — це виклик, з яким стикаються тисячі людей по всьому світу. Завдяки сучасним дослідженням та інноваційним підходам, як-от використання генних ножиць CRISPR, можливості терапії стрімко розширюються. Ми бачимо значне покращення якості та тривалості життя пацієнтів, але боротьба триває, адже муковісцидоз залишається невиліковним.
Ми висловлюємо подяку всім, хто щодня присвячує свої зусилля пацієнтам з МВ: лікарям, дослідникам, сім’ям, а також самим хворим за їхню сміливість і незламність.
Нехай цей день стане ще одним кроком до розуміння, підтримки та натхнення для тих, хто працює над майбутнім без муковісцидозу!
З найкращими побажаннями,
Команда платформи "Аксемедін"
За останні шістдесят років у лікуванні муковісцидозу (МВ) досягнуто значного прогресу, перетворивши колись смертельне захворювання немовлят на стан, що дозволяє значно покращити тривалість і якість життя. Однак МВ все ще залишається серйозним викликом, зокрема для пацієнтів, їхніх родин і систем охорони здоров’я.
Епідеміологічні дослідження останніх десятиліть підтвердили, що захворювання поширене серед людей не лише європейського походження. Це змінило підходи до лікування, включаючи впровадження генетичного тестування та розробку терапій, які усувають основний дефект CFTR-білка. Муковісцидоз (МВ), описаний у 1938 році, став прикладом медичного прогресу, що перетворив смертельне захворювання дитинства на стан із середньою тривалістю життя понад 50 років. Цього вдалося досягти завдяки значним відкриттям та інноваціям у діагностиці та лікуванні.

Ключові досягнення в розумінні захворювання
Потовий тест: Виявлення підвищеного рівня солі в поті пацієнтів з МВ у 1950-х роках заклало основу для діагностики за допомогою стимульованого тесту на піт.
Генетичні відкриття: Відкриття гена CFTR у 1989 році допомогло зрозуміти механізми захворювання. Білок CFTR регулює транспорт іонів хлору, що є ключовим для функціонування епітеліальних клітин у різних тканинах.
Глобальні перспективи розвитку лікування
1. Зміна епідеміології муковісцидозу:
- Ранній скринінг новонароджених дозволяє швидко діагностувати захворювання.
- Удосконалена молекулярна діагностика розширила знання про МВ у популяціях із некласичними проявами захворювання.
- Дослідження функції CFTR дозволяє краще зрозуміти спектр проявів захворювання.
2. Клінічна допомога:
- Діти з МВ мають кращі результати здоров’я завдяки мультидисциплінарному підходу.
- Потреба у вдосконаленні моніторингу для раннього виявлення ускладнень і нових інфекцій є ключовою.
- Моделі догляду повинні зосереджуватися на підтримці якості життя, затримуючи необхідність трансплантації легенів.
Перегляньте записи дводенного майстер-класу BreatheEasy Forum: Otolaryngology, Allergology, Pulmonology!
3. Виклики країн із низьким і середнім рівнем доходу (LMICs):
- Генетичні та клінічні дані в таких країнах потребують глибшого аналізу.
- Партнерства між урядами, фармацевтичною індустрією та НУО сприяють доступності лікування.
- Розробка клінічних реєстрів допоможе стандартизувати дані для досліджень та покращення догляду.
4. Інноваційні терапії:
Модулятори CFTR: Прогресивні методи лікування, спрямовані на молекулярний дефект, значно покращили функцію легень і якість життя пацієнтів. Нові модулятори можуть бути ефективними для пацієнтів, для яких попередні терапії не підходили, особливо якщо лікування розпочато на ранніх стадіях.
Проблема: висока вартість терапії залишається бар’єром для багатьох країн.
5. Залучення пацієнтів:
- Збільшення тривалості життя ускладнює процес догляду та створює психоемоційне навантаження на пацієнтів та їхні родини.
- Технології можуть підтримати самоконтроль і співпрацю між пацієнтами та медичними командами.
- Активна участь пацієнтів у прийнятті рішень щодо лікування та пріоритетів досліджень є критично важливою.
Генетичні аспекти та варіанти гена CFTR
- Відомо понад 2000 варіантів гена CFTR. Їх вплив на функціональність білка значною мірою варіюється:
- Класи I-III: Тяжкі мутації, пов'язані з мінімальною або відсутньою функцією білка.
- Класи IV-V: Мутації із залишковою функцією, що супроводжуються менш тяжкими клінічними проявами.
- Дефекти CFTR викликають мультисистемні прояви, які залежать не лише від генетичного типу, але й від факторів середовища та модифікаторних генів.

Клінічні прояви
Фенотипові особливості включають:
- Респіраторні: Бронхоектази, хронічні інфекції (часто мультирезистентні), дихальна недостатність.
- Шлунково-кишкові: Меконіальний ілеус, гастроезофагеальний рефлюкс, екзокринна недостатність підшлункової залози, ризик розвитку раку.
- Метаболічні: Діабет, остеопороз, камені сечоводу.
- Чоловіче безпліддя: Часто пов’язане з відсутністю сім’явивідних проток.
Приклади повсякденного та невідкладного лікування дорослих із муковісцидозом із хронічною інфекцією Pseudomonas aeruginosa
Щоденне лікування
Сприяння очищенню секрету дихальних шляхів
- Методи очищення дихальних шляхів: фізіотерапія, маска позитивного тиску на видиху, коливальні пристрої — двічі на день.
- Фізична активність: збільшення рівня активності.
- Небулізована дорназа альфа: один раз на день.
- Розпилення гіпертонічного розчину/інгаляції маніту: двічі на день.
Профілактика гострих загострень
- Антибіотики: інгаляційні або небулізовані (тобраміцин, колістину сульфат, азтреонам лізин) — два-три рази на день залежно від препарату.
- Азитроміцин: тричі на тиждень.
- Щеплення: проти грипу щорічно, а також інших інфекцій дихальної системи.
Перегляньте записи дводенного майстер-класу в галузі сімейної медицини Ukrainian Family Medicine Forum 2024!
Інші ускладнення
- Синусит/назальний поліпоз: інтраназальні стероїди, неседативні антигістаміни.
- Кровохаркання: емболізація бронхіальної артерії.
- Пневмоторакс: зондування грудної клітини або операція.
- Алергічний бронхолегеневий аспергільоз: системні стероїди, протигрибкові препарати (азоли), анти-IgE (омалізумаб).
- Синдром дистальної кишкової непрохідності: проносні засоби або клізми.
Підтримка харчування
- Дієта: високий вміст жирів і калорій.
- Панкреатичні ферменти: прийом під час кожного вживання їжі.
- Вітаміни: жиророзчинні (A, D, E, K) — один раз на день.
Корекція основного дефекту CFTR (при наявності відповідної мутації)
- Препарати:
- Івакафтор — двічі на день (для мутації p.Gly551Asp).
- Люмакафтор–івакафтор або Тезакафтор–івакафтор — двічі на день (для мутації p.Phe508del).
Лікування дихальної недостатності
- Киснева терапія.
- Неінвазивна вентиляція.
- Легенева реабілітація.
Лікування супутніх захворювань
- Діабет: інсулін або репаглінід.
- Остеопенія/остеопороз: добавки кальцію, вітамін D, бісфосфонати.
- Тривога та депресія: когнітивно-поведінкова терапія, антидепресанти (наприклад, СІЗЗС).
Перегляньте запис:
Виклики майбутнього:
- Доступність терапій: Висока вартість інноваційних ліків створює нерівності у доступі до лікування між розвиненими країнами та країнами із середнім і низьким рівнем доходів.
- Ускладнення захворювання: Зі збільшенням віку пацієнтів зростає частота ускладнень, що потребує більш кваліфікованих спеціалістів і нових технологій у догляді.
- Розширення доступу до лікування: У країнах із недостатнім ресурсним забезпеченням необхідно інтегрувати нові моделі мультидисциплінарної допомоги.
- Нові методи лікування: Незважаючи на успіхи модуляторів CFTR, подальші дослідження муколітичних, протизапальних і протиінфекційних препаратів залишаються критично важливими.
Плани на майбутнє:
- Створення глобальної системи лікування МВ.
- Розширення можливостей терапії, особливо для країн із обмеженими ресурсами.
- Активне залучення пацієнтів до розробки нових методів лікування.
Спільні зусилля всіх учасників процесу — від пацієнтів і лікарів до політиків і спонсорів — забезпечать можливість надання високоякісної медичної допомоги пацієнтам з МВ у будь-якому куточку світу.
ДЖЕРЕЛО: The Lancet
На платформі Accemedin багато цікавих заходів! Аби не пропустити їх, підписуйтесь на наші сторінки! Facebook. Telegram. Viber. Instagram.
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу
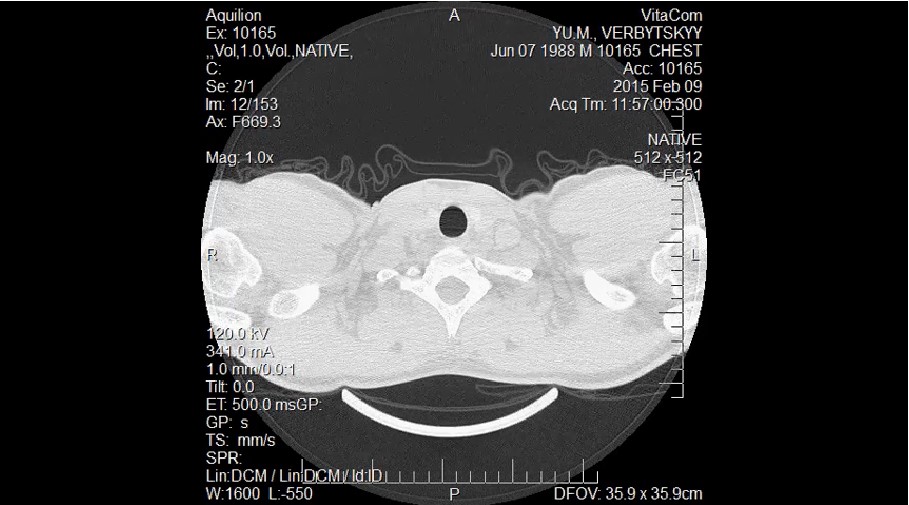
Результати комп’ютерної томографії у паціє ...
Нове дослідження: міокардит частіше зустрі ...
З 1 січня оновлюється Календар профілактич ...

Гендерно-специфічні соціальні фактори можу ...

Десять порад щодо лікування пероральними а ...

Уряд ухвалив рішення про створення Націо ...



.jpg)