Нова вакцина може допомогти запобігти рецидиву раку підшлункової залози
Дата публікації: 22.08.2025
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: імунопрофілактика, вакцина, колоректальний рак, Т-клітини, імунна відповідь, рак підшлункової залози, імунотерапія, KRAS, клінічні випробування, персоналізована медицина, рецидив раку, молекулярна онкологія, мРНК-технології, онкологічна імунологія, мутації KRAS, пептидні вакцини, залишкова хвороба, резектабельний рак
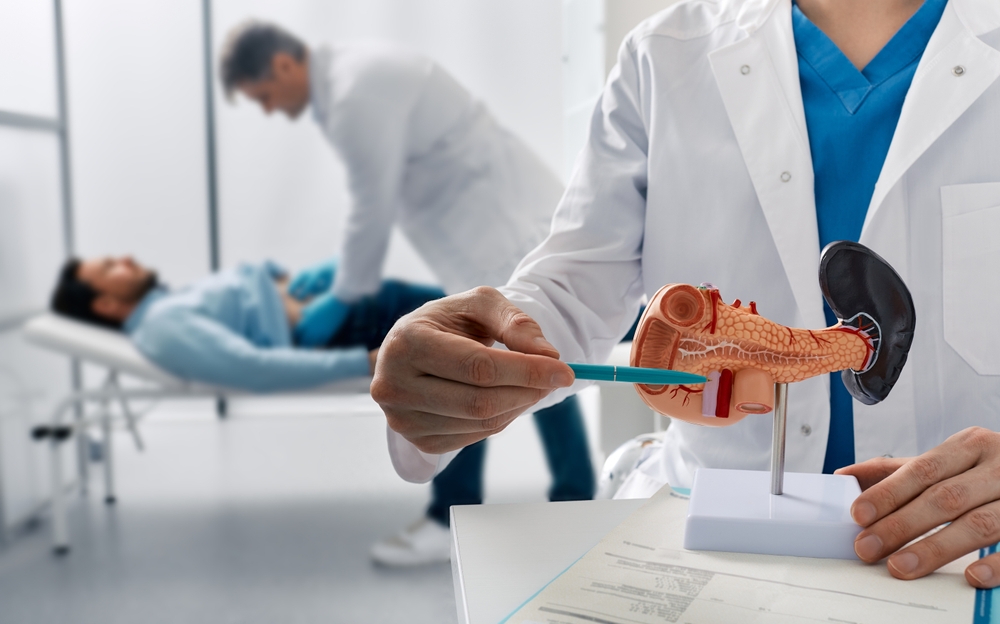
Рак підшлункової залози є одним із найбільш агресивних та смертельних видів онкопатології. За даними Американського онкологічного товариства, п’ятирічна виживаність становить лише близько 13%. Висока частота рецидивів після лікування робить пошук ефективних методів профілактики особливо актуальним.
Мішень KRAS
Мутації гена (англ. KRAS proto-oncogene, GTPase) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 12-ї хромосоми, спостерігаються приблизно у 25% усіх випадків раку та є ключовою ознакою:
- до 90% випадків раку підшлункової залози,
- близько 40% випадків колоректального раку.
Раніше ці мутації вважалися «недосяжними» для терапевтичного впливу, але сучасні технології дозволили розробити нові методи.
Експериментальна вакцина ELI-002 2P
- Використовує синтетичні пептиди для навчання імунної системи розпізнавати та знищувати клітини з мутаціями KRAS.
- Має унікальну структуру з «хвостом», що дозволяє пептидам залишатися у лімфатичних вузлах і стимулювати імунні клітини — перевага над попередніми пептидними вакцинами.
- Виготовляється як готова до застосування, тому не потребує індивідуального секвенування пухлини, на відміну від персоналізованих вакцин.
Перегляньте запис:
Дизайн дослідження (фаза 1, Nature Medicine, серпень 2025)
- Учасники: 20 пацієнтів з раком підшлункової залози та 5 з колоректальним раком.
- Усі мали мутації KRAS та вже перенесли операцію і хімієтерапію.
- Аналізи крові показали наявність залишкових мікроскопічних пухлинних клітин.
- Протягом 6 місяців пацієнти отримали до 6 доз вакцини; 13 із них також отримали ревакцинацію.
Основні результати
- 85% (21 із 25) учасників продемонстрували імунну відповідь проти мутацій KRAS.
- Дві третини з них мали настільки потужну відповідь, що вона могла усунути залишкові пухлинні клітини.
- Майже 70% пацієнтів виробили імунітет і до інших пухлинних антигенів, не включених у вакцину.
- Декілька «суперреспондентів» показали надзвичайно потужну імунну реакцію та найкращі клінічні результати.
У групі пацієнтів з раком підшлункової залози середня тривалість виживаності без рецидиву становила 29 місяців, із понад 15 місяцями без прогресування після вакцинації. Це значно перевищує типові показники для резектабельного раку підшлункової залози.
Вакцини проти раку створювати складно, оскільки пухлинні клітини мають багато спільних білків зі здоровими клітинами. Проте прогрес у секвенуванні генів і використанні мРНК-технологій робить такі підходи перспективними.
Стефані Дуган (Dana-Farber Cancer Institute, Бостон), яка не брала участі у дослідженні, зазначила, що унікальна будова пептидів забезпечує краще накопичення у лімфатичних вузлах та активацію Т-клітин, а кореляція між імунною відповіддю та виживаністю підтверджує ефективність вакцини.
Для підтвердження ефективності потрібні додаткові дані. Наразі триває фаза 2 клінічних випробувань, де ELI-002 2P порівнюється зі стандартним лікуванням.
Експериментальна вакцина, спрямована на мутації KRAS, продемонструвала здатність викликати потужну імунну відповідь та покращувати виживаність пацієнтів із раком підшлункової залози. Якщо результати підтвердяться у наступних фазах випробувань, це може стати проривом у лікуванні одного з найбільш смертоносних видів раку.
ДЖЕРЕЛО: healthday
На платформі Accemedin багато цікавого! Аби не пропустити — підписуйтесь на наші сторінки! Facebook. Telegram. Viber. Instagram.
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу

Нове дослідження підкреслює шкоду від спож ...

Проблема ожирения в общеврачебной практике

Експериментальна сполука на основі гідразо ...
Інші стани, не пов’язані з ГЕРХ

Початок сезону посиленого епіднагляду за х ...

Кишкова бактерія відновлює баланс жовчн ...