Функціональний абдомінальний біль у дітей та підлітків: лікування в первинній медичній допомозі
Дата публікації: 09.10.2023
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: лікування, біль, клінічна настанова, дитина, функціональне порушення травлення, функціональний абдомінальний біль, порушення травлення
ВСТУП
Функціональні абдомінальні болі (FAPD), які також називаються функціональними шлунково-кишковими розладами з переважанням болю, є найпоширенішою причиною хронічного абдомінального болю у дітей і підлітків. FAPD включає взаємодію регуляторних факторів у кишковій та центральній нервовій системах. FAPDs можуть бути пов’язані з вісцеральною гіпералгезією, зниженим порогом для болю, аномальним болем, що посилається після розтягнення прямої кишки, або порушенням реакції розслаблення шлунка на прийом їжі.
Запрошуємо 16 жовтня о 17:00, в День здорового харчування, відвідати сертифікований семінар «Функціональні розлади травлення – топ звернень до лікаря первинної ланки. Алгоритм дії» від провідного фахівця Кожевіна Романа Володимировича. Реєструйтесь!
ТЕРМІНОЛОГІЯ
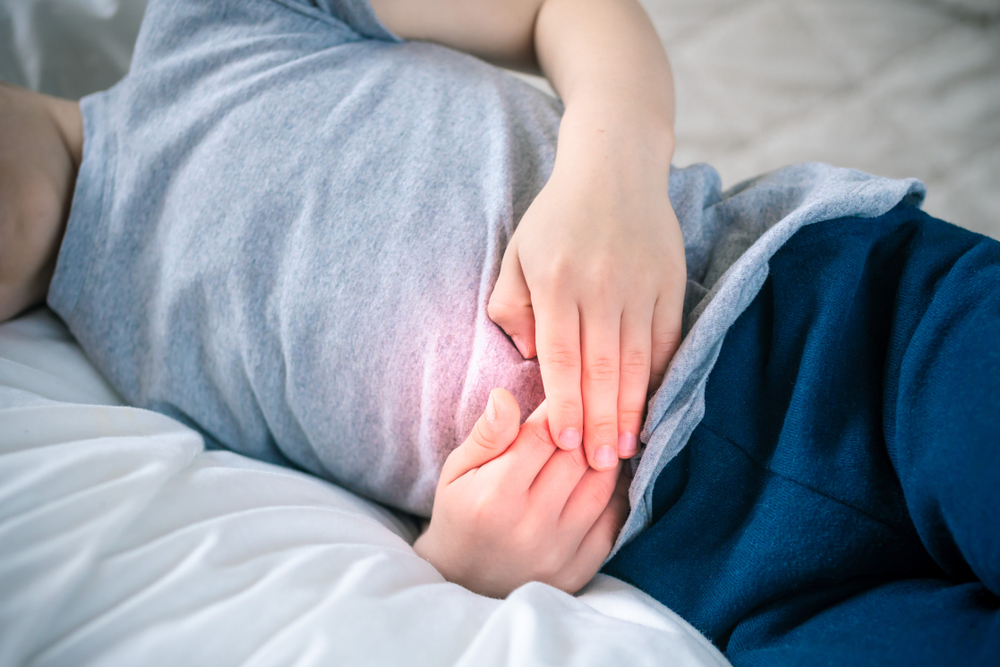
Функціональний абдомінальний біль (FAP) може бути діагностований у дітей, які мають усі з перерахованих нижче:
● Хронічний (≥2 місяців) біль у животі
● Немає сигналів тривоги
● Нормальний фізикальний огляд
● Зразок калу негативний на приховану кров
Декілька функціональних шлунково-кишкових розладів у дитинстві, у яких переважає біль, мають впізнавані моделі симптомів і включають функціональну диспепсію, синдром подразненого кишечника (СПК), абдомінальну мігрень та ФАП-неуточнене (FAP-NOS). Терміни, які використовуються як синоніми з FAP-NOS (часто називають FAP), включають «неорганічний біль у животі», «психогенний біль у животі» та «рецидивуючий біль у животі». Хоча Американська академія педіатрії та Північноамериканське товариство дитячої гастроентерології, гепатології та харчування в клінічному звіті про хронічний абдомінальний біль рекомендує не використовувати термін «рецидивуючий абдомінальний біль» як синонім функціонального, психологічного або пов’язаного зі стресом абдомінального болю, це використання зберігається.
УПРАВЛІНСЬКИЙ ПІДХІД
Метою лікування функціональних абдомінальних больових розладів (FAPD) у дітей і підлітків є повернення до нормальної функції (тобто реабілітація), а не повне усунення болю. Більшість випадків можна лікувати в установах первинної медичної допомоги. Направлення може бути необхідним для дітей і підлітків, які не покращилися після втручання первинної медичної допомоги.
Лікування FAPD є складним, оскільки підтипи гетерогенні, а патофізіологія не повністю вивчена. Люди з FAPDs можуть мати схожі симптоми (наприклад, біль у животі, нудота, зміни в випорожненні), але різні основні причини. Таким чином, лікування є індивідуальним відповідно до поведінки дитини та сім’ї, тригерів і симптомів.
«Відповідь» на будь-яке втручання може відображати природну історію поліпшення з часом або відповідь на плацебо, оскільки FAPD з часом зникає у більшості дітей.
У метааналізі 17 плацебо-контрольованих рандомізованих досліджень (фармакологічних або немедикаментозних) у дітей віком від 4 до 18 років із функціональним шлунково-кишковим розладом, пов’язаним з болем у животі, об’єднаний рівень відповіді на плацебо для покращення (як визначено авторами дослідження) становив 41 відсоток (95% ДІ 34-49 відсотків), а загальна частота відповіді на плацебо для відсутності болю становила 17 відсотків (95% ДІ 8-32 відсотки). Хоча дослідження не виявило жодних факторів, які можна було б використовувати в клінічній практиці для оптимізації відповіді на плацебо, високий рівень відповіді на плацебо може бути цінним інструментом для
ЗАГАЛЬНІ СТРАТЕГІЇ МЕНЕДЖМЕНТУ
Підхід до функціональних абдомінальних больових розладів (FAPD) у дітей і підлітків зазвичай передбачає різні комбінації: терапевтичних стосунків, модифікації поведінки, стратегій для покращення толерантності до болю та подолання, уникнення тригерів і симптоматичне лікування. Пацієнтам, у яких біль не вщухає та продовжує заважати функціонуванню, може бути виправданим направлення на неінвазивні втручання, такі як гіпнотерапія та нейромодуляція вушної раковини. Хоча необхідні додаткові дослідження, докази добре спланованих одноцентрових досліджень підтверджують ефективність цих втручань.
Терапевтичні стосунки. Терапевтичні стосунки клініцист-пацієнт/родина є важливим компонентом лікування FAPDs. Пацієнт і сім’я повинні вірити, що їхні скарги та занепокоєння сприймаються серйозно. Їхнє занепокоєння щодо конкретних органічних захворювань має бути розглянуто (зазвичай шляхом перегляду проявів цього захворювання, які відсутні у пацієнта), перш ніж можна буде продовжити лікування FAPD. Пояснення біопсихосоціальної моделі функціонального захворювання може бути корисним, оскільки воно розглядає хворобу як позитивний діагноз, а не як діагноз виключення (з притаманним очікуванням розгорнутої оцінки). Здатність сім’ї прийняти таку біопсихосоціальну модель болю може бути важливим фактором у одужанні дитини.
Деякі центри розробили мультидисциплінарну модель догляду за пацієнтами з FAPD, яка зазвичай включає дитячого гастроентеролога, фахівця з болю та психолога. Мультидисциплінарна команда підсилює біопсихосоціальні аспекти FAPD і демонструє, що занепокоєння пацієнта та родини сприймаються серйозно. У обсерваційних дослідженнях міждисциплінарна допомога була пов’язана зі зменшенням болю, підвищенням функції та зменшенням використання медичних послуг у дітей із FAPD.
Пацієнта та сім’ю може заспокоїти лікар, який визнає, що біль реальний і вплинув на важливі дії в житті пацієнта. Пацієнт і сім'я повинні бути впевнені, що клініцист розпочне план лікування та продовжуватиме регулярне спостереження за пацієнтом. Періодичне спостереження підтверджує постійну підтримку клініциста та інтерес до пацієнта та його родини.
Терапевтичний альянс можна зміцнити, зосередившись на спільній меті повернення до нормального функціонування як пацієнта, так і сім’ї. Біль може бути центром життя сім’ї, створюючи стрес для інших членів. Лікар-педіатр може усунути ці наслідки, призначивши повернення до структурованої повсякденної діяльності, включаючи відвідування школи (реабілітаційний підхід).
Навчання пацієнтів — FAPD найкраще лікувати в контексті біопсихосоціальної моделі догляду. У невеликому обсерваційному дослідженні прийняття опікуном біопсихосоціальної моделі хвороби було пов’язане зі зникненням болю.
Перед початком терапії педіатр повинен пояснити очікування опікунів і пацієнта. Деяким особам, які доглядають за ними, може просто потрібна впевненість, що біль не спричинений органічною хворобою. Очікування мають бути реалістичними (наприклад, покращення функцій або відвідування школи, а не повне усунення болю).
Навчання має включати такі моменти:
- FAPD є поширеним явищем, яке зустрічається приблизно у 10-20 відсотків дітей.
- Біль від FAPD реальна; вважається, що це спричинено підвищеною чутливістю до нормальної функції шлунка та кишківника.
- Як і інші типи болю, біль у FAPDs може бути викликаний, загострений або підтримуватися екологічними (наприклад, шлунково-кишкова інфекція, ліки) і психосоціальними факторами, включаючи стрес, тривогу та соціальне підкріплення (наприклад, увага, не йти вдома).
- Інші приклади фізіологічної реакції на стрес або тривогу включають головний біль, збурювання шлунка перед тестом і нудоту, коли отримують погані новини.
- Біль від FAPDs не загрожує життю та не потребує обмеження активності.
- Лікування зосереджено на реабілітації: поверненні до нормальної діяльності, незважаючи на дискомфорт.
- Управління болем передбачає уникнення тригерів і вдосконалення навичок подолання; біль може зберігатися, але якість життя дитини та сім’ї може бути покращена.
- Цілі лікування повинні бути реалістичними (наприклад, підтримка нормальної діяльності, підвищення толерантності до симптомів).
- Хронічний біль, незалежно від етіології, може бути пов’язаний з депресією або тривогою (як причина, так і наслідок).
Повернення до школи — План повернення до школи має вирішальне значення. Прогули в школі посилюють сімейний стрес і можуть заважати успішності пацієнта в школі та соціальному функціонуванню. Навчання вдома настійно не рекомендується, якщо тільки клініцист і шкільний консультант не погодяться, що це необхідно (наприклад, на основі академічної успішності або потреб).
У більшості випадків повернення до школи має відбуватися негайно після встановлення діагнозу FAPD. Вихователям, які стурбовані емоційною реакцією своєї дитини на повернення до школи, може знадобитися допомога у формуванні та реалізації плану повернення до школи з оцінками. Їх можна заохотити співпрацювати зі школою, щоб розробити графік неповного робочого дня, щоб полегшити перехід. Перший день повернення повинен бути достатньо коротким, щоб гарантувати успіх і підвищити впевненість дитини та сім’ї в здатності дитини відвідувати школу.
Поверненню до школи може сприяти:
● Завчасне планування епізодів болю в школі (наприклад, дозвіл ходити до кабінету медсестри, поки біль не вщухне, із застереженням, що регулярне відвідування кабінету медсестри в школі може посилити симптоми).
● Надання вказівок, які допоможуть вихователю вирішити, коли дитина занадто хвора, щоб йти до школи, чи настільки хвора, щоб їй дозволили повернутися додому (наприклад, лихоманка, блювота, діарея). Регулярне відправлення дитини додому зі школи може посилити симптоми.
● Надання вказівок щодо обмеження активності, коли дитина залишається вдома після школи (наприклад, спати без телевізора чи інших розваг).
● Виявлення та усунення джерел стресу, пов’язаних зі школою (наприклад, знущання, соціальна ізоляція, невідповідне розміщення в класі).
● Для дітей із FAPD та зміненою структурою кишечника надсилання листа з проханням дозволити дитині користуватися туалетом, коли це необхідно.
● Для сімей, які мають суперечливі стосунки зі школою, пов’язані з частою відсутністю, надсилання листа для підтвердження того, що дитина пройшла обстеження щодо шлунково-кишкових симптомів, які заважали відвідуванню.

Модифікація поведінки — Поверненню до нормальної функції сприяє підсилення неболючої (здорової або адаптивної) поведінки та уникнення/припинення підсилення больової (хворої, хворобливої або дезадаптивної) поведінки. Пропозиції щодо методів модифікації поведінки можуть бути надані постачальником первинної медичної допомоги та/або, якщо необхідно, у більш формальній психотерапевтичній програмі (наприклад, когнітивно-поведінкова терапія [КПТ]).
Приклади посилення поведінки колодязя включають:
● Хвалити/винагороджувати дитину за відвідування школи або позакласних заходів (наприклад, використання діаграми наклейок для отримання винагород, узгоджених заздалегідь, за все більш тривалий період послідовного відвідування)
● Виявлення та підтримка інтересів і навичок дитини поза хворою роллю (наприклад, спортивні чи художні здібності)
● Моделювання опікуном здорових реакцій на біль у животі (наприклад, глибоке дихання)
Намагаючись підтримувати та піклуватися, особи, які доглядають за дітьми з FAPDs, можуть ненавмисно посилювати поведінку, яка викликає біль або хворобу. Приклади підсилення больової поведінки, яких слід уникати, включають:
● Звертання уваги на біль (наприклад, запитання про симптоми); у рандомізованому дослідженні спонтанні скарги на біль під час провокації симптомів (навантаження водою) майже удвічі зросли серед дітей, чиї опікуни були призначені для надання уваги (наприклад, «Я можу уявити, що це відчуває себе дуже незручно») порівняно з дітьми, чиї опікуни не отримували будь-яку конкретну відповідь.
Планування «звіту про симптоми» один раз на день може бути корисним для опікунів і дітей, які мають труднощі з негайним і повним припиненням запитувати про симптоми або повідомляти про них.
● Дозволити болю порушити нормальні функції та активність (наприклад, дозволивши дитині залишитися вдома зі школи або залишити школу, звільнивши дитину від виконання домашнього завдання).
● Дозволити дитині, яка залишається вдома після школи, дивитися телевізор або мати доступ до інших форм розваг.
Поліпшення подолання — Подолання визначається як добровільні зусилля з регулювання емоцій, думок, поведінки, фізіології та навколишнього середовища у відповідь на стресові події чи обставини. Ми пропонуємо включити психологічне лікування, щоб покращити адаптацію до лікування дітей та підлітків із FAPDs.
Навчання справлятися з болем полегшує повернення до нормального функціонування. Рандомізовані та обсерваційні дослідження надають відносно переконливі, але обмежені докази того, що психологічні втручання (наприклад, релаксація, відволікання [включаючи кероване зображення/гіпнотерапія], КПТ, біологічний зворотний зв’язок) пов’язані з покращенням переносимості болю, зниженням тривоги, підвищенням поведінки без болю та покращенням самоконтролю.
Хоча небагато досліджень прямо порівнюють психологічні втручання зі «стандартною педіатричною допомогою» (яка, як правило, передбачає освіту та заспокоєння з або без дієтичних втручань або фармакотерапії), психологічні втручання виявляються більш ефективними.
Технікам релаксації та відволікання можуть навчити кваліфіковані клініцисти первинної медичної допомоги; КПТ та біологічний зворотний зв’язок зазвичай вимагають направлення до спеціалістів із психічного здоров’я зі спеціалізованою підготовкою.
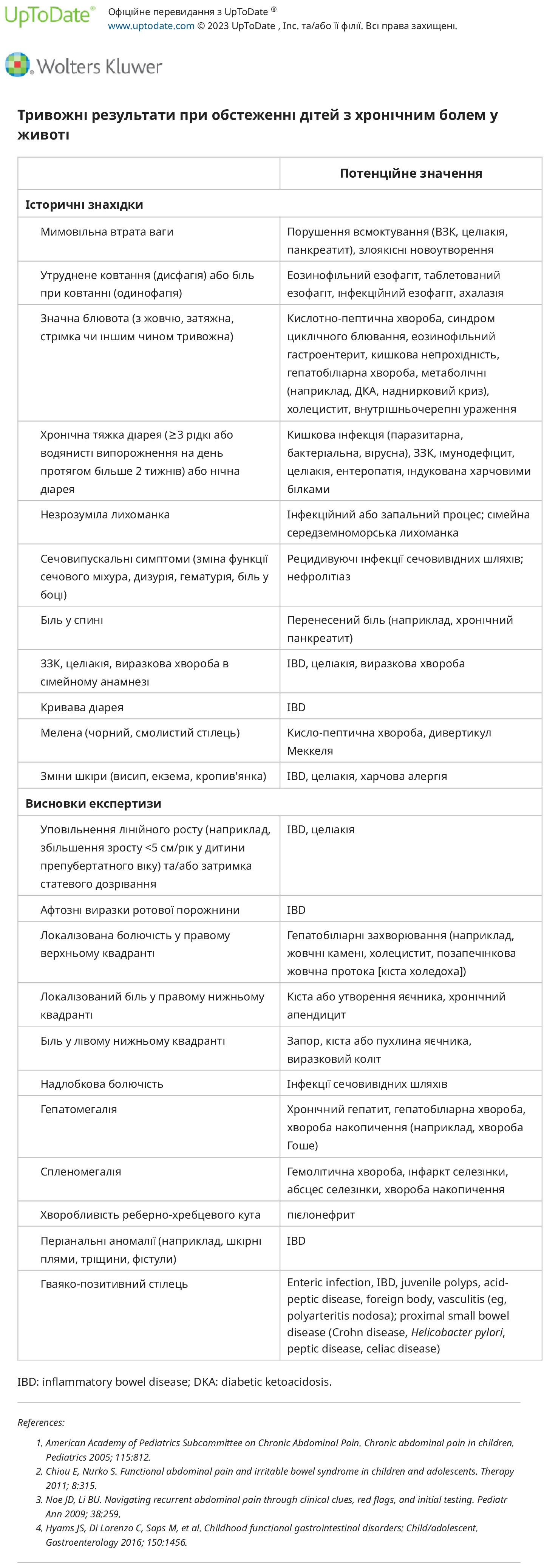
●Техніки релаксації. Дітей старшого віку та підлітків можна навчити коротких технік розслаблення м’язів, таким як вправи на глибоке дихання, які потрібно виконувати принаймні двічі на день. У разі потреби «тренером» може виступати член родини. Мета полягає в тому, щоб допомогти дитині або підлітку розслабитися, коли відчуває біль.
Прогресивна м’язова релаксація – ще одна техніка релаксації, яка передбачає систематичне напруження та розслаблення кожної групи м’язів, зосереджуючи увагу на відчутті після розслаблення м’язів.
У обсерваційних дослідженнях і метааналізах релаксаційна терапія допомогла зменшити біль і покращити функцію у дітей із FAPD.
Відволікання – відволікання відволікає увагу від болю. Техніки відволікання включають розмову, ігри, телебачення та керовані образи. У рандомізованому дослідженні спонтанні скарги на біль під час провокації симптомів (навантаження водою) були зменшені наполовину серед дітей, чиї опікуни були призначені для відволікання (наприклад, «Що б ти хотів зробити сьогодні ввечері?») уваги порівняно з дітьми. вихователям яких не було надано жодних спеціальних інструкцій.
●Керовані образи/гіпнотерапія – Керовані образи (також звані гіпнотерапією або самогіпнозом) – це техніка відволікання, за допомогою якої дитина залучається до образів і розслаблення, що відволікає увагу від хворобливих подразників. Керовані образи можуть включати уявні картини, звуки або відчуття для підвищення сприйнятливості до специфічних пропозицій та ідей, що також відомі як «інтуаційна» гіпнотерапія. Керована образна терапія/гіпнотерапія може проводитись самостійно або виконуватися кваліфікованим терапевтом.
У 2017 році в метааналізі чотирьох невеликих рандомізованих досліджень, включно з 146 дітьми з рецидивуючим болем у животі, керована образна терапія/гіпнотерапія була більш успішною (визначається як безболісна або полегшення болю, відповідно до індивідуального дослідження), ніж контрольна медикаментозна терапія (абсолютна швидкість покращення 53 проти 14 відсотків; співвідношення шансів 6,8, 95% ДІ 2,4-19). Кероване зображення/гіпнотерапія також була ефективною для зменшення інтенсивності та частоти болю та зменшення кількості пропущених дій. У довгостроковому спостереженні після одного випробування, сприятливий ефект керованого зображення/гіпнотерапії зберігався протягом п'яти років.
У подальшому дослідженні, у якому 260 дітей із FAPD (віком від 8 до 18 років) випадковим чином розподіляли на тримісячну самостійну домашню кишкову гіпнотерапію з використанням компакт-диска або індивідуальну кишкову гіпнотерапію з кваліфікованим терапевтом, підтвердили ефективність обох підходів до гіпнотерапії. Хоча самостійна гіпнотерапія була менш ефективною, ніж гіпнотерапія під керівництвом терапевта, через три місяці, результати через один і шість років були подібними. Самостійна гіпнотерапія може бути привабливим варіантом для дітей старшого віку та підлітків, які приймають підхід самостійного застосування, особливо якщо підготовлених терапевтів немає.
● КПТ – це психотерапевтичний підхід, який визначає зв’язки між поведінкою, думками та почуттями для здійснення терапевтичних змін. Індивідуальна програма КПТ може включати різні комбінації навчання, релаксації, управління стресом і методів модифікації поведінки. Надання КПТ вимагає спеціальної підготовки та зазвичай здійснюється психологом. Інші методи лікування
- Біологічний зворотний зв’язок – Біологічний зворотний зв’язок – це техніка, яка забезпечує візуальне або слухове відображення фізіологічних реакцій на біль/занепокоєння (наприклад, частота серцевих скорочень, температура шкіри), щоб можна було перевірити вплив технік релаксації ззовні.
- Йога – йога зазвичай використовується як техніка релаксації для зменшення стресу та тривоги.
УПРАВЛІННЯ ТРИГЕРАМИ
Уникнення тригерів може бути корисним у лікуванні функціональних абдомінальних болів (FAPD) у дітей і підлітків, якщо тригери можна ідентифікувати. Тригери можна визначити, запитавши про фактори, що посилюють і полегшують, або попросивши пацієнта вести щоденник болю.
Дієтичні тригери
● Харчування загалом – серед пацієнтів із FAPD та вісцеральною гіперчутливістю акт прийому їжі може бути пов’язаний із появою болю. Зазвичай пацієнти, особливо підлітки, пропускають їжу, щоб уникнути симптомів. Ця практика повинна викликати підозру на розлад харчової поведінки, коли підліток також має втрату ваги та запор.
● Специфічні тригери – Ми пропонуємо не регулярно обмежувати дієту дітей із FAPDs. За визначенням, діти з FAPDs не мають харчової алергії, яка зазвичай виключається відсутністю інших характерних симптомів (наприклад, кропив’янка, орофарингеальні симптоми). Достовірних доказів користі бракує, а обмежені дієти можуть призвести до дефіциту поживних речовин.
Однак у кожному конкретному випадку, якщо здається, що існує кореляція симптомів із певними тригерами їжі, може бути виправданим обмежене за часом дослідження усунення тригера(ів). Специфічні дієтичні тригери включають цитрусові, кофеїн, сорбіт (міститься в цукерках і гумках без цукру) і продукти, що утворюють гази (наприклад, квасоля, цибуля, селера, морква, родзинки, банани, абрикоси, чорнослив, брюссельська капуста, зародки пшениці).
Може бути важко визначити конкретні дієтичні тригери у дітей із FAPD. Незважаючи на те, що вони ідентифікують різноманітні продукти, які посилюють їхні симптоми (найчастіше повідомляють про гостру їжу, коров’яче молоко, піцу, смажену їжу, фаст-фуди, газовані напої, сир, морозиво та сальсу), вони не ідентифікують одну їжу чи інгредієнт (наприклад, пшениця, лактоза). Крім того, дієтичне обмеження може призвести до дефіциту поживних речовин; клініцисти повинні подбати про те, щоб обмежена дієта забезпечувала адекватне харчування. Може знадобитися консультація дієтолога.
Потенційні специфічні тригери включають:
- Лактоза. Випробування безлактозної дієти може бути виправданим, якщо симптоми відповідають непереносимості лактози (наприклад, судомний біль, здуття живота або гази, пов’язані з прийомом лактози). Дієта без лактози може бути досягнута шляхом виключення молока та молочних продуктів або використання замінників ферменту лактази. Пацієнти, які виключають молоко та молочні продукти, повинні бути проінформовані щодо достатнього споживання кальцію та вітаміну D. Лактозу слід відновити, якщо симптоми не покращуються після двох тижнів виведення лактози. Уникання лактози можна продовжувати у дітей, симптоми яких покращуються під час безлактозної дієти. Для тих пацієнтів, у яких користь від уникнення лактози неясна, може бути корисним провести лактозо-водневий дихальний тест.
Чи безлактозна дієта зменшує частоту нападів болю у дітей і підлітків із FAPD, невідомо. Дослідження, що оцінюють вплив безлактозної дієти або дієти з низьким вмістом лактози у дітей із FAPD, дали неоднозначні результати. - Глютен/пшениця – Пацієнти з FAPD можуть пов’язувати свої симптоми з вуглеводами, відмінними від лактози. Безглютенові дієти стали популярними через збільшення занепокоєння щодо ролі чутливості до глютену або целіакії в хронічному болі в животі. Однак целіакія є рідкісною причиною хронічного болю в животі у дітей. У проспективному дослідженні лише 1 із 227 дітей віком ≥5 років із рецидивуючим болем у животі виявили целіакію.
Нецеліакічна чутливість до глютену (також називається синдромом непереносимості пшениці) може бути пов’язана з шлунково-кишковими симптомами у невеликої підгрупи дітей. У проспективному багатоцентровому дослідженні у 1114 дітей із хронічними шлунково-кишковими симптомами симптоми корелювали з глютеном у 36 (3,3 відсотка); серед 28, які пройшли рандомізоване подвійне сліпе плацебо-контрольоване перехресне введення глютену, 11 відреагували позитивно. Пшениця та глютен також були пов’язані з шлунково-кишковими симптомами у дорослих пацієнтів із синдромом подразненого кишківника (СПК) без ознак целіакії. Потрібне подальше розуміння поширеності та механізму чутливості не целіакії до пшениці, перш ніж можна буде рекомендувати уникати глютену для дітей та підлітків із FAPD. Рандомізованих досліджень уникнення глютену у дітей із FAPD бракує. - FODMAP – FODMAP – це ще одна група вуглеводів, які вважаються потенційними тригерами FAPDs. FODMAP – це вуглеводи з коротким ланцюгом, які погано засвоюються шлунково-кишковою системою і можуть призвести до газоутворення, розтягнення товстого кишечника, здуття живота та болю в животі. Є деякі докази того, що дієта з низьким вмістом FODMAP може бути корисною для дорослих із СПК.
Проте інформація про роль FODMAP у дітей з FAPD обмежена. Кілька досліджень, які зосереджувалися на непереносимості фруктози у дітей із FAPD, повідомляли про зменшення болю при обмеженні фруктози, але ці дослідження не включали контрольну групу. У рандомізованому перехресному дослідженні 48-годинної дієти з низьким і високим вмістом FODMAP у 33 дітей (від 7 до 17 років) із СПК дієта з низьким вмістом FODMAP була пов’язана з деяким покращенням шлунково-кишкових симптомів (наприклад, здуття живота, нудота) та зниження виробництва водню в диханні. Середні показники тяжкості болю зменшилися на обох дієтах порівняно з базовим рівнем.
Хоча немає достатніх доказів за або проти ефективності та безпеки регулярного використання дієти з низьким вмістом FODMAP для лікування дітей із FAPD, потенційним показанням є надмірне газоутворення.
Дієтичні обмеження у дітей слід вводити після консультації з дієтологом, оскільки вони можуть вплинути на адекватність харчування, їх важко дотримуватися та сприяти спотворенню харчування у вразливих дітей і підлітків. У дорослих дієта з низьким вмістом FODMAP зазвичай включає три фази: повне виведення (зазвичай протягом двох-шести тижнів); повторне введення (під час якого використовуються окремі вуглеводи FODMAP, щоб визначити, які з них найбільш пов’язані із симптомами); та персоналізація (пристосування дієти з низьким вмістом FODMAP, щоб насамперед уникнути тригерів FODMAP, визначених раніше). Як альтернатива, спрощена версія дієти, яка називається «щадною дієтою FODMAP» або «підходом знизу», яка спочатку виключає лише кілька продуктів із високою концентрацією FODMAP і поступово виключає з раціону додаткові продукти FODMAP, доки симптоми не зникнуть. було запропоновано полегшити лікування дітей, щоб уникнути надмірного обмеження та/або покращити прихильність.

Тривога. Виявлення супутньої тривоги у пацієнтів із FAPD є критично важливим. За оцінками, тривожні розлади вражають від 42 до 85 відсотків педіатричних пацієнтів із FAPD. Важливо пояснити пацієнту та особам, які доглядають за ним, що перевірка тривоги не означає, що FAPD є проявом психологічного розладу, а скоріше те, що тривога та FAPD можуть співіснувати через спільні причинні фактори або як наслідок боротьби з хронічним болем. Крім того, є докази того, що тривога може бути пов’язана з більш високим рівнем функціональних порушень у дітей і підлітків із FAPDs.
МЕНЕДЖМЕНТ СИМПТОМІВ
Біль у животі. Медичні втручання, які можна поєднувати із загальними поведінковими стратегіями лікування болю в животі у дітей із функціональними абдомінальними розладами (FAPD), включають пробіотики, добавки з водорозчинною клітковиною (наприклад, псиліум/лушпиння іспагули) або м’яту перцеву,масло. Хоча ці втручання не були добре закріплені в алгоритмах лікування, вони мають низький ризик шкоди, і короткострокові випробування є розумними. Ці втручання можна спробувати в будь-якому порядку або комбінації. Зазвичай ми починаємо з пробіотиків у пацієнтів із нормальним випорожненням і пробіотиків із клітковиною у пацієнтів із запорами.
●Пробіотики. Пробіотики в поєднанні із загальними стратегіями лікування можуть бути корисними для лікування болю в животі, але механізм дії неясний. Зміни в комменсальних бактеріальних популяціях були причетні до порушення моторики, вісцеральної гіперчутливості, аномального бродіння в товстій кишці та імунологічної активації. Пробіотики можуть покращити шлунково-кишкові симптоми, відновлюючи мікробний баланс у кишечнику через метаболічну конкуренцію з патогенами, посилюючи слизовий бар’єр кишечника або змінюючи запальну реакцію кишечника.
Найбільш ефективний пробіотичний штам, доза або тривалість лікування не встановлені. З огляду на те, що пробіотики, як правило, безпечні, рішення про використання пробіотиків зазвичай ґрунтується на потенційних перевагах, витратах і перевагах пацієнта/родини. Коли приймається рішення спробувати пробіотики, ми пропонуємо комерційні препарати штамів, які мають деякі докази користі при шлунково-кишкових захворюваннях (наприклад, Lactobacillus reuteri DSM 17938 у дозі ≥10 8 колонієутворюючих одиниць на день). Ми пропонуємо спробувати пробіотик протягом чотирьох-шести тижнів до повторної оцінки симптомів болю в животі та/або ненормального випорожнення.
У 2023 році метааналіз шести рандомізованих досліджень за участю 554 дітей із ФАП показав, що пробіотики були ефективнішими, ніж плацебо, для успіху лікування (50 проти 33 відсотків; співвідношення ризиків 1,57, 95% ДІ 1,05-2,36), на основі доказів із низькою достовірністю. Аналіз не зміг визначити, чи є пробіотики більш ефективними, ніж плацебо, для повного усунення болю. Він також не зміг розрізнити ефективність різних пробіотиків, але більшість даних стосувалися L. reuteri або Lactobacillus rhamnosus GG. Незважаючи на те, що жодних випадків серйозних побічних ефектів не було зареєстровано, неможливо зробити висновки через низький рівень достовірності через неточність через дуже низькі цифри та ризик упередження.
● Клітковина. Дітям із FAPD та зміненим випорожненням може бути виправданим додавання водорозчинної клітковини на додаток до загальних стратегій лікування. Точні механізми, за допомогою яких клітковина може зменшити біль у животі, недостатньо вивчені, але можуть включати модифікацію кишкової мікробіоти, змінений склад стільця та газів та/або прискорений шлунково-кишковий транзит. Переваги харчових волокон слід порівнювати з низьким, але потенційним ризиком збільшення здуття живота та болю.
Оптимальна доза, тип клітковини та тривалість лікування дітей із болем у животі не встановлені. Зазвичай ми пропонуємо використовувати водорозчинну клітковину (наприклад, гідрофільний муцилоїд подорожника [лушпиння іспагули]) у дозі від 1,5 до 12,5 грамів на день, залежно від розміру пацієнта та базового споживання клітковини з їжею. Розумна ціль для загального споживання харчових волокон — це вік дитини в роках плюс 5–10 грамів на день. Ми продовжуємо випробування добавок клітковини протягом принаймні чотирьох тижнів, перш ніж визначити, чи відбулося покращення частоти та тяжкості болю в животі.
● Олія м’яти перцевої. Олія м’яти перцевої є ще одним втручанням, яке може бути корисним у поєднанні із загальними стратегіями лікування абдомінального болю у дітей із FAPD.
Хоча докази обмежені, вважається, що олія м’яти перцевої зменшує спазми гладкої мускулатури шлунково-кишкового тракту. У 2022 році систематичний огляд фармакологічного лікування FAPDs у дітей включав два рандомізовані контрольовані дослідження, в яких оцінювалося 2-4 тижні лікування олією м’яти перцевої, і було знайдено докази з низьким рівнем достовірності того, що олія м’яти перцевої зменшувала вираженість, тривалість і частоту болю порівняно з плацебо або лактолом (Bacillus коагулянти плюс фруктоолігосахариди). Жоден пацієнт не припинив лікування через побічні ефекти. У 2011 році метааналіз рандомізованих досліджень за участю пацієнтів старше 12 років прийшов до висновку, що олія перцевої м’яти ефективна в лікуванні синдрому подразненого кишківника (СПК).
Капсули з олією м’яти доступні у продажу. В обох включених дослідженнях олію м’яти перцевої застосовували у вигляді pH-залежних капсул, покритих кишковорозчинною оболонкою (187 мг три рази на день для дітей вагою <45 кг; 374 мг тричі на день для дітей вагою >45 кг). Надмірне споживання олії м’яти перцевої може призвести до загострення гастроезофагеального рефлюксу та асоціюється з інтерстиціальним нефритом і гострою нирковою недостатністю.
● Інші спазмолітики – інші спазмолітики включають дротаверин, мебеверин, тримебутин, гіосціамін і дицикломін. У той час як спазмолітичні препарати перевершують плацебо в лікуванні дорослих із СПК, кілька досліджень оцінювали ефективність спазмолітиків у лікуванні FAPD у дітей. Систематичний огляд фармакологічного лікування FAPD у дітей 2022 року включав три рандомізовані контрольовані дослідження, у яких оцінювали три-чотири тижневе лікування іншими спазмолітиками (дротаверин, мебеверин, тримебутин) і виявив докази низької достовірності того, що ці препарати покращують ефективність лікування та зменшують епізоди болю. Троє учасників припинили прийом мебеверину через побічні ефекти (сонливість, нервозність, нудота), а один учасник припинив прийом дротаверину через кропив’янку.
Тривале застосування інших спазмолітичних препаратів у дітей може бути обмежене антихолінергічними побічними ефектами (наприклад, сухість у роті, розмитість зору). Необхідні додаткові дослідження безпеки та ефективності, перш ніж спазмолітичні препарати можна буде регулярно рекомендувати дітям із FAPD.
● Інші втручання
- Антидепресанти. Ми пропонуємо не призначати регулярно антидепресанти дітям і підліткам із FAPD, якщо вони не відповідають діагностичним критеріям асоційованої депресії. Вважається, що значна частина болю в животі при функціональних розладах пов’язана з ненормальним сприйняттям вісцеральних відчуттів. Ліки, спочатку показані для лікування депресії та тривоги, були досліджені для лікування FAPD через їх вплив на нейромедіатори центральної та кишкової нервової системи, такі як ацетилхолін і серотонін. Проте дослідження цих препаратів у дітей і підлітків із FAPD обмежені, і невідомо, чи ефективні антидепресанти при лікуванні FAPD у дітей.
- Ципрогептадин – ципрогептадин є препаратом із багатьма механізмами дії, включаючи антигістамінні, антихолінергічні та антисеротонінергічні властивості, а також можливу дію на блокаду кальцієвих каналів. Його використовували для стимуляції апетиту та профілактики болю та блювоти при абдомінальній мігрені та синдромі циклічної блювоти. У ретроспективних дослідженнях повідомлялося, що ципрогептадин безпечний і ефективний для лікування FAPD і диспепсичних симптомів у дітей. У рандомізованому дослідженні за участю 29 дітей і підлітків із FAPD у 86 відсотків групи, яка отримувала ципрогептадин протягом двох тижнів, спостерігалося покращення або зникнення болю в животі порівняно з 35,7 відсотками в групі плацебо. Ці результати мають бути підтверджені більшими додатковими дослідженнями, перш ніж ципрогептадин можна буде регулярно рекомендувати для лікування FAPDs.
•Терапія нейростимуляцією вушної раковини – у терапії нейростимуляцією вушної раковини черезшкірну стимуляцію електричним нервовим полем (PENFS) проводять за допомогою неінвазивного пристрою, який носять за вухом, щоб націлити центральні шляхи болю, залучені до посилення болю. У рандомізованому фіктивно-контрольованому дослідженні за участю 115 підлітків нейростимуляція вушної раковини зменшила тяжкість, частоту та тривалість абдомінального болю без серйозних побічних ефектів у підлітків із FAPD. В іншому рандомізованому фіктивно-контрольованому дослідженні за участю 50 підлітків із СПК нейростимуляція вушної раковини зменшила показники болю в животі та покращила загальне самопочуття. На додаток до покращення самооцінених симптомів абдомінального болю та нудоти, PENFS було пов’язано зі змінами у вісцеральній чутливості за допомогою завдання водного навантаження, актіграфічних та суб’єктивних показників сну та інших психологічних факторів, таких як катастрофічні та соматичні скарги.
Незважаючи на те, що ці висновки є багатообіцяючими, і Управління з контролю за якістю харчових продуктів і медикаментів США надало дозвіл на продаж пристрою для полегшення ФАП у підлітків віком від 11 до 18 років із СПК, необхідні додаткові дослідження для підтвердження результатів, визначення оптимального налаштування та тривалість лікування та визначити оптимальну цільову популяцію до того, як PENFS можна буде регулярно рекомендувати дітям із FAPD.

Диспепсія — це біль або дискомфорт, що зосереджуються в епігастральній ділянці або верхній частині живота. Дискомфорт може характеризуватися повнотою, раннім відчуттям насичення, здуттям живота, нудотою, блювотою або блювотою. Біль або дискомфорт можуть посилюватися під час їжі. У дітей із функціональною диспепсією домінуючим симптомом є диспепсія.
Ми пропонуємо наступні заходи для симптоматичного лікування функціональної диспепсії:
● Невеликі часті прийоми їжі
● Уникання їжі, напоїв і ліків, які посилюють симптоми (наприклад, їжа з високим вмістом жиру, напої з кофеїном, нестероїдні протизапальні препарати).
Ми пропонуємо не регулярно використовувати фармакологічну терапію (наприклад, H2-блокатори, інгібітори протонної помпи) для дітей та підлітків із функціональною диспепсією. Ми пропонуємо не регулярно використовувати прокінетичні агенти (наприклад, метоклопрамід, домперидон, еритроміцин) у лікуванні дітей та підлітків із FAPD. Існує мало доказів ефективності та потенційних побічних ефектів, особливо метоклопраміду та домперидону.
Діарея. Діарея може бути домінуючим симптомом у дітей із СПК. Діти та підлітки, у яких діарея складається з ≥3 рідких або рідких випорожнень на день протягом більше двох тижнів (що є тривожним симптомом), потребують обстеження на наявність органічних захворювань.
З практичної точки зору, для клініциста може бути корисним надати до школи записку з проханням дозволити дитині чи підлітку з FAPD і діареєю користуватися туалетом, коли це необхідно. Крім того, пацієнту важливо підтримувати достатнє споживання рідини.
Ми пропонуємо не регулярно обмежувати дієту дітей із FAPD та діареєю. Проте, в кожному конкретному випадку, якщо існує кореляція діареї з певним харчовим тригером (наприклад, лактоза, сорбітол), може бути виправданим обмежене за часом дослідження усунення тригера.
Ми рекомендуємо не регулярно використовувати препарати, що пригнічують моторику, для дітей або підлітків із FAPD та діареєю. Діарея, пов’язана з FAPD, як правило, короткочасна, і засоби, що пригнічують моторику, зазвичай не рекомендуються для лікування інших типів діареї (наприклад, інфекційної, пов’язаної з прийомом антибіотиків) у дітей.
Запор — Виявлення основного запору є критичним для пацієнтів із FAPD.
ПОКАЗИ ДО НАПРАВЛЕННЯ
● Тривожні ознаки – дітей, у яких виникають тривожні ознаки, може знадобитися направлення до гастроентеролога або іншого спеціаліста для оцінки та/або лікування.
● Інвалідність, пов’язана з болем у животі. Дітям із інвалідністю, пов’язаною з болем у животі (наприклад, пропущені шкільні чи позакласні заходи, тривога, депресія), може бути корисним направлення до психіатра для консультування або терапії та реабілітації, включаючи когнітивно-поведінкову терапію (КПТ).
Направлення до педіатра з питань розвитку та поведінки (для дітей молодшого віку), фахівця з підліткової медицини (для підлітків), постачальника психіатричних послуг або багатопрофільної клініки може бути корисним у забезпеченні стратегій повернення до повсякденної діяльності та уникнення триваючої інвалідності, спричиненої болем.
Деякі пацієнти та сім’ї, особливо ті, які продовжують зосереджуватися на пошуку органічної етіології, можуть протистояти направленню до терапевта чи консультанта. Педіатр може сприяти направленню, пояснюючи родині їхні обмеження в лікуванні без додаткової допомоги терапевта. Постачальник повинен обговорити потенційну користь для сім'ї від консультування з терапевтом, який може допомогти дитині впоратися з болем і може підтримати необхідні зміни в житті дитини (наприклад, повернення до школи).
● Рефрактерний запор – Дітям із запорами, які не піддаються первинній медичній допомозі, може бути корисним направлення до гастроентеролога.
ПРОГНОЗ
Функціональні абдомінальні болі (FAPD) зникають у більшості дітей. У систематичному огляді 18 проспективних досліджень, включаючи 1331 дитину з хронічним болем у животі, біль у животі зберігався у 29,1 відсотка (95% ДІ 28,1-30,2) при медіані спостереження протягом п’яти років (діапазон від 1 до 29). У проспективному дослідженні 132 дітей із FAPD, які спостерігалися в гастроентерологічній клініці, симптоми покращилися приблизно у 85 відсотків пацієнтів через два місяці, а покращення зберігалося через один і п’ять років.

РЕЗЮМЕ ТА РЕКОМЕНДАЦІЇ
●Термінологія. Діагноз функціональних абдомінальних болів (FAPD) можна діагностувати у дітей, які мають усі з перерахованих нижче ознак:
- Хронічний (≥2 місяців) біль у животі
- Немає сигналів тривоги
- Нормальний фізикальний огляд
- Зразок калу негативний на приховану кров
Кілька функціональних шлунково-кишкових розладів у дитинстві мають характерні симптоми, включаючи синдром подразненого кишечника (СПК), функціональну диспепсію та абдомінальну мігрень.
● Підхід до лікування. Метою лікування FAPD у дітей та підлітків є повернення до нормальної функції, а не повне усунення болю (реабілітаційний підхід). Лікування здійснюється індивідуально відповідно до поведінки дитини та сім’ї, тригерів і симптомів. Більшість випадків можна лікувати в закладі первинної медичної допомоги.
Загальні стратегії управління
- FAPD найкраще лікувати в контексті біопсихосоціальної моделі догляду. Пацієнт і сім'я повинні вірити, що їхні скарги та занепокоєння сприймаються серйозно. Встановлення терапевтичних стосунків, навчання пацієнта та сім’ї та план повернення до школи є важливими компонентами лікування.
- Поверненню до нормальної функції сприяє посилення неболючої (здорової або адаптивної) поведінки та уникнення посилення болю або болю (хвороба, хвороба, дезадаптивна) поведінки.
- Ми пропонуємо психологічні втручання (наприклад, релаксацію, відволікання, кероване уявлення, когнітивно-поведінкову терапію [КПТ], щоб покращити пристосування та зменшити стрес/тривожність у дітей і підлітків із ФАПД (клас 2B).
● Дієтичні тригери – Ми пропонуємо не регулярно обмежувати дієту дітей і підлітків із FAPD (ступінь 2C). Однак у кожному конкретному випадку може бути виправданим проведення обмеженого за часом випробування щодо уникнення певних харчових тригерів (наприклад, лактози, сорбіту).
Управління симптомами
- Медичні втручання, які можна поєднувати з поведінковими втручаннями, включають випробування пробіотиків, додавання водорозчинної клітковини (наприклад, подорожника / лушпиння іспагули) або олії перцевої м’яти. Ці втручання можна спробувати в будь-якому порядку або комбінації. Зазвичай ми починаємо з пробіотиків у пацієнтів із нормальним випорожненням і пробіотиків із клітковиною у пацієнтів із запорами.
- Ми пропонуємо невеликі часті прийоми їжі та уникання їжі, напоїв і ліків, які посилюють симптоми, а не фармакологічну терапію для початкового лікування функціональної диспепсії (ступінь 2C).
- Ми пропонуємо не регулярно використовувати препарати, що пригнічують моторику, для дітей або підлітків із ФАП та діареєю (ступінь 2C).
Подальше спостереження та показання для направлення – Регулярне спостереження необхідне для підтримки терапевтичних стосунків, забезпечення постійного навчання та заспокоєння, моніторингу відповіді на втручання та моніторингу розвитку тривожних знахідок.
Дітям із постійним болем у животі, що впливає на функціонування пацієнта та сім’ї, може бути корисно направити до психіатра чи іншого спеціаліста. Діти, у яких виникають тривожні ознаки, потребують обстеження на наявність органічних захворювань.
● Прогноз – у більшості дітей FAPD зникає протягом кількох місяців.
ДЖЕРЕЛО: https://www.uptodate.com/
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу

Домашній пристрій для діагностики хвороб з ...
Кишечник під тиском: клінічний випадок роз ...

Дослідження показало, що організм по-різно ...

Клінічна загадка: водяниста діарея

Новий препарат для лікування ожиріння демо ...

Дані, що змінюють клінічну практику при га ...


