Дані, що змінюють клінічну практику при гастроезофагеальній аденокарциномі
Дата публікації: 16.01.2026
Автори: Відкриті джерела , Редакція платформи «Аксемедін»
Ключові слова: біспецифічні антитіла, загальна виживаність, гастроезофагеальна аденокарцинома, HER2-позитивний рак, занідатамаб, тислелізумаб, виживаність без прогресування, перша лінія терапії

Нові результати дослідження III фази продемонстрували, що схеми лікування, які включають занідатамаб, забезпечують статистично значуще подовження виживаності без прогресування захворювання (ВБП) та загальної виживаності в першій лінії терапії у пацієнтів із HER2-позитивною місцево-поширеною або метастатичною гастроезофагеальною аденокарциномою.
Дослідження показало, що застосування занідатамабу в комбінації з хіміотерапією, з інгібітором PD-1 тислелізумабом або без нього, призводило до медіани ВБП понад 12 місяців та медіани загальної виживаності понад 24 місяці. Це перше дослідження III фази, у якому вдалося досягти таких результатів у цій популяції пацієнтів, повідомила керівниця дослідження доктор медичних наук Олена Елімова з Онкологічного центру принцеси Маргарет (Торонто, Канада) під час пресбрифінгу на симпозіумі ASCO Gastrointestinal Cancers Symposium 2026.
«Це результати, що змінюють практику та пропонують новий терапевтичний варіант для пацієнтів із HER2-позитивним раком верхніх відділів шлунково-кишкового тракту», — зазначила доктор медичних наук Рачна Шрофф, співкерівниця клінічної дослідницької групи з пухлин шлунково-кишкового тракту Онкологічного центру Університету Аризони (Тусон, США).
Задоволення нагальної клінічної потреби
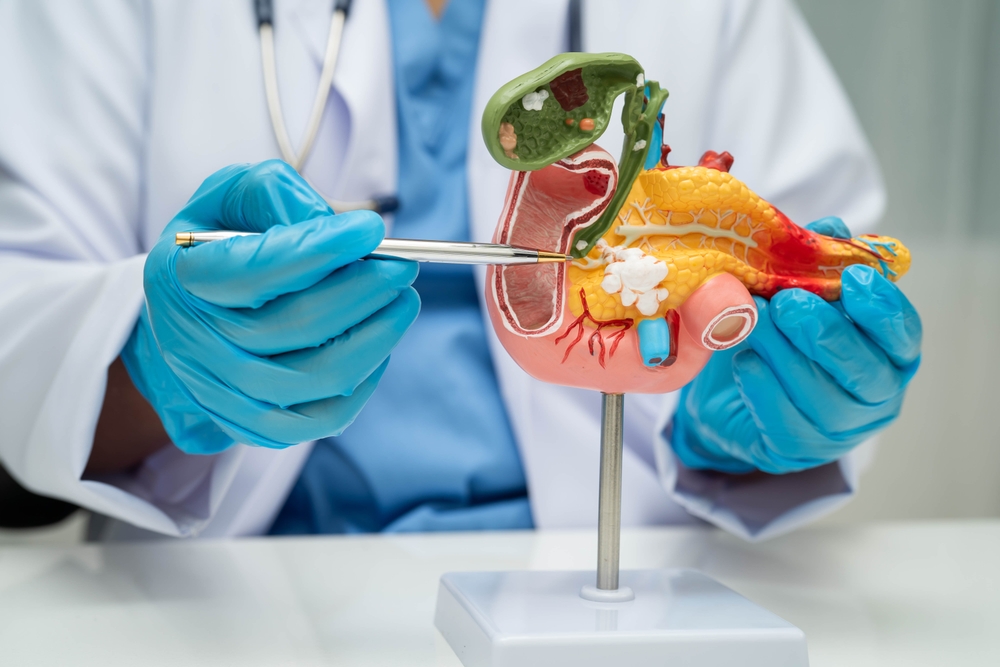
Близько 20% пацієнтів із гастроезофагеальною аденокарциномою, включно з раком шлунка, гастроезофагеального переходу та стравоходу, мають HER2-позитивний статус пухлини. У значної частини пацієнтів із метастатичною формою захворювання прогресування відбувається протягом першого року лікування.
За словами Олени Елімової, у цій когорті існує «нагальна» незадоволена потреба в нових стратегіях, спрямованих на HER2, які дозволили б покращити довгострокові клінічні результати.
Занідатамаб є подвійним біспецифічним антитілом, спрямованим проти HER2, яке одночасно зв’язується з двома різними позаклітинними доменами рецептора HER2 (домени 2 та 4). Такий механізм дії призводить до зшивання білків HER2, кластеризації рецепторів на поверхні клітини та реалізації кількох протипухлинних механізмів дії.
Дизайн і характеристика дослідження
У дослідженні взяли участь 914 пацієнтів із раніше нелікованою метастатичною або місцево-поширеною неоперабельною гастроезофагеальною аденокарциномою. Пацієнтів було рандомізовано у співвідношенні 1:1:1 до трьох груп лікування:
- занідатамаб у комбінації з хіміотерапією та тислелізумабом
- занідатамаб у комбінації з хіміотерапією
- трастузумаб у комбінації з хіміотерапією (стандарт лікування для цієї категорії пацієнтів)
Хіміотерапевтичні режими включали капецитабін у поєднанні з оксаліплатином або, за вибором лікаря, 5-фторурацил у поєднанні з цисплатином.
Усі пацієнти, які отримували занідатамаб, отримували профілактику діареї — відомого побічного ефекту цього препарату. Також усі учасники дослідження отримували стандартну профілактику для запобігання інфузійним реакціям.
Демографічні та клінічні характеристики були збалансованими між групами. Більшість пацієнтів були чоловіками; близько половини походили з азійських регіонів; у більшості було de novo метастатичне захворювання. У 83% учасників визначався статус HER2 IHC 3+, а приблизно у 30% показник позитивності площі пухлини становив менше 1%.
Ефективність лікування
Після медіанного періоду спостереження понад 2 роки виживаність без прогресування була статистично значуще вищою в обох групах, що отримували занідатамаб, порівняно з групою трастузумабу. Медіана ВБП становила 12,4 місяця у пацієнтів, які отримували занідатамаб у поєднанні з хіміотерапією з тислелізумабом або без нього, порівняно з 8,1 місяця у групі трастузумабу.
Занідатамаб знижував ризик прогресування захворювання або смерті на 35% у групі занідатамаб + хіміотерапія (HR 0,65; p < 0,0001) та на 37% у групі потрійної терапії (HR 0,63; p < 0,0001). Переваги спостерігалися в усіх ключових підгрупах, зокрема залежно від географічного регіону та статусу PD-L1.
Перегляньте запис:
Загальна виживаність та протипухлинна активність
Під час першого проміжного аналізу відзначено чітку тенденцію до покращення загальної виживаності при застосуванні занідатамабу в поєднанні з хіміотерапією порівняно з трастузумабом (медіана 24,4 проти 19,2 місяця; HR 0,80; p = 0,0564).
При застосуванні занідатамабу у комбінації з тислелізумабом та хіміотерапією медіана загальної виживаності становила 26,4 місяця проти 19,2 місяця у контрольній групі (HR 0,72; p = 0,0043).
Відповіді на лікування у групах із занідатамабом були глибшими та тривалішими. Медіана тривалості відповіді наближалася до 21 місяця у групі потрійної терапії, близько 14 місяців — у групі занідатамаб + хіміотерапія та близько 8 місяців — у групі трастузумабу.
Безпека та переносимість
Загальні профілі безпеки відповідали відомим профілям кожного з методів лікування. Побічні ефекти III ступеня або вище спостерігалися у 72% пацієнтів у групі потрійної терапії та приблизно у 59% пацієнтів у двох інших групах.
Припинення лікування через побічні ефекти відбулося у 12% пацієнтів, які отримували потрійну терапію, у 8,5% пацієнтів у групі занідатамаб + хіміотерапія та у 2,3% пацієнтів у групі трастузумабу. Летальні побічні явища, пов’язані з лікуванням, зафіксовані у одного пацієнта в групі занідатамаб + хіміотерапія, у семи пацієнтів (2,4%) у групі потрійної терапії та у чотирьох пацієнтів (1,3%) у контрольній групі.
Діарея була найпоширенішим побічним явищем у всіх групах, однак терапія, спрямована на HER2, рідко припинялася через цей побічний ефект.
Клінічні перспективи
Дослідники планують провести додатковий проміжний аналіз загальної виживаності в середині 2026 року для комбінації занідатамабу з хіміотерапією.
ДЖЕРЕЛО: Medscape
На платформі Accemedin багато цікавих заходів! Аби не пропустити їх, підписуйтесь на наші сторінки! Facebook. Telegram. Viber. Instagram.
Щоб дати відповіді на запитання до цього матеріалу та отримати бали,
будь ласка, зареєструйтеся або увійдіть як користувач.
Реєстрація
Вхід
Матеріали з розділу

Бактерії ротової порожнини як чинник розви ...
Варіанти скринінгу колоректального раку: ч ...

Рак стравоходу та стравохідно-шлункового п ...
Нове дослідження визначає, як рак печінки, ...

Кетогенна дієта при розсіяному склерозі: н ...

Клінічне завдання. Втрата маси тіла. Діагн ...